明 細 書 メラニン凝集ホルモン拮抗剤 技術分野
本発明は、 肥満症の予防 ·治療剤などとして有用なメラニン凝集ホルモン 拮抗剤に関する。 景技術
摂食行動はヒトを含め、 多くの生物にとって、 欠くことの出来ない行為で ある。 そのため、 摂食行動に異常をきたすと正常な生命活動に狂いが生じ、 疾患につながる場合が多い。 近年、 食事環境の変化に伴い、 肥満が社会的な 問題になりつつある。 肥満はさらに糖尿病、 高血圧、 動脈硬化症などの生活 習慣病の重大なリスクファクターであるだけでなく、 体重増加が膝などの関 節に過度の負担を与えることにより、 関節炎や疼痛をもたらすことも広く知 られている。 また、 ダイエットブームなどにより、 減量を望む潜在人口も多 い。 一方、 遺伝的あるいはストレスなどの神経症などが原因で起きる過食症 などの摂食障害も多数報告されている。
そのため、 肥満の予防 ·治療剤あるいは摂食抑制剤の開発研究が古くから 活発に進められており、 中枢性食欲抑制薬としてはマジンドール (mazindol) が市販されている。
一方、 レブチンに代表される食欲調節因子が最近数多く見いだされつつあ り、 これらの食欲調節因子の働きを制御する新たな抗肥満薬あるいは食欲抑 制薬の開発が進められている。 なかでもメラニン凝集ホルモン (以下、 MCH と略記することもある) は、 視床下部由来のホルモンで、 食欲宂進作用を有 することが知られている。さらに、 MCHノックアウトマウスは日常行動が正常 であるにもかかわらず、 正常マウスと比べて、 摂食量が有意に減少し、 かつ 体重も軽いことが報告されている [ネイチヤー (Nature) 、 396巻、 670頁、 1998年] 。 これらのことから、 MCH拮抗薬ができれば優れた食欲抑制薬ある
いは抗肥満薬になると期待されているが、未だ MCH拮抗作用を有する化合物、 特に非ペプチド型化合物は知られていない。 ァミン誘導体として、 以下の化合物が知られている。
1)特表平 10— 504315には、 5-HT1Dアンタゴニスト活性を有す る式
〔式中、 R1は、 水素、 ハロゲン、 Ci-eアルキル、 C3_6シクロアルキル、 COCj— 6アルキル、 — 6アルコキシ、 ヒドロキシ、 ヒドロキシ ( 6アル キル、 ヒドロキシ Ci— 6アルコキシ、 ァシル、 ニトロ、 トリフルォロメチル、 シァノ、 CH〇、 SR9、 S〇R9、 S02R9、 SOaNR^R11, CO^1 NR^0SO2R11^ CONR^R1^ CO^R^R11, CONR10(C
(CH
2)
p C ONR
10 R
1 (CH
2)
アルキル、 C〇
2 (CH
2)
p OR
1。、 CONHNR^R
11^ NR^R
11^ NR^CO^
11, NR
10CONR
10 RII、 CR
10 = NOR
X 1, CNR
10 = NOR
X 1 (ここに、 R
10および R
11 は独立して水素または C;_
6アルキルであり、 pは 1ないし 4である) であ り ;
R2および R3は独立して、 水素、 ハロゲン、 ^— 6アルキル、 C3— 6シクロア ルキル、 C 3— 6シクロアルケニル、 — 6アルコキシ、 ァシル、 ァリール、 ァ シルォキシ、 ヒドロキシ、 ニトロ、 トリフルォロメチル、 シァノ、 ヒドロキ シ ( 6アルキル、 C , _ 6アルキル O C! _ 6アルキル、 CO2R10、 CON R^R11, N ^R11 (ここに、 R 10および R 11は独立して水素または _6アルキルである) であり ;
R 4および R 5は独立して、 水素または アルキルであり ;
R6は、 水素、 ハロゲン、 ヒドロキシ、 アルキルまたは アルコキ シであり ; '
R7および R8は独立して、 水素、 ^— 6アルキル、 ァラルキル、 または結合 している窒素原子と一緒になつて、 酸素、 窒素または硫黄から選択される 1 または 2個の複素原子を含有する所望により置換されていてもよい 5ないし 7員複素環を形成し;
Aは酸素、 S(〇)q (ここに、 qは 0、 1または 2である) 、 CR4 = CR5 または CR4R5 (ここに、 R4および R5は独立して水素または Cト 6アルキ ルである) であるか、 または Aは NR 12 (ここに、 !^^ま水素または。 ^ アルキルである) であり ;
Bは(CR13R14)q (ここに、 Qは 2、 3または 4であり、 R13および R14 は独立して水素または 6アルキルである) であるか、 または Bは(CR13 R14) r.-D (ここに、 rは 0、 1または 2であり、 Dは酸素、 硫黄または C R13 = CR14である) であり ;
mは 1ないし 4であり ;および nは 1または 2を意味する] で示される化合 物またはその塩が記載されている。
具体例としては、 1— (4 '一ァセトアミドメチル— 2 '—メチルビフエ ニル一 4一力ルポニル) 一5—クロロー 2, 3—ジヒドロ一 6— (2—ジメ チルアミノエトキシ) 一1H—インド一ルゃ 1— (4 '—ァセトアミドメチ ル— 2 -—メチルビフエ二ルー 4—力ルポニル) 一 2, 3—ジヒドロ— 6— ( 3—ジメチルァミノプロピル) 一 5—エトキシー 1 H—インドールなどが 記載されている。
2) 特表平 9一 506885 (WO 95/17398) には、 5- HT1D アンタゴニスト活性を有する式
R1 R2
A—(CRSR6^— NR7R8
〔式中、 Pは酸素、 窒素または硫黄から選択される 1または 3個のへテロ原 子を含有する 5ないし 7員複素環であり ;
R\ R2および R3は、 独立して、 水素、 ハロゲン、 ^— 6アルキル、 C3_6 シクロアルキル、 C 3— 6シクロアルケニル、 アルコキシ、 ァシル、 ァリ ール、 ァシルォキシ、 ヒドロキシ、 ニトロ、 トリフルォロメチル、 シァノ、 C02R9、 CONR^R11, NR10R1X (ここに、 R9、 R10および R11 は、 独立して、 水素または ^-eアルキルである) であり ;
R4は、 水素、 ハロゲン、 ヒドロキシ、 6アルキルまたは Ci_6アルコキ シである) であり ;
R5および R6は独立して、 水素または アルキルであり ;
R7および R8は独立して、 水素、 C^— 6アルキル、 ァラルキル、 またはそれ らが結合している窒素原子と一緒になつて、 酸素、 窒素または硫黄から選択 される 1または 2個のへテロ原子を含有する所望により置換されていてもよ い 5ないし 7員複素環を形成し;
Aは酸素、 S(〇)n (ここに、 nは 0、 1または 2である) であるか、 または Aは NR12 (ここに、 R 12は水素または — 6アルキルである) であるか、 または Aは CR5 = CR6または CR5R6 (ここに、 R5および R6は独立して 水素または — 6アルキルである) であり ;
mは 1ないし 4であり ;
nは 1または 2であって;
Bは一(CR13R14)q— (ここに、 Qは 2、 3または 4であり、 R13および R14は独立して水素または — 6アルキルである) であるか、 または Bは(C R13R14)r-D (ここに、 rは 0、 1または 2であり、 Dは酸素、 硫黄また は CR13 = CR14である) を意味する] で示される化合物またはその塩が記 載されている。
具体例としては、 [7— (2—ジメチルアミノエトキシ) —6—メトキシー 3, 4ージヒドロー 2 H—キノリン一 1一ィル]一 [2 '—メチルー 4 ' - (5 —メチルー 1, 2, 4—ォキサジァゾール— 3—ィル) ビフエ二ルー 4ーィ
- (3—ジメチルァミノプロピル) 一 6—メトキシ— 3,
4—ジヒドロ一 2H—キノリン一 1一ィル]— [2 '—メチル一 4 '— (5— メチルー 1, 2, 4一ォキサジァゾ一ルー 3—ィル) ピフエ二ル— 4—ィル] メタノンなどが記載されている。
3) 特開平 6— 211800には、 バソプレシン拮抗活性あるいはォキシ トシン拮抗活性を有する式
〔式中 R1は、 水素原子、 八ロゲン原子、 水酸基、 低級アルカノィルォキシ基、 置換基として低級アルキル基及び低級アルカノィル基.なる群より選ばれた基 を有することのあるアミノ低級アルコキシ基、 力ルポキシ置換低級アルコキ シ基、 低級アルコキシカルポニル置換低級アルコキシ基又は置換基として低 級アルキル基を有することのあるアミノカルボニル低級アルコキシ基を示す。 R4は水素原子、 基一 NR6R7 (R6及び R7は、 同一又は異なって、 水素原 子、 低級アルキル基、 低級アルケニル基又はフエニル環上に置換基としてハ ロゲン原子を有するベンゾィル基を示す。 ) 、 低級アルケニルォキシ基、 水 酸基置換低級アルキル基、 基一〇一 CO— ANR8R9 (Aは低級アルキレン 基を示す。 R8及び R9は、 同一又は異なって、 水素原子又は低級アルキル基 を示す。 また R8及び R9はこれらが結合する窒素原子と共に窒素原子もしく は酸素原子を介し又は介することなく 5〜 6員環の飽和又は不飽和の複素環 を形成してもよい。該複素環上には、低級アルキル基が置換していてもよい。)、 基一 0— R1Q (R1Gはアミノ酸残基を示す。 ) 、 低級アルコキシカルボニル 置換低級アルキリデン基、 低級アルコキシカルポニル置換低級アルキル基、 カルポキシ置換低級アルキル基、 基— ACONRHR12 (Aは前記に同じ。
R 11及び R 12は、 同一又は異なって、 水素原子、 水酸基を有することのある 低級アルキル基、 ピぺリジン環上にフエニル低級アルキル基を有することの あるピペリジニル基、 力ルバモイル置換低級アルキル基、 ピリジル置換低級 アルキル基、 ピリジル基、 基一 ANR39; 4() (Aは前記に同じ。 R39及び R 4Qは、 同一又は異なって、 水素原子又は水酸基を有することのある低級アル キル基を示す。 また R39及び R4Gは、 これらが結合する窒素原子と共に窒素 原子もしくは酸素原子を介し又は介することなく 5〜 6員環の飽和の複素環 を形成してもよい。該複素環上には、低級アルキル基が置換していてもよい。)、 ピラジン環上に置換基として低級アルキル基を有することのあるピラジニル 置換低級アルキル基、 ピロール環上に置換基として低級アルキル基を有する ことのあるピロリル置換低級アルキル基、 ピ口リジン環上に置換基として低 級アルキル基を有することのあるピロリジニル置換低級アルキル基、 又はフ ェニル環上にハロゲン原子を有することのあるフエ二ル基を示す。 また R 11 及び R 12は、 これらが結合する窒素原子と共に窒素原子もしくは酸素原子を 介し又は介することなく 5〜 7員環の飽和の複素環を形成してもよい。 該複 素環上には、 低級アルキル基、 低級アルコキシカルポニル基、 置換基として 低級アルキル基及び低級アルカノィル基なる群より選ばれた基を有すること のあるアミノ基、 低級アルコキシカルボニル置換低級アルキル基、 フエニル 環上にハ口ゲン原子を有することのあるフエニル基、 シァノ置換低級アルキ ル基、 低級アルケニル基、 ォキシラニル置換低級アルキル基、 力ルバモイル 置換低級アルキル基、 置換基として水酸基及び低級アルキル基を有すること のあるアミノ基なる群より選ばれた基を 1〜 2個有する低級アルキル基又は ピロリジニルカルポニル低級アルキル基が置換していてもよい。 ) 、 基—〇 ACONR23 24 (Aは前記に同じ。 R23及び R24は、 同一又は異なって、 水素原子、 低級アルキル基、低級アルコキシカルボニル置換低級アルキル基、 カルポキシ置換低級アルキル基、 ピペリジン環上に低級アルキル基を有する ことのあるピペリジニル基又は基一 B— NR23AR24A (式中 Bは低級アルキ レン基を示す。 R23A及び R24Aは、 同一又は異なって、 水素原子又は低級ァ ルキル基を示す。 また R23A及び R24Aは、 これらが結合する窒素原子と共に
窒素原子もしくは酸素原子を介し又は介することなく 5〜 6員環の飽和の複 素環を形成してもよい。 ) を示す。 R23及び R24は、 これらが結合する窒素 原子と共に窒素原子もしくは酸素原子を介し又は介することなく 5〜 7員環 の飽和の複素環を形成してもよい。 該複素環上には低級アルキル基が置換し ていてもよい。 ) 、 ピロリジン環上に低級アルコキシ力ルポ二ル基を有する ピロリジニルカルポニル低級アルコキシ基、 低級アルコキシ置換低級アル力 ノィルォキシ基、 基— B〇C〇ANR25R26 (Aは前記に同じ。 Bは低級ァ ルキレン基を示す。 R25及び R26は、 同一又は異なって、 水素原子又は低級 アルキル基を示す。 ) 、 置換基として低級アルキル基を有することのあるァ ミノ置換低級アルキリデン基、 基一〇ANR27R28 (Aは前記に同じ。 R27 及び R28は、 同一又は異なって、 水素原子、 低級アルキル碁、 低級アルケニ ル基、 低級アルキニル基、 低級アルキルスルホニル基、 置換基として低級ァ ルキル基を有することのあるアミノチォカルポニル基、 基
41
R
( R
41は水素原子又はシァノ基を示す。 R
42は低級アルキル基又は置換基と して低級アルキル基を有することのあるアミノ基を示す。 ) 、 力ルバモイル 基、 低級アルコキシカルポニル基、 シクロアルキル基、 フエニル環上に置換 基としてハロゲン原子を有することのあるフエニル低級アルキル基、 シァノ 置換低級アルキル基、 ハロゲン原子置換低級アルキルスルホニル基又は低級 アルキル基を有することのあるアミノ置換低級アルキル基を示す。 R
27及び R
28は、 これらが結合する窒素原子と共に窒素原子もしくは酸素原子を介し 又は介することなく 5〜10員環の単環もしくは二項環の飽和又は不飽和の 複素環を形成してもよい。 該複素環上には、 ォキソ基、 低級アルキル基、 低 級アルコキシカルポニル基、 低級アル力ノィル基又は低級アル力ノィルアミ ノ基が置換していてもよい。 ) 、 シァノ基、 シァノ置換低級アルキル基、 フ
ェニル環上に置換基として低級アルキル基を有することのあるフエニルスル ホニルォキシ基もしくは水酸基を有する低級アルコキシ基、基— ANR
29R
3 0 (Aは前記に同じ。 R
29は水素原子又は低級アルキル基を示す。 ;
3()は低 級アルケニル基、 シクロアルキル基又は低級アルキニル基を示す。 R
29及び R
3Qは、 これらが結合する窒素原子と共に窒素原子もしくは酸素原子を介し 又は介することなく 5〜 6員環の飽和の複素環を形成してもよい。 該複素環 上には、 低級アルキル基、 低級アルカノィル基、 低級アルキル基及び低級ァ ルカノィル基なる群より選ばれた基を有することのあるアミノ基、 低級アル キルスルホニル基、 低級アルコキシ力ルポニル基又は置換基として低級アル キル基を有することのあるアミノカルポニル基が置換していてもよい。 ) 、 フェ二ル環上に置換基として低級アルキル基を有することのあるフエニルス ルホニルォキシ置換低級アルキル基、 フタルイミド置換低級アルキル基、 シ ァノ置換低級アルキリデン基、 ハロゲン原子置換低級アルキル基、 イミダゾ リル置換低級アルキル基、 1, 2, 4一トリァゾリル置換低級アルコキシ基、 1, 2, 3、 4ーテトラゾリル置換低級アルコキシ基、 1, 2, 3, 5—テ トラゾリル置換低級アルコキシ基、 1, 2, 3、 4ーテトラゾリル置換低級 アルキル基、 1, 2, 3, 5—テトラゾリル置換低級アルキル基、 1, 2, 4一トリァゾリル置換低級アルキル基、 カルポキシ置換低級アルコキシ基、 低級アルコキシカルポニル置換低級アルコキシ基、 ピリジルチオ置換低級ァ ルコキシ基、 ピリミジン環上に低級アルキル基を有することのあるピリミジ 二ルチオ置換低級アルコキシ基、 イミダゾリルチオ置換低級アルコキシ基、 ピリジルスルフィニル置換低級アルコキシ基、 ピリジルスルホニル置換低級 アルコキシ基、 ィミダゾリルスルフィニル置換低級アルコキシ基又はィミダ ゾリルスルホニル置換低級アルコキシ基を示す。 R
5は水素原子又は水酸基を 示す。 R
4と R
5とは、一緒になつてォキソ基を形成してもよい。 R
2は水素原 子、 低級アルキル基、 水酸基、 ハロゲン原子又は低級アルコキシ基を示す。 R
3は基
(R13は、 ハロゲン原子、 水酸基、 力ルバモイル基、 低級アルキル基、 ピぺ ラジン環の 4位に低級アルカノィル基を有するピペラジニル低級アルコキシ 基、 イミダゾリル置換低級アルコキシ基、 ピぺリジン環上に低級アルカノィ ルァミノ基を有するピペリジニル低級アルコキシ基、 1, 2, 4—トリァゾ リル置換低級アルコキシ基、 低級アルキル基を有することのあるウレィド置 換低級アルコキシ基又は置換基として低級アルキル基を有することのあるァ ミノ置換低級アルコキシ基を示す。 mは 0又は 1〜3の整数を示す。 フエ二 ル環上に置換基としてハロゲン原子、 低級アルコキシ基、 低級アルキル基及 び二ト口基からなる群より選ばれた基を 1〜 3個有するフエニル低級アル力
(nは 1又は 2を示す) 又は基
を示す。 ベンゾァセピン骨格の 4, 5位の炭素間結合は一重結合又は二重結 合を示すものとする。 ただし R
1が水素原子又はハロゲン原子を示し、 R
4が 水素原子、 基— NR
6R
7 (尺
6及び1
7は、 フエニル環上に置換基としてハロ ゲン原子を有するベンゾィル基以外の前記 R
6及び R
7を示す。 ) 、 基一〇一 CO—ANR
8R
9 (Aは前記に同じ。 R
8及び R
9は、 同一又は異なって、 水 素原子又は低級アルキル基を示す。 ) 、 水酸基置換低級アルキル基、 力ルポ
キシ置換低級アルコキシ基、 低級アルコキシカルポニル置換低級アルコキシ 基又は基一 0— A— NR
27R
28 (Aは前記に同じ。 R
27及び R
28は、 同一又 は異なって、 水素原子又は低級アルキル基を示す。 ) を示し、 R
5が水素原子 又は水酸基を示すか又は R
4と R
5が一緒になつてォキソ基を示し、 更に R
3
を示す場合には、 R
13はカルパモイル基、 ピぺラジン環の 4位に低級アル力 ノィル基を有するピぺラジニル低級アルコキシ基、 ィミダゾリル置換低級ァ ルコキシ基、 ピぺリジン環上に低級アル力ノィルアミノ基を有するピぺリジ ニル低級アルコキシ基、 1, 2, 4_トリァゾリル置換低級アルコキシ基又 は低級アルキル基を有することのあるウレィド置換低級アルコキシ基でなけ. ればならない。 ] で表される化合物またはその塩が記載されている。
具体例としては、 N— [4— [[7— [3— (ジメチルァミノ) プロボキシ]一
2, 3, 4, 5—テトラヒドロー 1H— 1—ベンズァゼピン一 1—ィル] 力 ルポニル]フエニル]一 2—メチルベンズアミドなどが記載されている。
肥満症の予防,治療剤などとして有用であり、 経口吸収性に優れ、 力つ安 全なメラニン凝集ホルモン拮抗剤の開発が切望されている。 発明の開示
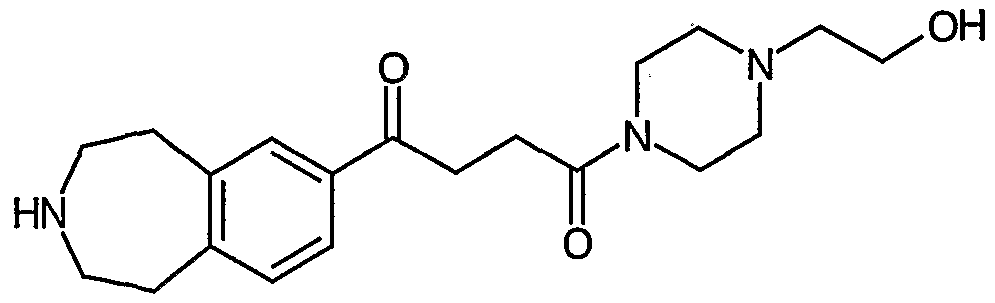
本発明者らは MCH拮抗作用を有する化合物について鋭意検討を行なつた結 果、 式
(式中の記号は前記と同意義を示す)で表される化合物に、 式: R— X— (式 中の記号は前記と同意義を示す)で表される基を導入した誘導体が優れた MCH 拮抗作用を有することを見いだし、 本発明を完成した。
すなわち、 本発明は、
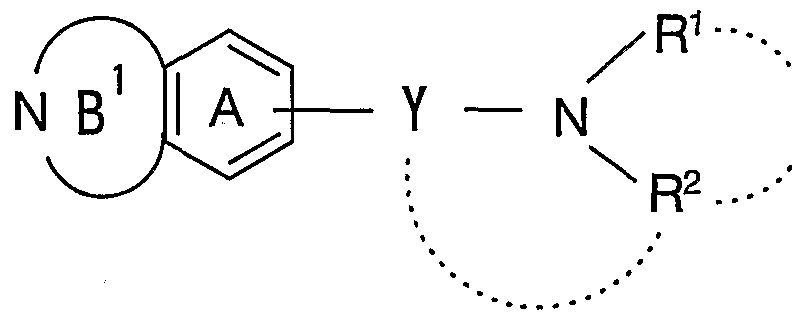
1 ) 式
R— X— ( I )
[式中、 : は水素原子、 ハロゲン原子または置換基を有していてもよい環状 基を;
Xは結合手または主鎖の原子数 1ないし 1 0のスぺ一サ一を;
Yは主鎖の原子数 1ないし 6のスぺーサ一を;
A環はさらに置換基を有していてもよいベンゼン環を;
B環はさらに置換基を有していてもよい 5ないし 9員含窒素非芳香族複素環 を;
R 1および R 2は同一または異なって水素原子、 置換基を有していてもよい炭 化水素基または置換基を有していてもよい複素環基を示すか、 R 1と R 2とは 隣接する窒素原子とともに置換基を有していてもよい含窒素複素環を形成し てもよく、 R 2は隣接する窒素原子および Yとともに置換基を有していてもよ い含窒素複素環を形成していてもよい] で表される化合物またはその塩を含 有してなるメラニン凝集ホルモン拮抗剤;
2 ) Rが置換基を有していてもよい環状基であり、 Xが主鎖の原子数 1ない し 6のスぺ一サ一であり、 R 1および R 2が同一または異なつて水素原子また は置換基を有していてもよい炭化水素基を示すか、 R 1と R 2とが隣接する窒 素原子とともに置換基を有していてもよい含窒素複素環を形成するか、 R '2が 隣接する窒素原子および Yとともに置換基を有していてもよい含窒素複素環 を形成する前記 1 ) 記載の剤;
3 ) メラニン凝集ホルモンに起因する疾患の予防 ·治療剤である前記 1 ) 記 載の剤;
4 ) 肥満症の予防 ·治療剤である前記 1 ) 記載の剤;
5 ) 式
Ar1— X— N B |l J— Y— N ; (に)
" R2 .ノ'
[式中、 Ar 1は置換基を有していてもよい環状基を;
Xは結合手または主鎖の原子数 1ないし 1 0のスぺ一サーを;
Υは主鎖の原子数 1ないし 6のスぺーサ一を;
Α環はさらに置換基を有していてもよいベンゼン環を;
B 1環はさらに置換基を有していてもよい 5ないし 9員含窒素非芳香族複素 環を;
R 1および R 2は同一または異なって水素原子、 置換基を有していてもよい炭 化水素基または置換基を有していてもよい複素環基を示すか、 R 1と R 2とは 隣接する窒素原子とともに置換基を有していてもよい含窒素複素環を形成し てもよく、 R 2は隣接する窒素原子および Yとともに置換基を有していてもよ い含窒素複素環 (ピペリジンを除く) を形成していてもよい。 ただし、 が C Oであるとき、 B 1環がそれぞれさらに置換墓を有していてもよいァゼパン または 4 , 5—ジヒドロアゼピンでないか、 または Ar 1が置換基を有してい てもよぃビフエ二リルでない。 また、 Yは一 CO— (C (R a )H) n a— (R aは 水素原子または置換基を有していていもよい炭化水素基を、 n aは 1ないし 10の整数を示す) でなく、 ァミノ基で置換された 2環性含窒素複素環を有し ない。 ] で表される化合物またはその塩;
6 ) Xが主鎖の原子数 1ないし 1 0のスぺ一サ一であり、 R 1および R 2が同 一または異なって水素原子または置換基を有していてもよい炭化水素基を示 すか、 R 1と R 2とが隣接する窒素原子とともに置換基を有していてもよい含 窒素複素環を形成するか、 R 2が隣接する窒素原子および Yとともに置換基を 有していてもよい含窒素複素環'(ピペリジンを除く) を形成する前記 5 ) 記 載の化合物;
7 ) Ar 1で示される環状基が芳香族基である前記 5 ) 記載の化合物;
8 ) 芳香族基が、 炭素数 6ないし 1 4の単環式または縮合多環式芳香族炭化 水素および 5ないし 10員芳香族複素環から選ばれる 2または 3個で形成され
る芳香環集合体から任意の水素原子 1個を除いた基である前記 7) 記載の化 合物;
9) Xおよび Yで示されるスぺ一サ一が、 一 0—;一 S—;—CO—;一 SO—; -SO 2-; -N 8- (R 8は水素原子、 ハロゲン化されていてもよい Cト6アル キル、ハロゲン化されていてもよい Cエ アルキル一力ルポニル、ハロゲン化 されていてもよい C ^6アルキルスルホニルを示す) ;および置換基を有して いてもよい 2価の Cト6非環式炭化水素基から選ばれる 1ないし 3個からなる 2価基である前記 5) 記載の化合物;
10) Xが COである前記 5) 記載の化合物;
11) Y力置換基を有していてもよい C 2_6アルケニレンである前記 5)記載 の化合物;
である前記 5) 記載の化合物;
13) R 1と R 2とが隣接する窒素原子とともに置換基を有していてもよい含 窒素複素環を形成する前記 5) 記載の化合物;
14) R 1および R 2が (^_6アルキルである前記 5) 記載の化合物;
15) 前記 5) 記載の化合物またはその塩を含有してなる医薬組成物;
16) 前記 5) 記載の化合物のプロドラッグ;
17) 式: Ar1— X— L (lib)
[式中、 Lは脱離基を、 その他の記号は前記 5) 記載と同意義を示す]で表さ れる化合物またはその塩と、 式 .
-ヽ -
[式中の記号は前記 5) 記載と同意義を示す]で表される化合物またはその塩 とを反応させることを特徴とする、 式
[式中の記号は前記と同意義を示す]で表される化合物またはその塩の製造方 法; '
18) 式
R— X— —— N Rb (に,)
[式中、 Rは水素原子、 ハロゲン原子または置換基を有していてもよい環状 基を;
' Xは結合手または主鎖の原子数 1ないし 10のスぺ一サーを;
Y aは主鎖の原子数 1ないし 5のスぺーサーを;
A環はさらに置換基を有していてもよいベンゼン環を;
B環はさらに置換基を有していてもよい 5ないし 9員含窒素非芳香族複素環 を;
• Zは CHまたは Nを;
R bは水素原子または置換基を有していてもよい炭化水素基を示す。 ただし、
Y aはァミノ基で置換された 2環性含窒素複素環を有しない。 ] で表される 化合物またはその塩。
19) Rが水素原子である前記 18) 記載の化合物;
20) 丫&がー((;112 1(:00112;^2— (wlおよび w2は 0ないし 5の整数 を、 かつ wl+w2が 0ないし 5を示す) である前記 18) 記載の化合物;
21) Zが CHである前記 18) 記載の化合物;
H 2 • 2) R bが置換基を有していてもよい C6— 14ァリールである前記 18) 記 載の化合物;
23 式
である前記 18) 記載の化合物;
24) 前記 18) 記載の化合物またはその塩を含有してなる医薬組成物; 25) 前記 18) 記載の化合物のプロドラッグ;
26) 式: R— X— L (Ila)
[式中、 Lは脱離基を、 その他の記号は前記 18) 記載と同意義を示す]で表 される化合物またはその塩と、 式
[式中の記号は前記 18)記載と同意義を示す]で表される化合物またはその 塩とを反応させることを特徴とする、 式
R— X— Z— Rb ( ,)
[式中の記号は前記と同意義を示す]で表される化合物またはその塩の製造方 法;
27 ) 式
0
R1
R— X— N B C-(CH2)w7-C N (I" ")
R2.--
[式中、 Rは水素原子、 ハロゲン原子または置換基を有していてもよい環状 基を;
Xは結合手または主鎖の原子数 1ないし 10のスぺ一サーを;
A環はさらに置換基を有していてもよいベンゼン環を;
B環はさらに置換基を有していてもよい 5ないし 9員含窒素非芳香族複素環 を;
w 7は 0ないし 4の整数を;
R 1および R 2は同一または異なって水素原子、 置換基を有していてもよい炭 化水素基または置換基を有していてもよい複素環基を示すか、 R 1と R2とは 隣接する窒素原子とともに置換基を有していてもよい含窒素複素環を形成し てもよい。 ] で表される化合物またはその塩;
28) 前記 27) 記載の化合物またはその塩を含有してなる医薬組成物;
29) 前記 27 ) 記載の化合物のプロドラッグ; ·
30) 式
R— X— (CH9 V) 2 N -Rc (!' " ")
[式中、 Rは水素原子、 ハロゲン原子または置換基を有していてもよい環状
Xは結合手または主鎖の原子数 1ないし 10のスぺ一サ一を;
A環はさらに置換基を有していてもよいベンゼン環を;
B環はさらに置換基を有していてもよい 5ないし 9員含窒素非芳香族複素環 を;
w 2は 0ないし 5の整数を;
Zは CHまたは Nを;
R cは置換基を有していてもよい炭化水素基を示す。 ]で表される化合物また はその塩;
31) Zが CHである前記 30) 記載の化合物;
32) R cが置換基を有していてもよい C6_14ァリールである前記 30) 記 載の化合物;
33) 前記 30) 記載の化合物またはその塩を含有してなる医薬組成物; 34) 前記 30) 記載の化合物のプロドラッグ;
35) 摂食抑制剤である前記 1) 記載の剤;
36) 前記 1) 記載のメラニン凝集ホルモン拮抗剤と、 糖尿病治療薬、 高血 圧治療薬および動脈硬化症治療薬から選ばれる少なくとも 1種以上とを組み 合わせてなる医薬; '
37) 式'(I) で表される化合物またはその塩の有効量を哺乳動物に投与する ことを特徴とする、 該哺乳動物におけるメラニン凝集ホルモンに起因する疾 患の予防または治療方法;
38) 式
R— X— ( ,,)
[式中、 Rは水素原子、 ハロゲン原子または置換基を有していてもよい環状 基を;
Xは結合手または主鎖の原子数 1ないし 10のスぺーサ一を;
Ybは主鎖の原子数 1ないし 6のスぺ一サ一を;
A環はさらに置換基を有していてもよいベンゼン環を;
B環はさらに置換基を有していてもよい 5ないし 9員含窒素非芳香族複素環 を;
R 1および R 2は同一または異なって水素原子、 置換基を有していてもよい炭 化水素基または置換基を有していてもよい複素環基を示すか、 R 1と R 2とは 隣接する窒素原子とともに置換基を有していてもよい含窒素複素環 (ピペリ ジンを除く) を形成してもよく、 R 2は隣接する窒素原子および Yとともに置 換基を有していてもよい含窒素複素環を形成していてもよい。 ただし、 Yb は— CO—(C(R a)H)n - (R aは水素原子または置換基を有していていも
よい炭化水素基を、 n, aは 1ないし 10の整数を示す) でない。 ] で表される 化合物またはその塩の有効量を哺乳動物に投与することを特徴とする、 該哺 乳動物における肥満症の予防または治療方法;
3 9 ) メラニン凝集ホルモンに起因する疾患の予防 ·治療剤を製造するため の、 式 (I) で表される化合物またはその塩の使用;
4 0 ) 肥満症の予防 ·治療剤を製造するための、 式 (1"') で表される化合物 またはその塩の使用;などに関する。
Rおよび Ar1で示される 「置換基を有していてもよい環状基」 における 「環 状基」 としては、 芳香族基、 非芳香族環状炭化水素基、 非芳香族複素環基な どが挙げられる。
ここで、 「芳香族基」 としては、 例えば、 単環式芳香族基、 縮合芳香族基、 環集合芳香族基などが挙げられる。
該単環式芳香族基としては、 単環式芳香環から任意の 1個の水素原子を除 いてできる I価基が挙げられる。 該 「単環式芳香環」 としては、 例えばベン ゼン環、 5または 6員芳香族複素環が挙げられる。
Γ5または 6員芳香族複素環」 としては、例えば、炭素原子以外に窒素原子、 硫黄原子および酸素原子から選ばれるヘテロ原子 1個以上 (例えば、 1〜3個) を含む 5または 6員芳香族複素環などが挙げられる。 具体的には、 チォフエ ン、 フラン、 ピロール、 イミダゾール、 ピラゾール、 チアゾール、 イソチア ゾ一ル、 ォキサゾール、 イソォキサゾ一ル、 ピリジン、 ピラジン、 ピリミジ ン、ピリダジン、 1 , 2, 4—ォキサジァゾール、 1, 3, 4—ォキサジァゾ一ル、 1 , 2, 4 ーチアジアゾール、 1, 3, 4—チアジアゾール、 フラザンなどが挙げられる。
「単環式芳香族基」 の具体例としては、 フエニル、 2—または 3—チェニル、 2—,3—または 4一ピリジル、 2—または 3—フリル、 2—, 4—または 5—チアゾ リル、 2—, 4一または 5—才キサゾリル、 1一 3—または 4一ピラゾリル、 2—ピ ラジニル、 1一、 4一または 5—ピリミジニル、 1— , 2—または 3—ピロリル、 1 一, 2—または 4一^ Γミダゾリル、 3—または 4一ピリダジニル、 3—イソチアゾ リル、 3—イソォキサゾリル、 1 , 2, 4—ォキサジァゾ一ルー 5—ィル、 1 , 2, 4—
ォキサジァゾ一ル— 3—ィルなどが挙げられる。
「縮合芳香族基」 としては、 縮合多環式 (好ましくは 2ないし 4環式 さら に好ましくは 2または 3環式)芳香環から任意の 1個の水素原子を除いてでき る 1価基を示す。 該 「縮合多環式芳香環」 としては、 縮合多環式芳香族炭化 水素、 縮合多環式芳香族複素環などが挙げられる。
該 「縮合多環式芳香族炭化水素」 としては、 例えば、 炭素数 9ないし 14の 縮合多環式 (2または 3環式)芳香族炭化水素 (例、 ナフ夕レン、 インデン、 フ ルオレン、 アントラセンなど)などが挙げられる。
該 「縮合多環式芳香族複素環」 としては、 例えば、 炭素原子以外に窒素原 子、 硫黄原子および酸素原子から選ばれるヘテロ原子を 1個以上 (例えば、 1
〜4個)を含む 9ないし 14員、 好ましくは 9または 10員の縮合多環式芳香族 複素環などが挙げられる。 「縮合多環式芳香族複素環」 は、 さらに好ましく は 10員縮合多環式芳香族複素環である。
「縮合多環式芳香族複素環」 の具体例としては、 ベンゾフラン、 ベンズィ ' ミダゾール、 ベンズォキサゾール、 ベンゾチアゾ一ル、 ベンズイソチアゾー レ、 ナフト [2, 3— b]チォフェン、 イソキノリン、 キノリン、 インドール、 キ ノキサリン、 フエナントリジン、 フエノチアジン、 フエノキサジン、 フタラ ジン、 ナフチリジン、 キナゾリン、 シンノリン、 カルパゾール、 β一カルボ リン、 ァクリジン、 フエナジン、 フタルイミド、 チォキサンテンなどが挙げ られる。
「縮合芳香族基」の具体例としては、 1一ナフチル; 2—ナフチル; 2— , 3—, 4 ー, 5—または 8—キノリル; 1—, 3—, 4—,5— , 6—, 7—または 8—イソキノリ ル; 1 _,2—,3— , 4— , 5—,6—または 7—インドリル; 1—,2—, 4—または 5 _ イソインドリル; 1—, 5—または 6—フタラジニル; 2— , 3—または 5—キノキ サリニル; 2—, 3—,4— , 5—または 6—ベンゾフラエル; 2—, 4一, 5—または 6 一べンゾチアゾリル; 1— , 2—, 4一, 5—または 6—べンズイミダゾリルなどが 挙げられる。
「環集合芳香族基」は、 2個以上 (好ましくは 2または 3個)の芳香環が単結 合で直結していて、 環を直結している結合の数力環系の数より 1個少ない芳
香環集合体から任意の水素原子 1個を除いた基を意味する。
該芳香環集合体としては、 例えば、 炭素数 6ないし 1 4の単環式または縮 合多環式芳香族炭化水素.(例、 ベンゼン、 ナフタレンなど) および 5ないし 10員 (好ましくは 5または 6員)芳香族複素環から選ばれる 2または 3個 (好ま しくは 2個)で形成される芳香環集合体などが挙げられる。
芳香環集合体の好ましい例としては、 例えばベンゼン、 ナフタレン、 ピリ ジン、 ピリミジン、 チォフェン、 フラン、 チアゾ一ル、 イソチアゾール、 ォ キサゾール、 イソォキサゾール、 1, 2, 4—ォキサジァゾール、 1, 3, 4—ォキサ ジァゾ一ル、 1, 2, 4—チアジアゾ一ル、 1, 3, 4—チアジアゾール、 キノリン、 イソキノリン、 インドール、 ベンゾチォフェン、 ベンズォキサゾール、 ベン ゾチアゾールおよびべンゾフランから選ばれる 2または 3個の芳香環からな る芳香環集合体が挙げられる。
「環集合芳香族基」 の具体例としては、 2— , 3—または 4ーピフエ二リル; 3 ― (1一ナフチル)一 1, 2, 4一ォキサジァゾ一ルー 5—ィル; 3— (2—ナフチル) - 1, 2, 4—ォキサジァゾ一ルー 5—ィル; 3—(2—べンゾフラニル)—1, 2, 4ーォキ サジァゾール—5—ィル; 3—フエ二ルー 1, 2, 4—ォキサジァゾ一ルー 5—ィ リレ; 3—(2—べンズォキサゾリル)— 1, 2, 4—ォキサジァゾ一ルー 5—ィル; 3— (3 _インドリル)一 ί , 2, 4—ォキサジァゾール— 5—ィル; 3—(2—インドリル) —1, 2, 4—ォキサジァゾ一ルー 5—ィル; 4一フエ二ルチアゾール—2—ィル; 4 一(2—べンゾフラエル)チアゾールー 2—ィル; 4—フエニル— 1, 3—ォキサゾ —ルー 5—ィル; 5—フエニル一^ Γソチアゾ一ルー 4—ィル; 5—フエ二ルォキ サゾールー 2—ィル; 4一(2—チェニル)フエニル; 4一(3—チェニル)フエ二 ル; 3— (3—ピリジル)フエニル; 4一(3—ピリジル)フエニル; 6—フエ二ルー 3—ピリジル; 5—フエ二ルー 1, 3, 4—ォキサジァゾ一ル一 2—ィル; 4一 (2—ナ フチル)フエニル; 4一(2—ベンゾフラエル)フエニル; 4, 4 '—テルフエニル; 5—フエ二ルー 2—ピリジル; 2—フエ二ルー 5 —ピリミジニル; 4一(4— ピリジル)フエニル; 2—フエニル一 1 , 3—ォキサゾール—5—ィル; 2 , 4—ジ フエ二ルー 1, 3—ォキサゾ一ルー 5—ィル; 3 —フエ二ルーイソォキサゾール — 5—ィル; 5—フエニル— 2—フリル; 4一(2—フリリレ)フエニルなどが挙げ
られる。
前記した 「芳香族基」 のなかでも、 「炭素数 6ないし 1 4の単環式または 縮合多環式芳香族炭化水素および 5ないし 10員芳香族複素環から選ばれる 2 または 3個で形成される芳香環集合体から任意の水素原子 1個を除いた基 (好ましくは 2—, 3—または 4—ビフエ二リル; 6—フエ二ルー 3—ピリジル、 5 _フエニル一 2—ピリジルなど) j が好ましい。
「非芳香族環状炭化水素基」 としては、 例えば C 3 _ 8シクロアルキル、 C 3 — 8シクロアルケニルなどが挙げられる。
ここで、 C 3— 8シクロアルキルの具体例としては、 シクロプロピル、 シクロ プチル、 シクロペンチル、 シクロへキシル、 シクロへプチル、 シクロォクチ ルなどが挙げられる。
C 3— 8シクロアルケニルの具体例としては、 シクロプロべニル、 シクロブテ ニル、 シクロペンテニル、 シクロへキセニル、 シクロへプテニル、 シクロォ クテニルなどが挙げられる。
前記した 「非芳香族環状炭化水素基」 のなかでも、 c 3 _ 8シクロアルキルが 好ましく、 とりわけシクロへキシルが好ましい。
「非芳香族複素環基」 としては、 例えば、 単環式非芳香族複素環基、 縮合 多環式非芳香族複素環基などが挙げられる。
該 「単環式非芳香族複素環基」 としては、 単環式非芳香族複素環から任意 の 1個の水素原子を除いてできる 1価基が挙げられる。 該 「単環式非芳香族 複素環」 としては、 例えば炭素原子以外に窒素原子、 硫黄原子および酸素原 子から選ばれるヘテロ原子 1個以上 (例えば、 1〜3個)を含む 5ないし 8員の 単環式非芳香族複素環などが挙げられる。 具体的には、 テトラヒドロチオフ ェン、 テトラヒドロフラン、 ピロリジン、 イミダゾリン、 イミダゾリジン、 ピラゾリン、 ビラゾリジン、 テトラヒドロチアゾ一ル、 テトラヒドロイソチ ァゾ一ル、 テトラヒドロォキサゾール、 テトラヒドロイソォキサゾ一ル、 ピ ペリジン、 テトラヒドロピリジン、 ジヒドロピリジン、 ピぺラジン、 モルホ
リン、 チオモルホリン、 テトラヒドロピリミジン、 テトラヒドロピリダジン、 へキサメチレンィミンなどが挙げられる。
「縮合多環式非芳香族複素環基」 としては、 縮合多環式 (好ましくは 2ない し 4環式、さらに好ましくは 2または 3環式)非芳香族複素環から任意の 1個 の水素原子を除いてできる 1価基を示す。 該 「縮合多環式非芳香族複素環」 としては、 例えば、 炭素原子以外に窒素原子、 硫黄原子および酸素原子から 選ばれるヘテロ原子を 1個以上 (例えば、 1〜4個!)を含む 9ないし 14員、好ま しくは 9または 10員の縮合多環式非芳香族複素環などが挙げられる。具体的 には、 ジヒドロべンゾフラン、 ジヒドロべンズイミダゾ一ル、 ジヒドロベン ズォキサゾ一ル、 ジヒドロべンゾチアゾール、 ジヒドロべンズイソチアゾ一 レ、 ジヒドロナフト [2, 3 _b]チォフェン、 テトラヒドロイソキノリン、 テト ラヒドロキノリン、 インドリン、 イソインドリン、 テトラヒドロキノキサリ ン、 テ ラヒドロフエナントリジン、 へキサヒドロフエノチアジン、 へキサ ヒドロフエノキサジン、 テトラヒドロフタラジン、 テトラヒドロナフチリジ ン、 テトラヒドロキナゾリン、 テトラヒドロシンノリン、 テトラヒドロカル バゾール、 テトラヒドロー i3—力ルポリン、 テトラヒドロアクリジン、 テト ラヒドロフエナジン、 テトラヒドロチォキサンテンなどが挙げられる。
前記した 「非芳香族複素環基」 のなかでも、 「5ないし 8員の単環式非芳香 族複素環基 (好ましくはピペリジノ ; ピペラジニル; ピロリジニルなど) 」 が好ましい。
Rおよび Ar1で示される 「置換基を有していてもよい環状基」 における 「環 状基」 は、 好ましくは芳香族基、 さらに好ましくは単環式芳香族基 (好まし くはフエニル、 ピロリルなど) または環集合芳香族基 (好ましくビフエ二リ ルなど) である。
Rおよび Ar1で示される 「置換基を有していてもよい環状基」 における 「置 換基」 としては、 例えばォキソ、 ハロゲン原子 (例、 フッ素、 塩素、 臭素、 ョ ゥ素など)、 Cエ アルキレンジォキシ (例、 メチレンジォキシ、 エチレンジ才 キシなど)、 ニトロ、 シァノ、 ハロゲン化されていてもよい C,_6アルキル、
ヒドロキシー Cト6アルキル、 C 6 1 4ァリ一ルォキシ— C 6アルキル (例、 フ エノキシメチルなど)、 — 6アルキル—C 6 1 4ァリ一ルー C 2 6アルケニル (例、 メチルフエニルェテニルなど)、 ハロゲン化されていてもよい C 3_ 6シクロア ルキル、ハロゲン化されていてもよい C ^ 6アルコキシ、ハロゲン化されてい てもよい C i _ 6アルキルチオ、置換基を有していてもよい C 7 _ 1 9ァラルキル、 ヒドロキシ、 置換基を有していてもよい C 6 1 4ァリ一ルォキシ、 置換基を有 していてもよい C 7 _ 1 9ァラルキルォキシ、 置換基を有していてもよい C 6 ^ 4ァリール一力ルバモイル、 ァミノ、 アミノー C アルキル (例、 アミノメチ ル、 アミノエチル、 ァミノプロピル、 アミノブチルなど)、 モノー Cト6アル キルアミノ( 、 メチルァミノ、 ェチルァミノ、 プロピルァミノ、 イソプロピ ルァミノ、 プチルァミノなど)、 ジー C ^ 6アルキルアミノ(例、 ジメチルアミ ノ、 ジェチルァミノ、 ジプロピルァミノ、 ジブチルァミノ、 ェチルメチルァ ミノなど)、 モノ— C i— 6アルキルアミノー C卜 6アルキル (例、 メチルァミノ メチル、 ェチルアミノメチル、 プロピルアミノメチル、 イソプロピルアミノ ェチル、 ブチルアミノエチルなど)、 ジー Cト6アルキルアミノー C ^ 6アルキ ル (例、 ジメチルアミノメチル、 ジェチルアミノメチル、 ジプロピルアミノメ チル、 ジイソプロピルアミノエチル、 ジブチルアミノエチルなど)、 置換基を 有していてもよい 5ないし 7員飽和環状ァミノ、置換基を有していてもよい 5 ないし 7員非芳香族複素環基、 ァシル、 ァシルァミノ、 ァシルォキシなどが 挙げられる。
Rおよび Ar1で示される 「環状基」 は、 上記置換基を、 環状基の置換可能な 位置に 1ないし 5個、 好ましくは 1ないし 3個有していてもよい。 また、 置 換基数が 2個以上である場合、 各置換基は同一であっても異なっていてもよ レ また、 Rおよび Ar1で示される 「環状基」 が非芳香族環状炭化水素基ある いは非芳香族複素環基である場合、 該 「環状基」 は、 置換基を有していても よい C 6 _ 1 4ァリール、 置換基を有していてもよい 5ないし 10員芳香族複素 環基などを置換基として有していてもよい。
ここで、 「置換基を有していてもよい C 4ァリール」 および 「置換基を 有していてもよい 5ないし 10員芳香族複素環基」 としては、 後述の 「置換基 を有していてもよい 5ないし 7員飽和環状ァミノ」 における 「置換基」 とし て例示するものが挙げられる。 置換基の数は、 例えば 1ないし 3個である。 また、 置換基数が 2個以上である場合、 各置換基は同一であっても異なって いてもよい。
前記 「ハロゲン化されていてもよい Cぃ6アルキル」 としては、 例えば、 1 ないし 5個、 好ましくは 1ないし 3個のハロゲン原子 (例、 フッ素、 塩素、 臭 素、 ヨウ素など)を有していてもよい Cト6アルキル (例、 メチル、 ェチル、 プ 口ピル、 イソプロピル、 ブチル、 イソプチル、 sec—ブチル、 tert—ブチル、 ペンチル、 へキシルなど)が挙げられる。 具体例としては、 メチル、 クロロメ チル、 ジフルォロメチル、 トリクロロメチル、 トリフルォロメチル、 ェチル、 2—ブロモェチル、 2, 2, 2—トリフルォロェチル、 ペン夕フルォロェチル、 プ 口ピル、 3, 3, 3—トリフルォロプロピル、 イソプロピル、 ブチル、 4, 4, 4—ト リフルォロブチル、 イソブチル、 sec—ブチル、 ter t—ブチル、 ペンチル、 ィ ソペンチル、 ネオペンチル、 5, 5, 5—トリフルォロペンチル、へキシル、 6, 6, 6 一トリフルォ口へキシルなどが挙げられる。
前記 「ヒドロキシー _ 6アルキル」 において、 C 6アルキルとしては、 前記「ハロゲン化されていてもよい Cエ アルキル」 における(^ _ 6アルキル が挙げられる。
前記「ハロゲン化されていてもよい C 3— 6シクロアルキル」 としては、例え ば、 1ないし 5個、 好ましくは 1ないし 3個のハロゲン原子 (例、 フッ素、 塩 素、臭素、 ヨウ素など)を有していてもよい C 3 _ 6シクロアルキル (例、 シクロ プロピル、 シクロブチル、 シクロペンチル、 シクロへキシルなど)などが挙げ られる。 .具体例としては、 シクロプロピル、 シクロブチル、 シクロペンチル、 シクロへキシル、 4, 4—ジクロロシクロへキシル、 2, 2, 3, 3—テトラフルォロ シクロべンチル、 4一クロロシクロへキシルなどが挙げられる。
前記「ハロゲン化されていてもよい C ^ 6アルコキシ」 としては、例えば、 1ないし 5個、 好ましくは 1ないし 3個のハロゲン原子 (例、 フッ素、 塩素、
臭素、 ヨウ素など)を有していてもよい C ^ 6アルコキシ (例、 メトキシ、 エト キシ、 プロボキシ、 ブトキシ、 ペンチルォキシなど)などが挙げられる。 具体 例としては、 例えば、 メトキシ、 ジフルォロメトキシ、 トリフルォロメトキ シ、 エトキシ、 2, 2, 2—トリフルォロエトキシ、 プロボキシ、 イソプロボキシ、 ブトキシ、 4, 4, 4一トリフルォロブトキシ、 イソブトキシ、 sec—ブトキシ、 ぺンチルォキシ、 へキシルォキシなどが挙げられる。
前記「ハロゲン化されていてもよい C ェ アルキルチオ」 としては、例えば、
1ないし 5個、 好ましくは 1ないし 3個のハロゲン原子 (例、 フッ素、 塩素、 臭素、 ヨウ素など)を有していてもよい C ^6アルキルチオ (例、メチルチオ、 ェチルチオ、 プロピルチオ、 イソプロピルチオ、 ブチルチオ、 sec—ブチルチ ォ、 ter t—プチルチオなど)などが挙げられる。 具体例としては、 例えばメチ ルチオ、 ジフルォロメチルチオ、 トリフルォロメチルチオ、 ェチルチオ、 プ 口ピルチオ、 イソプロピルチオ、 プチルチオ、 4, 4, 4一トリフルォロブチルチ ォ、 ペンチルチオ、 へキシルチオなどが挙げられる。
前記 「置換基を有していてもよい C 7_ 1 9ァラルキル」 における 「C 7— 1 9ァ ラルキル」 としては、 例えば、 ベンジル、 フエネチル、 ジフエニルメチル、 トリフエニルメチル、 1—ナフチルメチル、 2—ナフチルメチル、 2, 2—ジフエ ニルェチル、 3_フエニルプロピル、 4一フエニルブチル、 5—フエニルペンチ ルなどが挙げられる。 なかでもベンジルなどが好ましい。
前記 「置換基を有していてもよい 7_ 1 9ァラルキル」 における 「置換基」 としては、 例えば、 ハロゲン原子 (例、 フッ素、 塩素、 臭素、 ヨウ素など)、 C ^ 3アルキレンジォキシ (例、 メチレンジォキシ、 エチレンジォキシなど)、 二 トロ、 シァノ、ハロゲン化されていてもよい C 6アルキル、ハロゲン化され ていてもよい C 3— 6シクロアルキル、ハロゲン化されていてもよい C 6アル コキシ、 ハロゲン化されていてもよい Cト6アルキルチオ、 ヒドロキシ、 アミ ノ、 モノー Cト6アルキルアミノ(例、 メチルァミノ、 ェチルァミノ、 プロピ ルァミノ、 イソプロピルァミノ、 プチルァミノなど)、 ジー C アルキルァ ミノ(例、 ジメチルァミノ、 ジェチルァミノ、 ジプロピルアミノ、 ジブチルァ · ミノ、 ェチルメチルァミノなど)、 ァミノ— C 6アルキル (例、 アミノメチル、
アミノエチル、 ァミノプロピル、 アミノブチルなど)、 モノー C 6アルキル アミノー C 6アルキル (例、 メチルアミノメチル、 ェチルアミノメチル、 プ 口ピルアミノメチル、 イソプロピルアミノエチル、 ブチルアミノエチルなど)、 ジ—C ^ 6アルキルアミノー C ^ 6アルキル (例、 ジメチルアミノメチル、 ジェ チルアミノメチル、 ジプロピルアミノメチル、 ジイソプロピルアミノエチル、 ジブチルアミノエチルなど)、 ホルミル、 力ルポキシ、 力ルバモイル、 チ才力 ルバモイル、 ハロゲン化されていてもよい C ^ 6アルキル一力ルポニル、
—6アルコキシ一カルボニル (例、 メトキシカルボニル、エトキシカルポニル、 プロポキシ力ルポニル、 t er t—ブトキシカルポニルなど)、 モノー (^ - 6アル キル—力ルバモイル (例、 メチルカルバモイル、 ェチルカルバモイルなど)、 ジー C 6アルキル—力 jレバモイル (例、 ジメチルカルバモイル、 ジェチルカ ルバモイル、 ェチルメチルカルバモイルなど)、 ハロゲン化されていてもよい
C i _ 6アルキルスルホニル、 ホルミルァミノ、 ハロゲン化されていてもよい C j— 6アルキル—カルボキサミド、 C ^ 6アルコキシ一力ルポキサミド(例、メト キシカルポキサミド、 エトキシカルポキサミド、 プロポキシ力ルポキサミド、 ブトキシカルポキサミドなど)、 C ^ 6アルキルスルホニルァミノ(例、 メチル スルホニルァミノ、 ェチルスルホニルァミノなど)、 C 6アルキル一力ルポ ニルォキシ (例、 ァセトキシ、 プロパノィルォキシなど)、 C _6アルコキシ一 カルポニルォキシ (例、 メトキシカルボニルォキシ、 エトキシカルポ二ルォキ シ、 プ口ポキシカルボ二ルォキシ、 ブトキシカルポニルォキシなど)、 モノ—
C ^ 6アルキル—力ルバモイルォキシ (例、 メチルカルバモイルォキシ、 ェチ ルカルバモイルォキシなど)、 ジ— C J― 6アルキル一力ルバモイルォキシ (例、 ジメチルカルバモイルォキシ、 ジェチルカルバモイルォキシなど)、 ヒドロキ シー アルキル (例、 ヒドロキシェチルなど) など力挙げられる。 置換基 の数は、例えば 1ないし 5個、好ましくは 1ないし 3個である。.置換基数が 2 個以上の場合、 各置換基は同一であっても異なっていてもよい。
ここで、 「ハロゲン化されていてもよい C ^ 6アルキル」 、 「ハロゲン化さ れていてもよい C 3 _ 6シクロアルキル」 、 「ハロゲン化されていてもよい C! —6アルコキシ」 、 「ハロゲン化されていてもよい C i— 6アルキルチオ」 とし
ては、 それぞれ前記 「置換基を有していてもよい環状基」 における 「置換基」 として例示したものが用いられる。
前記「ハロゲン化されていてもよい C ^ 6アルキル—力ルポニル」 としては、 例えば、 1ないし 5個、 好ましくは 1ないし 3個のハロゲン原子 (例、 フッ素、 塩素、臭素、 ヨウ素など)を有していてもよい アルキル-力ルポニル (例、 ァセチル、 プロパノィル、 ブタノィル、 ペンタノィル、 へキサノィルなど)な どが挙げられる。 具体例としては、 例えば、 ァセチル、 モノクロロアセチル、 トリフルォロアセチル、 トリクロロアセチル、 プロパノィル、 ブタノィル、 ペンタノィル、 へキサノィルなどが挙げられる。
前記「ハロゲン化されていてもよい c i— 6アルキルスルホニル」としては、 例えば、 1ないし 5個、 好ましくは 1ないし 3個のハロゲン原子 (例、 フッ素、 塩素、臭素、 ヨウ素など)を有していてもよい アルキルスルホニル (例、 メチルスルホニル、 ェチルスルホニル、 プロピルスルホニル、 イソプロピル スルホニル、 ブチルスルホニル、 sec—ブチルスルホニル、 tert—ブチルスル ホニルなど)などが挙げられる。 具体例としては、例えばメチルスルホニル、 ジフルォロメチルスルホニル、 トリフルォロメチルスルホニル、 ェチルスル ホニル、 プロピルスルホニル、 イソプロピルスルホニル、 ブチルスルホニル、 4, 4, 4—トリフルォロブチルスルホニル、 ペンチルスルホニル、 へキシルスル ホニルなどが挙げられる。
前記「ハロゲン化されていてもよい C ;L_ 6アルキル一力ルポキサミド」 とし ては、 例えば、 1ないし 5個、 好ましくは 1ないし 3個のハロゲン原子 (例、 フッ素、 塩素、 臭素、 ヨウ素など)を有していてもよい C アルキル一カル ポキサミド(例、 ァセトアミド、 プロパンアミド、 ブタンアミドなど)などが 挙げられる。 具体例としては、 例えばァセトアミド、 トリフルォロアセトァ ミド、 プロパンアミド、 ブタンアミドなどが挙げられる。
前記 「置換基を有していてもよい C 6— 1 4ァリ一ルォキシ」 における 「C 6_ 1 4ァリールォキシ」 としては、 例えば、 フエニルォキシ、 1一ナフチルォキシ、 2—ナフチルォキシなどが挙げられる。
前記 「置換基を有していてもよい 9ァラルキルォキシ」 における 「C
7— 1 9ァラルキルォキシ」 としては、 例えば、 ベンジルォキシ、 フエネチルォ キシ、 ジフエニルメチルォキシ、 トリフエニルメチルォキシ、 1一ナフチルメ チルォキシ、 2—ナフチルメチルォキシ、 2, 2—ジフエニルェチルォキシ、 3- フエニルプロピルォキシ、 4一フエニルブチルォキシ、 5—フエ二ルペンチル ォキシなどが挙げられる。
前記 「置換基を有していてもよい c 6—1 4ァリ一ルー力ルバモイル」 におけ る 「c 6 _ 1 4ァリール—力ルバモイル」 としては、 例えば、 フエ二ルカルバモ ィル、 1—ナフチルカルバモイル、 2—ナフチルカルバモイルなどが挙げられ る。
該 「置換基を有していてもよい C 6— 1 4ァリールォキシ」 、 「置換基を有し ていてもよい C 7— 1 9ァラルキルォキシ」 、 「置換基を有していてもよい C 6 _
1 4ァリール一力ルバモイル」 における 「置換基」 としては、 前記 「置換基を 有していてもよい C 7 ^ 9ァラルキル」 における 「置換基」 として例示したも のが用いられる。置換基の数は、例えば 1ないし 5個、好ましくは 1ないし 3 個である。 また、 置換基数が 2個以上の場合、 各置換基は同一であっても異 なっていてもよい。
前記 「置換基を有していてもよい 5ないし 7員飽和環状ァミノ」 における 「5ないし 7員飽和環状ァミノ」 としては、 例えば, モルホリノ、 チオモルホ リノ、 ピぺラジン一 1一ィル、 ピペリジノ、 ピロリジン一1—ィルなどが挙げ られる。 該「5ないし 7員飽和環状ァミノ」 は、 ベンゼン環と縮合していても よい。
該「置換基を有していてもよい 5ないし 7員飽和環状ァミノ」における「置 換基」 としては、 例えば、 ォキソ、 ハロゲン化されていてもよい C i— 6アルキ ル、ハロゲン化されていてもよい C 6アルキル一力ルポニル、ハロゲン化さ れていてもよい C ^ 6アルキルスルホニル、置換基を有していてもよい C 6 _ 1 4ァリール、 置換基を有していてもよい C 7— 1 9ァラルキル、 置換基を有して いてもよい C 6 _ 1 4ァリ一ル—カルボニル、 置換基を有していてもよい 5ない し 10員芳香族複素環基、 ヒドロキシ、 5ないし 8員の単環式非芳香族複素環 基 (例、 ピベリジニル、 ピペラジニル、 ピロリジニルなど) 、 力ルバモイル、
ヒドロキシー C i_6アルキル、 C ^6アルコキシ一力ルポ二ルー C ^6アルキル
(例、 エトキシカルボニルメチルなど) 、 c8_19ァリールアルケニル (例、 スチリル、 3—フエ二ルー 2—プロブー 2—ェニルなど) 、 Cュ_6アルキル一 カルポキサミド (例、 メチルカルボキサミドなど) 、 (N— (^— 6アルキル) _Cト6アルキル一力ルポキサミド (例、 (N—ェチル) メチルカルポキサミ ドなど) 、 ァミノ、 モノ— C ^6アルキルアミノ(例、 メチルァミノ、 ェチル ァミノ、 プロピルアミノ、 イソプロピルァミノ、 プチルァミノなど)、 ジ—C
^6アルキルアミノ(例、 ジメチルァミノ、 ジェチルァミノ、 ジプロピルアミ ノ、 ジブチルァミノ、 ェチルメチルァミノなど)、 5ないし 8員の単環式非芳 香族複素環基一 C i— 6アルキル (例、 ピロリジニルメチルなど) 、 1ないし 3 個の C ^6アルキルで置換されていてもよい C 6— 14ァリール一アミノー C
6アルキル(例、 2, 6-ジメチルフエニルァミノメチルなど) などが挙げられる。 置換基の数は,、 例えば 1ないし 5個、 好ましくは 1ないし 3個である。 また、 置換基数が 2個以上の場合、各置換基は同一であっても異なっていてもよい。 ここで、 「ハロゲン化されていてもよい C ^6アルキル」 、 「置換基を有し ていてもよい c7— 19ァラルキル」 としては、 それぞれ前記 「置換基を有して いてもよい環状基」 における 「置換基」 として例示したものが用いられる。
「ハロゲン化されていてもよい c i_6アルキル一力ルポニル」、 「ハロゲン 化されていてもよい c ^6アルキルスルホ ル」 としては、 前記「置換基を有 していてもよい C 7— 19ァラルキル」 における 「置換基」 として例示したもの が用いられる。
「置換基を有していてもよい C 6— 14ァリール」における「C 6— 14ァリール」 としては、 例えば、 フエニル、 1一ナフチル、 2—ナフチル、 2—インデニル、 2—アンスリルなどが挙げられる。 なかでも、 フエニルなどが好ましい。
該 「置換基を有していてもよい C 6— 14ァリール」 における 「置換基」 とし ては、 前記 「置換基を有していてもよい C 9ァラルキル」 における 「置換 基」 として例示したものが用いられる。 置換基の数は、 例えば 1ないし 5個、 好ましくは 1ないし 3個である。 置換基数が 2個以上の場合、 各置換基は同 一であっても異なっていてもよい。
「置換基を有していてもよい c 6—1 4ァリール一力ルポニル」 における 「c
6— 1 4ァリール一力ルポニル」 としては、 例えば、 ベンゾィル、 1一ナフトイ ル、 2—ナフトイルなどが挙げられる。
該「置換基を有していてもよい C 6 _ 1 4ァリ.一ルー力ルポニル」における「置 換基」 としては、 前記 「置換基を有していてもよい C 7 _ 1 9ァラルキル」 にお ける 「置換基」 として例示したものが用いられる。 置換基の数は、 例えば 1 ないし 5個、 好ましくは 1ないし 3個である。 置換基数が 2個以上の場合、 各置換基は同一であっても異なっていてもよい。
「置換基を有していてもよい 5ないし 10員芳香族複素環基」 における 「5 ないし 10員芳香族複素環基」 としては、 例えば、 炭素原子以外に窒素原子、 硫黄原子および酸素原子から選ばれる 1または 2種、 好ましくは、 1ないし 4 個のへテロ原子を含む 5ないし 10員の (単環式または 1環式)芳香族複素環基 が挙げられる。 具体的には、 例えば、 2—または 3—チェニル; 2—,3—または 4—ピリジル; 2—または 3—フリル; 2—, 4—または 5—チアゾリル; 2—, 4一 または 5—ォキサゾリル; 1一, 3—または 4—ピラゾリル; 2—ピラジニル; 2 一, 4一または 5—ピリミジニル; 1—, 2—または 3—ピロリル; 1 _ , 2—または 4一イミダゾリル; 3—または 4—ピリダジニル; 3—イソチアゾリル; 3—イソ ォキサゾリル; 1, 2, 4—ォキサジァゾ一ルー 5—ィル; ί , 2, 4—ォキサジァゾ一 ルー 3—ィル; 2—, 3—, 4— , 5—または 8—キノリル; 1ー, 3—, 4— , 5—,6—,7 一または 8—イソキノリル; 1一, 2— , 3— , 4— , 5—,6—または 7—インドリ ル; 1—, 2— , 4—または 5—イソインドリル; 1一, 5—まは 6—フタラジェル; 2—, 3—または 5—キノキサリニル; 2—, 3—, 4一, 5—または 6—ベンゾフラ二 ル; 2—, 4— , 5—または 6—べンゾチアゾリル; 1一, 2—, 4— , 5—または 6—べ ンズィミダゾリルなどが挙げられる。
該「置換基を有していてもよい 5ないし 10員芳香族複素環基」における「置 換基」 としては、 例えば、 ハロゲン原子 (例、 フッ素、 塩素、 臭素、 ヨウ素な ど)、 Cト3アルキレンジォキシ(例、 メチレンジォキシ、 エチレンジォキシな ど)、 ニトロ、 シァノ、 ハロゲン化されていてもよい Cエ アルキル、 C 6 _ 1 4 ァリールォキシ一 C ^6アルキル (例、 フエノキシメチルなど)、 _ 6アルキ
ルー C 6— 1 4ァリール一 C 2_6アルケニル (例、メチルフエニルェテニルなど)、 ハロゲン化されていてもよい C 3— 6シクロアルキル、ハロゲン化されていても よい 6アルコキシ、 ハロゲン化されていてもよい C 丄— 6アルキルチオ、 置 換基を有していてもよい C 7 _ 1 9ァラルキル、 ヒドロキシ、 置換基を有してい てもよい C 6_ 1 4ァリールォキシ、置換基を有していてもよい C 7__ 1 9ァラルキ ルォキシ、 ァミノ、 アミノー C ^ 6アルキル (例、 アミノメチル、 アミノエチ ル、 ァミノプロピル、 アミノブチルなど)、 モノ— C ^ 6アルキルアミノ(例、 メチルァミノ、 ェチルァミノ、 プロピルァミノ、 イソプロピルァミノ、 プチ ルァミノなど)、 ジ—C ェ アルキルアミノ(例、 ジメチルァミノ、 ジェチルァ ミノ、 ジプロピルアミノ、 ジブチルァミノ、 ェチルメチルァミノなど)、 モノ
- C 6アルキルアミノー C i— 6アルキル (例、 メチルアミノメチル、 ェチルァ ミノメチル、 プロピルアミノメチル、 イソプロピルアミノエチル、 プチルァ ミノェチルなど)、 ジ— C ^ eアルキルアミノー C ^6アルキル (例、 ジメチル アミノメチル、 ジェチルアミノメチル、 ジプロピルアミノメチル、 ジイソプ 口ピルアミノエチル、 ジブチルアミノエチルなど)、 5ないし 7員飽和環状ァ ミノ、 ァシル、 ァシルァミノ、 ァシルォキシなどが挙げられる。 置換基の数 は、 例えば 1ないし 5個、 好ましくは 1ないし 3個である。 置換基数が 2個 以上の場合、 各置換基は同一であっても異なっていてもよい。
ここで、 「ハロゲン化されていてもよい C i— 6アルキル」 、 「ハロゲン化さ れていてもよい C 3 _ 6シクロアルキル」 、 「ハロゲン化されていてもよい C i
_ 6アルコキシ」 、 「ハロゲン化されていてもよい — 6アルキルチオ」 、 「置 換基を有していてもよい C 7— 1 9ァラルキル」 、 「置換基 ¾有していてもよい C 6 _ 1 4ァリールォキシ」 、 「置換基を有していてもよい C 7— 1 9ァラルキルォ キシ」 としては、 それぞれ前記 「置換基を有していてもよい環状基」 におけ る 「置換基」 として例示したものが用いられる。
「5ないし 7員飽和環状ァミノ」 としては、前記「置換基を有していてもよ い環状基」 における 「置換基」 である 「置換基 有していてもよい 5ないし 7 員飽和環状アミノ」 に関し、 「5ないし 7員飽和環状ァミノ」 として例示した ものが用いられる。
前記 「ァシル」 としては、 例えば、 式: 一 CO— R 3、 —CO— OR 3、 -CO-NR 3R4、 一 CS— NR3R4、 -SO 2-R 3a 、 — SO— R3a、 — P0(— OR 3)— OR 4 また は— P02— R3a 〔式中、 R 3は(i)水素原子、 (ii)置換基を有していてもよい 炭化水素基、 または(iii) 置換基を有していてもよい複素環基; R3aは(i) 置換基を有していてもよい炭化水素基、または(ii) 置換基を有していてもよ い複素環基; R 4は水素原子または C ^6アルキルを示し; R 3と R 4とは隣接 する窒素原子と共に置換基を有していてもよい含窒素複素環を形成していて もよい〕 で表されるァシルなどが挙げられる。
R 3または R 3 aで示される 「置換基を有していてもよい炭化水素基」 におけ る 「炭化水素基」 としては、 例えば、 鎖状または環状炭化水素基 (例、 アルキ ル、 アルケニル、 アルキニル、 シクロアルキル、 ァリール、 ァラルキル、 ァ リールァルケエル、 ジヒドロインデンなど)などが挙げられる。 このうち、 以 下のような炭素数 1ないし 19個の鎖状または環状炭化水素基などが好ましい。 a)C卜6アルキル (例えば、 メチル、 ェチル、 プロピル、 ィゾプロピル、 プチ ル、 イソブチル、 sec—ブチル、 tert—ブチル、 ペンチル、 へキシルなど) ; b) C 2_6アルケニル (例えば、 ビエル、 ァリル、 イソプロべニル、 2—ブテニル など) ;
c) C 2— 6アルキニル (例えば、 ェチェル、 プロパルギル、 2—ブチェルなど) ; d)C 3_6シクロアルキル (例えば、 シクロプロピル、 シクロブチル、 シクロべ ンチル、 シクロへキシルなど)、 該 C 3— 6シクロアルキルは、 1個のベンゼン 環と縮合していてもよい;
e)C 6— 14ァリール (例えば、 フエニル、 1一ナフチル、 2—ナフチル、 2—イン 丁二
ル、 2—アンスリルなど)、 好ましくはフエニル;
0C 7_19ァラルキル (例えば、 ベンジル、 フエネチル、 ジフエニルメチル、 ト リフエニルメチル、 1—ナフチルメチル、 2—ナフチルメチル、 2, 2—ジフエ二 ルェチル、 3—フエニルプロピル、 4一フエニルブチル、 5—フエ二ルペンチル など)、 好ましくはベンジル、 フエネチル、 3—フエニルプロピル;
g) C 8— 1 9ァリールアルケニル (例えば、 スチリル、 3 —フエ二ルー 2—プロ プー 2—ェニルなど) ;
「炭化水素基」 は、 好ましくは C ^6アルキル、 c 6— 1 4ァリ一ル、 c 7 _ 1 9 ァラルキルなどである。
「置換基を有していてもよい炭化水素基」 における 「置換基」 としては、 例えば、 ハロゲン原子 (例、 フッ素、 塩素、 臭素、 ヨウ素など) ;(^ _3アルキ レンジォキシ (例、 メチレンジォキシ、 エチレンジォキシなど) ;ニトロ;シ ァノ;ハロゲン化されていてもよい C ^ 6アルコキシ;ハロゲン化されていて もよい C 6アルキルチオ;ヒドロキシ;ァミノ;モノー C 6アルキルアミ ノ(例、 メチルァミノ、 ェチルァミノ、 プロピルアミノ、 イソプロピルァミノ、 プチルァミノなど) ;ジ— (ヒドロキシで置換されていてもよい(^ _6アルキ ル) ァミノ(例、 ジメチルァミノ、 ジェチルァミノ、 ジプロピルアミノ、 .ジィ ソプロピルァミノ、 ジブチルァミノ、 ェチルメチルァミノ、 ジ (ヒドロキシ ェチル) ァミノなど) ; 1ないし 3個の Cト6アルキルで置換されていてもよ い C 6— 1 4ァリ一ル一ァ ノ (例、 フエニルァミノ、 2, 6-ジメチルフエニルァ ミノなど) ; N— C 6アルキル一 N— (C アルキルで置換されていても よい C 6一 1 4ァリ一ル) ァミノ(例、 N—メチルー N—フエニルァミノ、 N— ェチル—N— (メチルフエニル) ァミノなど);ニトロで置換されていてもよ い 5または 6員の単環式芳香族複素環ァミノ (例、 ニトロピリジルァミノな ど) ;ォキソまたは C ^ 6アルキルで置換されていてもよい 5ないし 8員の単 環式非芳香族複素環基 (例、 テトラヒドロフリル、. ピロリジニル、 ォキソピ 口リ.ジニル、 ピベリジニル、 メチルピベリジニル、 モルホリニル、 メチルピ ペラジニルなど) ;ホルミル;カルポキシ;力ルバモイル;チォカルバモイ ル;ハロゲン化されていてもよい Cト6アルキル一カルボニル; C 6アルコ キシ—カルポニル (例、 メトキシカルポ ル、 エトキシカルポニル、 プロポキ シカルポニル、 ter t—ブトキシカルポニルなど);置換基を有していてもよい 5ないし 10員芳香族複素環基;置換基を有していてもよい C 6— 1 4ァリール— カルポニル;置換基を有していてもよい C 6_ 1 4ァリールォキシ一力ルポ二
ル;置換基を有していてもよい C 7一 1 9ァラルキルォキシ一カルボニル;置換 基を有していてもよい 5ないし 6員複素環カルポニル;モノー Cト6アルキル 一力ルバモイル (例、 メチルカルバモイル、 ェチルカルバモイルなど);ジー C ^ 6アルキル一力ルバモイル (例、 ジメチルカルバモイル、 ジェチルカルパモ ィル、 ェチルメチルカルバモイルなど) ;置換基を有していてもよい C 6 _ 1 4 ァリール—力ルバモイル;置換基を有していてもよい 5ないし 6員複素環力 ルバモイル;ハロゲン化されていてもよい C i一 6アルキルスルホニル;置換基 を有していてもよい C 6_ 1 4ァリールスルホニル;ホルミルアミノ;ハロゲン 化されていてもよい C アルキル一力ルポキサミド; C 6アルコキシ一力 ルポキサミド(例、 メトキシカルポキサミド、 エトキシカルポキサミド、 プロ ポキシ力ルポキサミド、 ブトキシカルポキサミドなど) ; C ^6アルキルスル ホニルァミノ(例、メチルスルホニルァミノ、ェチルスルホニルァミノなど) ;
C 6アルキル—カルボニルォキシ (例、 ァセトキシ、 プロパノィルォキシな ど) ;置換基を有していてもよい C 6_ 1 4ァリール—カルポニルォキシ; c x _ 6 アルコキシ—カルポニルォキシ (例、 メトキシカルポニルォキシ、 エトキシカ ルポニルォキシ、 プロポキシ力ルポニルォキシ、 ブトキシカルポニルォキシ など);モノ— C i _ 6アルキル—力ルバモイルォキシ(例、 メチルカルバモイル 才キシ、 ェチルカルバモイルォキシなど) ;ジー C i _ 6アルキル一力ルバモイ ルォキシ(例、 ジメチルカルバモイルォキシ、 ジェチルカルバモイルォキシな ど) ;置換基を有していてもよい C 6— i 4ァリ一ルー力ルバモイルォキシ;二 コチノィルォキシなどが挙げられる。 置換基の数は、 例えば 1ないし 5個、 好ましくは 1ないし 3個である。 置換基数が 2個以上の場合、 各置換基は同 一であっても異なっていてもよい。 '
ここで、 「ハロゲン化されていてもよい C ^ 6アルコキシ」 、 「ハロゲン化 されていてもよい C アルキルチオ」 、 「置換基を有していてもよい C
4ァリール一力ルバモイル」 としては、 それぞれ前記「置換基を有していても よい環状基」 における'「置換基」 として例示したものが用いられる。
「ハロゲン化されていてもよい C uアルキル一力ルポニル」、 「ハロゲン 化されていてもよい Cい 6アルキルスルホニル」 「ハロゲン化されていても
よい C 6アルキル一力ルポキサミド」 としては、それぞれ前記「置換基を有 していてもよい C 7一 1 9ァラルキル」 における 「置換基」 として例示したもの が用いられる。
前記 「置換基を有していてもよい 5ないし 10員芳香族複素環基」 、 「置換 基を有していてもよい C 6_ 1 4ァリ一ルーカルボニル」 としては、 それぞれ前 記 「置換基を有していてもよい 5ないし 7員飽和環状ァミノ」 における 「置 換基」 として例示したものが用いられる。
「置換基を有していてもよい C 6_ 1 4ァリールォキシ一力ルポニル」 におけ る 「C 6― 1 4ァリールォキシ一力ルポニル」 としては、 例えばフエニルォキシ 力ルポニル、 1一ナフチルォキシカルポニル、 2—ナフチルォキシカルポニル などが挙げられる。
「置換基を有していてもよい C 7 ^ 9ァラルキルォキシ—力ルポニル」 にお ける 「C 7一 1 9ァラルキルォキシ一力ルポニル」 としては、 例えば、 ベンジル ォキシ力ルポニル、 フエネチルォキシ力ルポニル、 ジフエニルメチルォキシ カルボニル、 トリフエニルメチルォキシカルポニル、 ί一ナフチルメチルォキ シカルポニル、 2—ナフチルメチルォキシカルボニル、 2, 2—ジフエ二ルェチ ルォキシカルポニル、 3—フエニルプロピルォキシカルボニル、 4一フエニル プチルォキシカルポニル、 5—フエ二ルペンチルォキシカルポニルなどが挙げ られる。
前記 「置換基を有していてもよい 5ないし 6員複素環力ルポニル」 におけ る 「5ないし 6員複素環力ルポニル」 としては、 例えば、 ニコチノィル、 イソ ニコチノィル、 2—テノィル、 3—テノィル、 2—フロイル、 3—フロイル、 モ ルホリノ力ルポニル、 ピペリジノカルポニル、 ピロリジン一 1ーィルカルポ二 ルなどが挙げられる。
前記 「置換基を有していてもよい 5ないし 6員複素環力ルバモイル」 にお ける 「5ないし 6員複素環力ルバモイル」 としては、例えば、 モルホリノカル バモニル、 ピペリジノカルバモイル、 2—ピリジルカルバモイル、 3—ピリジ ルカルバモイル、 4—ピリジルカルバモイル、 2—チェ二ルカルバモイル、 3- チェ二ルカルバモイルなどが挙げられる。
前記「置換基を有していてもよい c6—14ァリ一ルスルホニル」 における「c
6— j 4ァリ一ルスルホニル J としては、 例えば、 フエニルスルホニル、 1—ナ フチルスルホニル、 2—ナフチルスルホニルなどが挙げられる。
前記 「置換基を有していてもよい C6_147リール一力ルポ ルォキシ」 に おける ΓΟ 6—14ァリ一ルー力ルポニルォキシ」 としては、 例えば、 ベンゾィ ルォキシ、 1一ナフトイルォキシ、 2_ナフトイルォキシなどが挙げられる。 前記 「置換基を有していてもよい C 6_14ァリール一力ルバモイルォキシ」 における 「C 6_14ァリール一力ルバモイルォキシ」 としては、 例えば、 フエ 二ルカルバモイルォキシ、 ナフチルカルバモイルォキシなどが挙げられる。 前記した「置換基を有していてもよい c6_14ァリールォキシ—カルボエル」、
「置換基を有していてもよい C 7— 19ァラルキルォキシ一力ルポニル」 、 「置 換基を有していてもよい 5ないし 6員複素環力ルポニル」 、 「置換基を有し ていてもよい 5ないし 6員複素環力ルバモイル」 、 「置換基を有していても よい C6_14ァリールスルホニル」 、 「置換基を有していてもよい C6_14ァリ —ルーカルボニルォキシ」 、 「置換基を有していてもよい C 6_14ァリ一ルー カルパモイルォキシ」 における 「置換基」 としては、 前記 「置換基を有して いてもよい c7_19ァラルキル」 における 「置換基」 として例示したものが挙 げられる。 置換基の数は、 例えば 1ないし 5'個、 好ましくは 1ないし 3個で ある。 置換基数が 2個以上の場合、 各置換基は同一であっても異なっていて fcよい。
R3または R3aで示される 「置換基を有していてもよい複素環基」 における 「複素環基」 としては、 例えば炭素原子以外に窒素原子、 硫黄原子および酸 素原子から選ばれる 1.または 2種、 1ないし 4個のへテロ原子を含む 5ないし 14員 (単環、 2環または 3環式)複素環、 好ましくは(i) 芳香族複素環、 (ii)5 ないし 10員非芳香族複素環または(iii)7ないし 10員複素架橋環から任意の 1個の水素原子を除いてできる 1価基などが挙げられる。
ここで、 「芳香族複素環」 としては、 例えば、 炭素原子以外に窒素原子、 硫黄原子および酸素原子から選ばれるヘテロ原子 1個以上 (例えば、 1ないし 4個)を含む 5ないし 14員、 好ましくは 5ないし 10員の芳香族複素環などが
挙げられる。 具体的には、 チォフェン、 フラン、 ピロ一ル、 イミダゾール、 ピラゾール、 チアゾ一ル、 イソチアゾ一ル、 ォキサゾ一ル、 イソォキサゾ一 ル、 ピリジン、 ピラジン、 ピリミジン、 ピリダジン、 1, 2, 4—ォキサジァゾ一 ル、 1 , 3, 4—ォキサジァゾール、 1 , 2, 4—チアジアゾ一ル、 1 , 3, 4—チアジアゾ ール、 フラザン、 ベンゾチォフェン、 ベンゾフラン、 ベンズイミダゾ一ル、 ベンズォキサゾール、ベンゾチアゾ一ル、ベンズイソチアゾ一ル、ナフト [2, 3 —b]チォフェン、 フエノキサチイン、 インドール、 イソインドール、 1H—ィ ンダゾール、 プリン、 4H—キノリジン、 イソキノリン、 キノリン、 フタラジ ン、 ナフチリジン、 キノキサリン、 キナゾリン、 シンノリン、 カルパゾール、 )3—力ルポリン、 フエナントリジン、 ァクリジン、 フエナジンフエノチアジ 'ン、フエノキサジン、フタルイミドなどの芳香族複素環、またはこれらの環 (好 ましくは単環)が 1ないし複数個 (好ましくは 1または 2個)の芳香環 (例、 ベ ンゼン環等)と縮合して形成された環などが挙げられる。
「5ないし 10員非芳香族複素環」 としては、 例えば、 2—または 3—ピロリ ン、 ピロリジン、 2—または 3—イミダゾリン、 2—才キサゾリン、 ォキサゾリ ジン、 2—または 3—ピラゾリン、 ピラゾリジン、 2—チアゾリン、 ピぺリジン、 ピぺラジン、 へキサメチレンィミン、 モルホリ,ン、 チオモルホリンなど^^挙 げられる。
「7ないし 10員複素架橋環」 としては、 例えば、 キヌクリジン、 7—ァザビ シクロ [2· 2. 1]ヘプタンなどが挙げられる。
該 「複素環基」 は、 好ましくは、 炭素原子以外に窒素原子、 硫黄原子およ び酸素原子から選ばれる 1または 2種、好ましくは、 1ないし 4個のへテロ原 子を含む 5ないし 10員の(単環式または 2環式)複素環基である。具体的には、 例えば、 2—または 3—チェニル; 2—, 3—または 4一ピリジル; 2—または 3 一フリル; 2— , 4—または 5—チアゾリル'; 2—, 4一または 5—ォキサゾリル; 1— 3—または 4一ピラゾリル; 2—ピラジニル; 2—、 4—または 5 _ピリミジ ニル; 1—, 2—または 3—ピロリル; 1ー, 2—または 4—イミダゾリル; 3—ま たは 4ーピリダジニル; 3—イソチアゾリル; 3—イソォキサゾリル; 1,2,4一 ォキサジァゾール— 5—ィル; 1 , 2, 4—ォキサジァゾ一ルー 3 _ィル; 2—, 3—, 4
一, 5—または 8—キノリル; 1一, 3—, 4一, 5— , 6— , 7—または 8—イソキノリ ル; 1—, 2—, 3—, 4— , 5— , 6—または 7—インドリル; 1一, 2—, 4一または 5— ィソィンドリル; 1— , 5 _ま'は 6—フタラジニル; 2— , 3—または 5—キノキサ リニル; 2—, 3— , 4—, 5—または 6—べンゾフラニル; 2— , 3—, 4— , 5—または 6—べンゾチェニル; 2— , 4—, 5—または 6—べンゾチアゾリル; 1一, 2—, 4一, 5 —または 6—べンズイミダゾリルなどの芳香族複素環基;例えば、 1— , 2—ま たは 3—ピロリジニル; 1一, 2 _ 4—または 5—イミダゾリジニル; 2―ま'たは 4 一イミダゾリニル; 2—,3—または 4ーピラゾリジニル;ピペリジノ ; 2—,3 —または 4ーピペリジル; 1一または 2—ピペラジニル;モルホリノなどの非 芳香族複素環基などが挙げられる。
該 「置換基を有していてもよい複素環基」 における 「置換基」 としては、 前記「置換基を有していてもよい 5ないし 10員芳香族複素環基」における「置 換基」 として例示したものが用いられる。 置換基の数は、 例えば 1ないし 5 個、 好ましくは 1ないし 3個である。 置換基数が 2個以上の場合、 各置換基 は同一であっても異なっていてもよい。
R 4で示される 「(^_6アルキル」 としては、 例えば、 メチル、 ェチル、 プ 口ピル、 イソプロピル、 プチル、 イソブチル、 sec—ブチル、 ter t—ブチル、 ペンチル、 へキシルなどが挙げられる。
R 3と R 4とが隣接する窒素原子と共に形成する 「置換基を有していてもよ い含窒素複素環」 における 「含窒素複素環」 としては、 例えば、 炭素原子以 外に少なくとも 1個の窒素原子を含み、 窒素原子、 硫黄原子および酸素原子 から選ばれる 1ないし 3個のへテロ原子を含んでいてもよい 5ないし 7員含 窒素複素環などが挙げられる。 該 「含窒素複素環」 は、 好ましくは、 ピペリ ジン、 モルホリン、 チオモルホリン、 ピぺラジン、 ピロリジンなどである。 該 「置換基を有していてもよい含窒素複素環」 における 「置換基」 として は、 前記 「置換基を有していてもよい 5ないし 10員芳香族複素環基」 におけ る 「置換基」 として例示したものが用いられる。 置換基の数は、 例えば 1な いし 5個、 好ましくは 1ないし 3個である。 置換基数が 2個以上の場合、 各 置換基は同一であっても異なっていてもよい。
該 「ァシル」.は、 好ましぐは、 ホルミル、 力ルポキシ、 力ルバモイル、 ハ ロゲン化されていてもよい C 6アルキル一力ルポニル(例、 ァセチルなど)、
C アルコキシ一カルボニル (例、 メトキシカルボニル、 エトキシカルボ二 ル、 プロポキシ力ルポニル、 tert—ブトキシカルポニルなど)、 置換基を有し ていてもよい C 6_14ァリ一ルーカルボニル (例、 ベンゾィル、 1_ナフトイ ル、 2—ナフトイルなど) 、 置換基を有していてもよい C 6_14ァリ一ルォキ シ一力ルポニル (例、 フエニルォキシカルポニル、 1一ナフチルォキシカルボ ニル、 2—ナフチルォキシカルポニルなど) 、 置換基を有していてもよい C 7 _i 9ァラルキルォキシ一力ルポニル(例、 ベンジルォキシカルポニル、 フエネ チルォキシカルポニルなど) 、 置換基を有していてもよい 5ないし 6員複素 環カルボニル (例、 ニコチノィルなど) 、 モノー C — 6アルキル一力ルバモイ ル (例、 メチルカルバモイル、 ェチルカルバモイルなど)、 ジ— アルキル 一力ルバモイル (例、 ジメチルカルバモイル、 ジェチルカルバモイル、 ェチル メチルカルバモイルなど)、 置換基を有していてもよい C 6— 14ァリール一力 ルバモイル (例、 フエ二ルカルバモイル、 4ーメトキシフエ二ルカルバモイ ル、 3, 4—ジメトキシフエ二ルカルバモイルなど) 、 置換基を有していても よい芳香族複素環力ルバモイル (例、 2—ピリジニルカルバモイル、 2—キ ノリニルカルバモイルなど)、ハロゲン化されていてもよい C 6アルキルス ルホニル (例、 メチルスルホニルなど) 、 置換基を有していてもよい C6_14 ァリ一ルスルホニル (例、 フエニルスルホニルなど) などである。
ここで、 「ハロゲン化されていてもよい C ^6アルキル一力ルポ二ル」、 「ハ ロゲン化されていてもよい C卜6アルキルスルホニル」としては、それぞれ前 記 「置換基を有していてもよい C 7— 19ァラルキル」 における 「置換基」 とし て例示したものが用いられる。
「置換基を有していてもよい C 6_14ァリ一ルーカルボニル」 としては、 前 記 「置換基を有していてもよい 5ないし 7員飽和環状ァミノ」 における 「置 換基」 として例示したものが用いられる。
「置換基を有していてもよい C 6_14ァリ一ルォキシ一力ルポニル」 、 「置
換基を有していてもよい C 7— 19ァラルキルォキシ一力ルポニル」 、 「置換基 を有していてもよい 5ないし 6員複素環力ルポニル」 、 「置換基を有してい てもよい芳香族複素環力ルバモイル」 、 「置換基を有していてもよい C 6_14 ァリールスルホニル」 としては、 それぞれ前記 「置換基を有していてもよい 炭化水素基」 における 「置換基」 として例示したものが用いられる。
「置換基を有していてもよい C 6_14ァリール一力ルバモイル」 としては、 前記 「置換基を有していてもよい環状基」 における 「置換基」 として例示し たものが用いられる。 前記 「ァシルァミノ」 としては、 例えば、 前記 「ァシル」 で 1ないし 2個 置換されたァミノが挙げられ、好ましくは、式:一NR 5— C0R 6、 -NR 5-C00R 6 a 、 —NR 5—S02R 6 a、 —NR 5— CONR 6 aR 6b、 一 PO (— OR 5)— OR 6 または -P02-R 6 〔式中、 R 5は水素原子または — 6アルキル; R 6は前記 R 3と 同意義; R 6 aは前記 R 3 aと同意義; R 6 bは R 4と同意義を示す〕 で表されるァ シルアミノなど力挙げられる。
R 5で示される 「( 6アルキル」 としては、 前記 R 4で示される 「( ト 6ァ ルキル」 と同様のものが挙げられる。
該 「ァシルァミノ」 は、 好ましくは、 ホルミルァミノ、 ハロゲン化されて いてもよい C i_6アルキル一力ルポキサミド (例、 メチルカルポキサミド、 ト リフルォロメチルカルポキサミドなど) 、 置換基を有していてもよい C 6_14 ァリール一力ルポキサミド (例、 フエ二ルカルポキサミド、 2—メトキシフ ェニルカルポキサミド、 4ーメトキシフエ二ルカルポキサミドなど) 、 N— (置換基を有していてもよい C 6— 14ァリール—力ルポニル) 一 N— C 6ァ ルキルアミノ (例、 N— 4ーメトキシベンゾィルー N—メチルァミノなど) 、 置換基を有していてもよい C 9ァラルキル—カルポキサミド (例、 ベンジ ルカルポキサミドなど) 、 置換基を有していてもよい芳香族複素環一力ルポ キサミド (例、 ベンゾチォフェン一 2—ィルカルポキサミドなど) 、 八ロゲ ン化されていてもよい(:ュ アルコキシ—力ルポキサミド(例、 メトキシカル ポキサミド、 エトキシカルポキサミド、 プロポキシカルポキサミド、 ブトキ
シカルポキサミドなど)、 置換基を有していてもよい C 6 14ァリールァミノ 力ルポニルァミノ (例、 フエニルァミノ力ルポニルァミノなど) 、 ハロゲン 化されていてもよい Cト6アルキルスルホニルァミノ (例、 メチルスルホニル ァミノ、 トリフルォロメチルスルホニルァミノ、 ェチルスルホニルァミノな ど)、 置換基を有していてもよい C 6_14ァリ一ルスルホニルァミノ (例、 4 —メトキシフエニルスルホニルァミノなど) などである。
ここで、 「置換基を有していてもよい c 6_14ァリール一力ルポキサミド」 、
「N— (置換基を有していてもよい C 6 14ァリール—力ルポニル) —N— C ト6アルキルァミノ」 、 「置換基を有していてもよい C 7 19ァラルキル一力 ルポキサミド」 、 「置換基を有していてもよい芳香族複素環—力ルポキサミ ド J、 「置換基を有していてもよいじ6—14ァリールアミノカルポニルァミノ」 および 「置換基を有していてもよい C 6_14ァリールスルホニルァミノ」 にお ける 「置換基」 としては、 前記 「置換基を有していてもよい(;7_19ァラルキ ル」 における 「置換基」 として例示したものが挙げられる。 置換基の数は、 例えば 1ないし 5個、 好ましくは 1ないし 3個である。 置換基数が 2個以上 の場合、 各置換基は同一であっても異なっていてもよい。 前記 「ァシルォキシ」 としては、 例えば、 前記 「ァシル」 1個で置換された ォキシが挙げられ、 好ましくは、 式:— 0— C0R 7、 — 0— C00R 7、 -0-C0NHR 7、 -P0(OH) -0R 7 または— P02— R 7 〔式中、 R 7は前記 R 3と同意義を示 す〕 で表されるァシルォキシなどが挙げられる。
該 「ァシルォキシ」 は、 好ましくは、 ハロゲン化されていてもよい C卜6 アルキル一力ルポニルォキシ (例、 ァセトキシ、 プロパノィルォキシなど)、 , 置換基を有していてもよい C 6_14ァリール—カルボニルォキシ (例、 ベンゾ ィルォキシ、 4 _メトキシベンゾィルォキシなど)、 ハロゲン化されていても よい C ^6アルコキシ一力ルポニルォキシ(例、 メトキシカルポニルォキシ、 トリフルォロメトキシカルポニルォキシ、 エトキシカルポニルォキシ、 プロ ポキシ力ルポニルォキシ、 ブトキシカルポニルォキシなど)、 モノー — 6ァ ルキル一力ルバモイルォキシ (例、 メチルカルバモイルォキシ、 ェチルカルバ
モイルォキシなど)、 ジー Cト6アルキル一力ルバモイルォキシ (例、 ジメチル 力ルバモイルォキシ、 ジェチルカルバモイルォキシなど)、 置換基を有してい てもよい C 6— 1 4ァリール一力ルバモイルォキシ (例、 フエ二ルカルバモイル 才キシ、 ナフチルカルバモイルォキシなど)、 ニコチノィルォキシなどである。 なお、 「置換基を有していてもよい C 6_ 1 4ァリール—力ルポ二ルォキシ」 、 「置換基を有していてもよい c 6_ 1 4ァリ一ルー力ルバモイルォキシ」 におけ る 「置換基」 としては、 前記「置換基を有していてもよい c 7 _ 1 9ァラルキル」 における 「置換基」 として例示したものが挙げられる。 置換基の数は、 例え ば 1ないし 5個、 好ましくは 1ないし 3個である。 置換基数が 2個以上の場 合、 各置換基は同一であっても異なっていてもよい。
Rおよび Ar1で示される 「置換基を有していてもよい環状基」 における 「置 換基」 である 「置換基を有していてもよい 5ないし 7員非芳香族複素環基」 における 「5ないし 7員非芳香族複素環基」 としては、 例えば 4,5—ジヒドロ - 1 , 3-ォキサゾール一 2—ィル、 4, 5—ジヒドロー 1, 3—チアゾ一ル _ 2—ィル、 4, 5—ジヒドロー 1 Η— 2—イミダゾリルなどが挙げられる。該「置換基を有し ていてもよい 5ないし 7員非芳香族複素環基」 における 「置換基」 としては、 前記 ·「置換基を有していてもよい 5ないし 7員飽和環状ァミノ」における「置 換基」 として例示したものが用いられる。 .
Rおよび Ar1で示される 「置換基を有していてもよい環状基」 における 「置 換基」 である 「ァシル」 、 「ァシルォキシ」 、 「ァシルァミノ」 としては、 ぞれぞれ前記「置換基を有していてもよい 5ないし 10員芳香族複素環基」 に おける 「置換基」 として例示したものが用いられる。
Rおよび Ar1で示される 「置換基を有していてもよい環状基」 における 「置 換基」は、好ましくは、ハロゲン原子(好ましくはフッ素、塩素、臭素など) ; ニトロ; Cト3アルキレンジォキシ (好ましくはメチレンジォキシなど) ;ハ ロゲン化されていてもよい C卜 6アルキル (好ましくは、 メチル、 ェチル、 プ 口ピル、 トリフルォロメチル、 tert-ブチルなど) ; ヒドロキシ一 C卜 6アル
キル(好ましくは、 ヒドロキシメチルなど) ;ハロゲン化されていてもよい C
3— 6シクロアルキル(好ましくは、 シクロへキシルなど) ;ハロゲン化されて いてもよい C ^ 6アルコキシ (好ましくは、 メトキシ、 エトキシなど) ;ハロ ゲン化されていてもよい C ^ 6アルキルチオ (好ましくは、メチルチオなど); ヒドロキシ;置換基を有していてもよい C 7 _ 1 9ァラルキルォキシ (好ましく はベンジルォキシ、 4—メトキシベンジルォキシ、 3—メトキシベンジルォ キシ、 4一フルォロベンジルォキシ、 4ーメチルチオべンジルォキシ、 4— ェチルベンジルォキシなど) ;置換基を有していてもよい C 6_ 1 4ァリールォ キシ (好ましくはフエニルォキシなど) ;ァミノ;モノー C ^ 6アルキルアミ ノ (好ましくは、 メチルァミノなど) ;ジー cト6アルキルアミノ (好ましく は、 ジメチルァミノなど) ;置換基を有していてもよく、 ベンゼン環と縮合 していてもよい 5ないし 7員飽和環状アミノ(好ましくは 1 , 3-ジォキソ -1 , 3- ジヒドロ- 2 H-イソインドール- 2-ィルなど) ;置換基を有していてもよい 5 ないし 7員非芳香族複素環基 (好ましくは 4, 5—ジヒドロー 1, 3—ォキサゾー ル—2—ィルなど) ;ホルミル;力ルポキシ;置換基を有していてもよい C 6
- 1 4ァリール一力ルポニル(好ましくはベンゾィルなど) ;置換基を有してい てもよい C 6_ 1 4ァリール—力ルバモイル (好ましくはフエ二ルカルバモイル、
4ーメトキシフエ二ルカルバモイル、 3, 4ージメトキシフエ二ルカルバモ ィルなど) ;置換基を有していてもよい芳香族複素環力ルバモイル (例、 一ピリジニルカルバモイル、 2—キノリニルカルバモイルなど) ; Cト 6アル コキシ一力ルポニル (好ましくは、 メトキシカルポニル、 エトキシカルポニル など) ;ハロゲン化されていてもよい(^ - 6アルキル一力ルポキサミド (好ま しくはメチルカルポキサミド、 トリフルォロメチルカルポキサミドなど) ; 置換基を有していてもよい C 6—1 4ァリール—力ルポキサミド (好ましくはフ ェニルカルポキサミド、 2—メトキシフエ二ルカルポキサミド、 4ーメトキ シフエ二ルカルポキサミドなど) ;置換基を有していてもよい C 7_ 1 9ァラル キル—カルポキサミド (好ましくはべンジルカルポキサミドなど) ;置換基 を有していてもよい芳香族複素環一力ルポキサミド (好ましくはベンゾチォ フェン一 2—ィルカルポキサミドなど) ; N— (置換基を有していてもよい C
6_ 1 4ァリール—力ルポニル) —N— C ^ 6アルキルアミノ (好ましくは N— 4—メトキシベンゾィルー N—メチルァミノなど) ;置換基を有していても よい C 6— 1 4ァリールアミノカルポニルァミノ (好ましくはフエニルァミノ力 ルポニルァミノなど) ;置換基を有していてもよい C 6_ 1 4ァリ一ルスルホニ ルァミノ (好ましくは 4—メトキシフエニルスルホニルァミノなど) ;置換 基を有していてもよい C 6_ 1 4ァリール一力ルポニルォキシ (好ましくは 4 _ メ卜キシベンゾィルォキシなど) ;ォキソなどである。
Rおよび Ar1で示される 「置換基を有していてもよい環状基」 における 「環 状基」 が非芳香族環状炭化水素基または非芳香族複素環基である場合、 置換 基を有していてもよい C 6_ 1 4ァリール (好ましくはフエニル) なども好適な 置換基として用いられる。
Rおよび Ar1で示される 「置換基を有していてもよい環状基」 における 「置 換基」 は、 より好ましくはハロゲン原子 (好ましくは塩素など) 、 (^ _6アル キル (好ましくはメチルなど) 、 C i一 6アルコキシで置換されていてもよい C 7— 1 9ァラルキルォキシ (好ましくはメトキシベンジルォキシなど) などであ る。
Rおよび Ar1は、 好ましくは、 ハロゲン原子 (好ましくはフッ素、 塩素、 臭 素など) ;ニトロ; C _3アルキレンジォキシ (好ましくはメチレンジォキシ など) ;ハロゲン化されていてもよい C ^ 6アルキル(好ましくは、 メチル ェチル、 プロピル、 トリフルォロメチル、 ter t-ブチルなど) ;ヒドロキシー C ^ 6アルキル (好ましくは、 ヒドロキシメチルなど) ;ハロゲン化されてい てもよい C 3— 6シクロアルキル(好ましくは、 シクロへキシルなど) ;ハロゲ ン化されていてもよい Cト6アルコキシ (好ましくは、 メトキシ、エトキシな ど) ;ハロゲン化されていてもよい C ^ 6アルキルチオ (好ましくは、 メチル チォなど) ;ヒドロキシ;置換基を有していてもよい C 7— 1 9ァラルキルォキ シ (好ましくはベンジルォキシ、 4ーメトキシベンジルォキシ、 3—メトキ シベンジルォキシ、 4—フルォロベンジルォキシ、 4—メチルチオべンジル ォキシ、 4—ェチルベンジルォキシなど) ;置換基を有していてもよい C 6—
1 4ァリールォキシ (好ましくはフエニルォキシなど) ;ァミノ;モノー
6アルキルアミノ (好ましくは、 メチルァミノなど) ;ジー (^— 6アルキルァ ミノ (好ましくは、 ジメチルァミノなど) ;置換基を有していてもよく、 ベ ンゼン環と縮合していてもよい 5ないし 7員飽和環状アミノ(好ましくは 1, 3 - ジォキソ -1 , 3 -ジヒドロ- 2 H-イソインドール- 2 -ィルなど) ;置換基を有して いてもよい 5ないし 7員非芳香族複素環基 (好ましくは 4, 5—ジヒドロー 1 , 3 —ォキサゾ一ルー 2—ィルなど) ;ホルミル;カルボキシ;置換基を有してい てもよい C 6 _ 1 4ァリール一力ルポニル (好ま.しくはベンゾィルなど) ;置換 基を有していてもよい C 6— 1 4ァリ一ルー力ルバモイル (好ましくはフエニル カルパモィル、 4—メトキシフエ二ルカルバモイル、 3, 4ージメトキシフ' ェニルカルバモイルなど) ;置換基を有していてもよい芳香族複素環力ルバ モイル (例、 2—ピリジニルカルバモイル、 2—キノリニルカルバモイルな ど) ; C 6アルコキシ一力ルポニル (好ましくは、 メトキシカルポニル、 ェ トキシカルポニルなど) ;ハロゲン化されていてもよい C ^ 6アルキル—カル ポキサミド (好ましくはメチルカルポキサミド、 トリフルォロメチルカルボ キサミドなど) ;置換基を有していてもよい C 6— 1 4ァリール一力ルポキサミ ド (好ましくはフエ二ルカルポキサミド、 2—メトキシフエ二ルカルポキサ ミド、 4ーメトキシフエ二ルカルポキサミドなど) ;置換基を有していても よい C 7— 1 9ァラルキル一力ルポキサミド (好ましくはべンジルカルポキサミ ドなど) ;置換基を有していてもよい芳香族複素環一力ルポキサミド (好ま しくはベンゾチォフェン— 2—ィルカルポキサミドなど) ; N— (置換基を 有していてもよい C 6— 1 4ァリ一ルー力ルポニル) 一 N— C 6アルキルアミ ノ (好ましくは N— 4—メトキシベンゾィルー N—メチルァミノなど) ;置 換基を有していてもよい C 6_ 1 4ァリールアミノカルポニルァミノ (好ましく はフエニルァミノ力ルポニルァミノなど) ;置換基を有していてもよい C 6— 1 4ァリールスルホニルァミノ (好ましくは 4ーメトキシフエニルスルホニル ァミノなど) ;置換基を有していてもよい C 6_ 1 4ァリール—力ルポ二ルォキ シ (好ましくは 4ーメトキシベンゾィルォキシなど) ;ォキソなどから選ば れる置換基をそれぞれ 1または 2個有していてもよいフエニル、 ビフエ二リ
ル(好ましくは 4ービフエ二リル) 、 フエ二ルーピリジル(好ましくは 6—フ ェニル—3—ピリジル、 5—フエ二ルー 2—ピリジル)、フエニル—フリル(好 ましくは 5—フエ二ルー 2—フリル) 、 フエニル—イソォキサゾ一ル (好ま しくは 3—フエ二ルーイソォキサゾールー 5—ィル) 、 ジフエ二ルーォキサ ゾ一ル (好ましくは 2 , 4—ジフエ二ルー 1、 3—才キサゾ一ルー 5—ィル) 、 ピリジル一フエニル (好ましくは 4— ( 4—ピリジル) フエニル) 、 フエ二 ル一ピリミジニル (好ましくは 2—フエ二ルー 5—ピリミジニル) ベンゾ フラニルーフェニル (好ましくは 4— ( 2—べンゾフラエル) フエニル) 、 フリル一フエニル(好ましくは 4一 (2—フリル) フエニル)、 ピロリル(好 ましくは 1—ピロリル) またはナフチルである。
また、 Rおよび Ariの好適な例としては、 ォキソ、 置換基を有していても よい C 6— i 4ァリール (好ましくはフエニル) から選ばれる置換基をそれぞれ 1または 2個有していてもよいピペリジノ、 ピペラジニル、 ピロリジニルな ども挙げられる。
Rで示されるハロゲン原子としては、 例えばフッ素、 塩素、 臭素、 ヨウ素 などが挙げられる。 なかでもフッ素が好ましい。
Xで示される 「主鎖の原子数 1ないし 1 0のスぺ一サ一」 とは、 主鎖の原 子が 1ないし 1 0個連なっている間隔を意味する。 ここで、 「主鎖の原子数」 は、 主鎖の原子が最小となるように数えるものとする。 例えば 1, 2—シク 口ペンチレンの原子数を 2個、 1 , 3—シクロペンチレンの原子数を 3個と して数える。
「主鎖の原子数 1ないし 1 0のスぺーサ一」 としては、 例えばー0—、 — S ―、 — CO—、 — S0_、 — S0 2 _、 -NR 8 - (R 8は水素原子、 ハロゲン化され ていてもよい Cト6アルキリレ、ハロゲン化されていてもよい C アルキル一 力ルポニル、ハロゲン化されて てもよい C ^ 6アルキルスル ニルを示す), 置換基を有していてもよい 2価の C ^ 6非環式炭化水素基、 および 2価の C 5 _ 8単環式非芳香族炭化水素基から選ばれる 1ないし 5個からなる 2価基など
'が挙げられる。
ここで、 「ハロゲン化されていてもよい (^_6アルキル」としては、前記「置 換基を有していてもよい環状基」 における 「置換基」 として例示したものが 用いられる。
「ハロゲン化されていてもよい Cェ アルキル—力ルポ二ル」、 「ハロゲン 化されていてもよい c i_6アルキルスルホニル」 とレては、それぞれ前記「置 換基を有していてもよい C 7_197ラルキル」 における 「置換基」 として例示 したものが用いられる。
「置換基を有していてもよい 2価の 非環式炭化水素基」 における 「2 価の — e非環式炭化水素基」 としては、 例えば
(DCト6アルキレン (例えば、 — CH2—、 一(CH2)2—、 —(CH2)3_、 - (CH 2) 4一、 一(CH 2)5—、 一(CH2)6—、 一 CH(CH 3)—、 一 C(CH 3)2—、 -CH 2-CH(CH 3)—、一(CH(CH3))2—、 - (CH 2) 2 C(CH 3)2—、 - (CH 2) 3 C(CH3)2—など);
(2) C 2_6アルケニレン(例えば、 — CH=CH—、 —CH 2—CH=CH—、 — CH=CH— CH2—、 一 CH=CH - CH 2—CH2—、 — CH 2— CF=CH—、 —C(CH 3) 2— CH=CH—、
— CH 2_CH=CH— CH 2—、 _CH 2 - CH 2— CH=CH -、 —CH=CH - CH=CH -、 一 CH=CH— CH 2— CH 2— CH 2—など) ;
(3) C 2— 6アルキニレン(例えば、 — C≡C一、 — CH 2— C≡C—、 — C≡C— CH2_、 — CH 2— C≡C— CH 2_CH 2—など) などが挙げられる。
「置換基を有していてもよい 2価の C ^6非環式炭化水素基」における「置 換基」 としては、例えば八ロゲン原子 (例、 フッ素、 塩素、臭素、 ヨウ素など)、 水酸基、 ニトロ、 シァノ、 ハロゲン化されていてもよい —6アルコキシ、 ハ ロゲン化されていてもよい C ^6アルキルチオ、 アミソ、 モノー C 6アルキ ルァミノ(例、 メチルァミノ、 ェチルァミノ、 プロピルァミノ、 イソプロピル ァミノ、.プチルァミノなど)、 ジー — 6アルキルアミノ(例、 ジメチルァミノ、 ジェチルァミノ、 ジプロピルアミノ、 ジブチルァミノ、 ェチルメチルァミノ など)、 'ホルミル、 力ルポキシ、 力ルバモイル、 チォカルバモイル、 ハロゲン 化されていてもよい C ^6アルキル—力ルポニル、 C ^6アルコキシ一カルボ ニル (例、 メトキシカルポニル、 エトキシカルポニル、 プロポキシ力ルポニル、
tert—ブトキシカルポニルなど)、 ハロゲン化されていてもよい C 6アルキ ルスルホニルなどが挙げられる。 該 「置換基」 の数は、 例えば 1ないし 5個、 好ましくは 1ないし 3個である。
' ここで、 「ハロゲン化されていてもよい C ^ 6アルコキシ」 、 「ハロゲン化 されていてもよい C i _ 6アルキルチオ」 としては、それぞれ前記「置換基を有 していてもよい環状基」 における 「置換基」 として例示したものが用いられ る。
「ハロゲン化されていてもよい C i— eアルキル—カルボニル」、 「ハロゲン 化されていてもよい Cト6アルキルスルホニル」 としては、それぞれ前記「置 換基を有していてもよい C 7_ 1 9ァラルキル」 における 「置換基」 として例示 したものが用いられる。
「置換基を有していてもよい 2価の C ^ 6非環式炭化水素基」における「置 換基」 は、 好ましくはハロゲン原子 (例、 フッ素、 塩素、 臭素、 ヨウ素など)、 水酸基などである。
該 「2価の C 5_8単環式非芳香族炭化水素基」 としては、 例えば C 5— 8シク 口アル力ン、 C 5_ 8シクロアルケンから任意の 2個の水素原子を除いてできる 2価基が挙げられる。 具体例としては、 例えば 1, 2—シクロペンチレン; 1, 3 —シクロペンチレン; 1 , 2—シクロへキシレン; 1, 3—シクロへ キシレン; 1, 4—シクロへキシレン; 1 , 2—シクロへプチレン; 1, 3 ーシクロへプチレン; 1, 4—シクロへプチレン; 3—シクロへキセン一 1, —4ーィレン; 3—シクロへキセン— 1, 2—ィレン; 2 , 5—シクロへキサ ジェン一 1, 4—ィレンなどが挙げられる。なかでも C 5— 8シクロアルキレン が好ましい。 ' Yで示される 「主鎖の原子数 1ないし 6のスぺ一サー」 としては、 例えば 記 Xで示される 「主鎖の原子数 1ないし 1 0のスぺーサ一」 のうち、 主鎖 の原子数が 1ないし 6のものが挙げられる。
Xおよび Yで示される 「スぺ一ザ一」 は、 好ましくは 「主鎖の原子数 1な いし 6のスぺーサ一」 であり、 さらに好ましくは一 0—;—S—;—CO—;一
SO-.; -SO 2-; -NR8- (R8は前記と同意義) ;および置換基を有してい てもよい 2価の C 一 6非環式'炭化水素基から選ばれる 1ないし 3個からなる 2 価基である。
該 「主鎖の原子数 1ないし 6のスぺーサ一」 の好適な例としては、
(1) 置換基(好ましくは、 ハロゲン原子、 水酸基など) を有していてもよい C ュ_6アルキレン(例えば、 —CH2—、 一(CH2)2—、 —(CH2)3—、 -CH(OH)- (CH2 —、 _(CH2)4—、 —(CH2)5—、 —(CH2)6—、 一 CHCH3—、 一 C(CH3) 2—、 — CH 2— CH(CH 3)—、 一 CH(CF3)—、 一(CH(CH 3)) 2—、 _(CF 2)2—、 一(CH2)2 C(CH3)2、 - (CH 2) 3 C(CH3)2—など) ;
(2) 置換基(好ましくは、 ハロゲン原子、 水酸基など) を有していてもよい C 2_6アルケニレン(例えば、 — CH=CH—、 — CH2—CH=CH—、 -CH=CH-CH 2 一、 — CH-CH— CH 2—CH 2—、 — CH2—CF=CH_、 — C(CH 3) 2— CH=CH―、 ― CH2— CH=CH— CH2—、 — CH 2— CH 2— CH=CH—、 一 CH=CH— CH=CH -、 一 CH =CH— CH 2_CH 2—CH 2_など) ;
(3) 置換基(好ましくは、 ハロゲン原子、 水酸基など) を有していてもよい C 2_6アルキニレン(例えば、 一 C≡C―、 —CH2— C≡C―、 一 C≡C— CH2—、 一 (12—(;≡(ー012—(112—など) ;
(4) —(CH2)wl0(CH2)w2—、 一(CH2)wlS(CH2)w2—、
- (CH 2)wl C0(CH 2)w2—、 - (CH 2)wl S0(CH 2)w2 -、
— (CH2)wlS02(CH2)w2—、 -(CH2)wl R8(CH2)w2-;
(5) 一(CH2)w3C0—、 —(CH2)w3C0NR8(CH2)w4—、
― (CH 2)w3 NR 8 C0(CH 2)w4―、 —(CH 2)w3 SO 2NR 8 (CH 2)w4—、
- (CH 2) w3 NR 8 SO 2 (CH 2) w4 -、 一 (CH 2)w3 COO (CH2)w4-;
(6) — (CH2)w5NR8C0—、 —(CH2)w5NR8CONR8b(CH2)w6—、
—(CH2)w5CH=CH(CH2)w6CO〜;
(7) —0(CH2)w7C0—、 —C0(CH2)w7C0—、 一 S(CH 2)w7 CO—、
— S0(CH 2)w7C0—、 —SO 2(CH 2)w7C0—、 _NR 8 (CH 2) w7 CO—、 一 C0CH=CHC0 -; '
(8) —NR 8C0(CH 2)w8C0—、 -CONR 8(CH2)w8C0-;
(R8は前記と同意義を; R8bは R8と同意義を; wlおよび w2は 0ないし 5の 整数を、 かつ wl+w2が 0ないし 5を; および w4は 0ないし 4の整数を、 かつ w3+w4が 0ないし 4を; w5および w6は 0ないし 3の整数を、 かつ w5+' 6が 0ないし 3を; w7は 0ないし 4の整数を; w8ほ 0ないし 3の整数を示す) などが挙げられる。
Xで示される 「主鎖の原子数 1ないし 10のスぺーサ一」 は、 さらに好ま しくは一(CH2)wl0(CH2)w2—、 — C0NR8—、 — NRsC0—、 一(CH2)w3C0—、 — (CH2)w5NR8C0—、 —CO—、 -(CH2)wlC0(CH2)w2- (記号は前記と同意 義を示す) 、 置換基 (好ましくは、 ハロゲン原子、 水酸基など) を有してい てもよい Cエ アルキレン(例えば、 — CH2_、 — (CH2)2—、 — (CH2)3—、 — CH2— CH(CH3)—など)、 置換基(好ましくは、 ハロゲン原子、 水酸基など) を有していてもよい C 2— 6アルケニレン(好ましくは、一 CH=CH—CH2_など)、 置換基 (好ましくは、 ハロゲン原子、 水酸基など) を有していてもよい C2_ 6アルキニレン (好ましくは、 — C≡C_CH2—など)、 -(CH2)wlS02(CH2)w2 一 (記号は前記と同意義を示す) などである。 とりわけ、 一 CO—などが好ま しい。
Yで示される 「主鎖の原子数 1ないし 6のスぺ一サー」 は、 さらに好まし くは—(CH 2)wl0(CH 2)w2 - (記号は前記と同意義を示す)(好ましくは— 0(CH 2)w2-) (例えば、 — 0(CH2)3—など) 、 置換基 (好ましくは、 ハロゲン原 子、 水酸基など) を有していてもよい C i_3アルキレン(例えば、 —CH2—、 — (CH2)2—、 —(CH2)3—、 — CH(OH)—(CH2)2—など)、 置換基(好ましくは、 ハロゲン原子、水酸基など)を有していてもよい C 2ー6アルケニレン(例えば、 — CH-CH -、 — CH2 - CH=CH―、 一 CH=CH— CH 2—、 -CH=CH-CH 2 -CH 2 - など)、 一(CH2)w3C0NH(CH2)w4 -、 —(CH 2) w3 C00(CH 2) w4 - (記号は前記 と同意義を示す) 、 一(CH2)wlC0(CH2)w2— (記号は前記と同意義を示す) (例えば、 一 C0(CH2)2—、 一 C0(CH2)3_、 一(CH2)2C0—、 一(CH2)3C0— など) 、 -C0(CH2)w7C0- (記号は前記と同意義を示す) (例えば—C0(CH2) 2 C0-, — C0(CH 2)3C0—など) 、 —C0CH=CHC0—、 —0(CH2)w7C0— (記号
は前記と同意義を示す) (例えば— 0(CH 2)2C0—など) 、 -C0NR 8(CH 2)w8 CO- (記号は前記と同意義を示す) (例えば _C0NHCH2C0—など) などで ある。
式 (1") 中、 Y aで示される 「主鎖の原子数 1ないし 5のスぺ一サー」 と しては、 例えば前記 Xで示される 「主鎖の原子数 1ないし 1 0のスぺーサ一」 のうち、 主鎖の原子数が 1ないし 5のものが挙げられる。 Yaは好ましくは -(CH 2)wlC0(CH 2)w2- (記号は前記と同意義を示す) (好ましくは一 C0(CH 2)2—など) などである。
式 (Γ") 中、 Ybで示される 「主鎖の原子数 1ないし 6のスぺーサ一」 は、 前記 Yと同意義を示す。 '
Xは、 特に好ましくは、 結合手、 —(CH 2)wlC0(CH 2)w2— (記号は前記と 阇意義を示す) 、 C丄 アルキレン (好ましくは、 一 CH 2—、 _(CH2)2—、 一 (CH 2)3—、 一CH 2— CH(CH 3)—など)、 C 2_6アルケニレン(好ましくは、 — CH = CH— CH 2—など)、 C 2— 6アルキニレン (好ましくは、 一 C≡C一 CH 2—など) などである。
Yは、 特に好ましくは、 -(CH
2)
wl0(CH
2)
w2- (記号は前記と同意義を示 す) (好ましくは一 0(CH
2)
W2—、 さらに好ましくは一 0(CH
2)
3—など) 、 水 酸基で置換されていてもよい C丄 アルキレン (好ましくは、 一(CH
2)
3—、 一 CH(0H)_(CH
2)
2—など)、 C
2_
6アルケニレン (好ましくは、 -CH=CH-CH
2 一、 — CH=CH— CH
2_CH
2—など)、 -(CH
2)
wlC0(CH
2)
w2- (記号は前記と 同意義を示す) (好ましくは、 —C0(CH
2)
3—など) 、 — C0(CH
2)
W7C0— (記 号は前記と同意義を示す) (好ましくは一 C0(CH
?.)
2C0—など) などである。 式
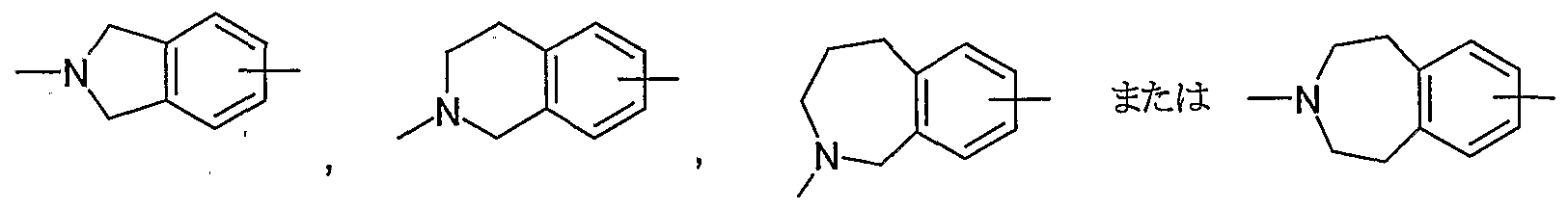
[式中の記号は、 前記と同意義を示す] で表される基、 および式
[式中の記号は、 前記と同意義を示す] で表される基は、 好ましくは、
などである。 なかでも、
なども好ましい。 A環で示される 「ベンゼン環」 、 および B環で示される 「5ないし 9員含 窒素非芳香族複素環」 が有していてもよい 「置換基」 としては、 前記 Rおよ び Ar1で示される 「置換基を有していてもよい環状基」 において例示した「置 換基」 が用いられる。
置換基の数は、 例えば 1ないし 5個、 好ましくは 1ないし 3個である。 置 換基数が 2個以上の場合、 各置換基は同一であっても異なっていてもよい。
A環および B環における置換基は、 好ましくはォキソ、 置換基 (好ましく は C アルコキシ) を有していてもよい C 6— 1 4ァリールなどである。
R 1および R 2で示される 「置換基を有していてもよい炭化水素基」 として は、 前記 R 3として例示したものが用いられる。
,該 「置換基を有していてもよい炭化水素基」 は、 好ましくは 「置換基を有 していてもよい C 6アルキル」 、 C 2— 6アルキニル (例、 ェチニルなど) 、 C
3 _6シクロアルキル (例、 シクロプロピル、 シクロへキシルなど) 、 C 6— 1 4 ァリール (例、 フエニル、 ナフチルなど) 、 ジヒドロインデンなどである。 なかでも、 「置換基を有していてもよい(^— 6アルキル」が好ましく、 さらに 「C 6アルキル」 が好ましい。
ここで、 「置換基を有していてもよい C i— eアルキル」 における 「(^ - 6ァ ルキル」 としては、 例えば、 メチル、 ェチル、 プロピル、 イソプロピル、 ブ チル、 イソブチル、. sec—ブチル、 ter t—ブチル、 ペンチル、 へキシルなどが 挙げられる。 なかでもメチル、 ェチル、 プロピルなどが好ましい。
また、 「置換基を有していてもよい Cト6アルキル」 における 「置換基」 と しては、 例えば、 ハロゲン原子 (例、 フッ素、 塩素、 臭素、 ヨウ素など) ;
_3アルキレンジォキシ (例、 メチレンジォキシ、 エチレンジォキシなど) ;二 トロ;シァノ;ハロゲン化されていてもよい C 3— 6シクロアルキル(例、 シク 口へキシルなど) ;.ハロゲン化されていてもよい C ェ アルコキシ (例、 メト キシ、 イソプロポキシなど) ;ハロゲン化されていてもよい C アルキルチ ォ (例、 メチルチオなど) ;ヒドロキシ;ァミノ;モノ— アルキルアミ ノ(例、 メチルァミノ、 ェチルァミノ、 プロピルァミノ、 イソプロピルァミノ、 プチルァミノなど) ;ジ— (ヒドロキシで置換されていてもよい C i _ 6アルキ ル) ァミノ(例、 ジメチルァミノ、 ジェチルァミノ、 ジプロピルアミノ、 ジィ ソプロピルァミノ、 ジブチルァミノ、 ェチルメチルァミノ、 ジ (ヒドロキシ ェチル) ァミノなど); 1 .ないし 3個の C i— 6アルキルで置換されていてもよ い C 6— 1 4ァリール一ァミノ (例、 フエニルァミノ、 2, 6-ジメチルフエニルァ ミノなど) ; N— C ^ 6アルキル一 N— .(C ^ 6アルキルで置換されていても
よい C 6 _ 1 4ァリール) ァミノ(例、 N—メチルー N—フエ二ルァ'ミノ、 N— ェチルー N— (メチルフエニル) ァミノなど);ニトロで置換されていてもよ い 5または 6員の単環式芳香族複素環ァミノ (例、 ニトロピリジルァミノな ど) ;ォキソまたは C 6アルキルで置換されていてもよい 5ないし 8員の単 環式非芳香族複素環基 (例、 テトラヒドロフリル、 ピロリジニル、 ォキソピ ロリジニル、 ピベリジエル、 メチルピペリジニル、 モルホリニル、 メチルピ ペラジニルなど) ;ホルミル;カルポキシ;力ルバモイル;チォカルパモイ ル;ハロゲン化されていてもよい Cェ- 6アルキル一力ルポニル; C i— 6アルコ キシ一力ルポニル (例、 メトキシカルポニル、 エトキシカルポニル、 プロポキ シカルポニル、 tert—ブトキシカルポニルなど) ;'モノー C ^ 6アルキル—力 ルバモイル (例、 メチルカルバモイル、 ェチルカルバモイルなど);ジー C i _ 6 アルキル一力ルバモイル (例、 ジメチルカルバモイル、 ジェチルカルバモイル、 ェチルメチルカルパモイルなど) ;ハロゲン化されていてもよい Cト6アルキ ルスルホニル;ホルミルァミノ;ハロゲン化されていてもよい C i _ 6アルキル —カルボキサミド; C ^ 6アルコキシ—力ルポキサミド(例、 メトキシカルポ キサミド、 エトキシカルポキサミド、 プロポキシカルポキサミド、 ブトキシ 力ルポキサミドなど); Cト6アルキルスルホニルァミノ(例、 メチルスルホニ ルァミノ、 ェチルスルホニルァミノなど); C i _ 6アルキル一力ルポ二ルォキ シ (例、 ァセトキシ、 プロパノィルォキシなど); Cト6アルコキシ一力ルポ二 ルォキシ (例、 メトキシカルポニルォキシ、 エトキシカルポニルォキシ、 プロ ポキシカルボニルォキシ、 ブトキシカルボニルォキシなど) ;モノ— (^ _ 6ァ ルキル一力ルバモイルすキシ(例、 メチルカルパモイルォキシ、 ェチルカルバ モイルォキシなど);ジー C i _ 6アルキル一力ルバモイルォキシ (例、 ジメチル 力ルバモイルォキシ、 ジェチルカルバモイルォキシなど);置換基を有してい てもよい芳香族基;ハロゲン化されていてもよい C s _ 1 9ァリールォキシ (例、 フエノキシ、 クロロフエノキシなど) などが挙げられる。 置換基の数は、 例 えば 1ないし 5個、 好ましくは 1ないし 3個である。 置換基数が 2個以上の 場合、 各置換基は同一であっても異なっていてもよい。
ここで、 「ハロゲン化されていてもよい C 3_ 6シクロアルキル」 、 「ハロゲ
ン化されていてもよい Cエ アルコキシ j 、 「ハロゲン化されていてもよい C 卜 6アルキルチオ」 としては、 前記「置換基を有していてもよい環状基」 にお ける 「置換基」 として例示したものが用いられる。
「ハロゲン化されていてもよい C ^ 6アルキル一力ルポニル」、 「ハロゲン
5 化されていてもよい C 6アルキルスルホニル」、 「ハロゲン化されていても , ' よい C アルキル一力ルポキサミド」 としては、 前記「置換基 有していて もよい C 7一 1 9ァラルキル」 における 「置換基」 として例示したものが用いら れる。
「置換基を有していてもよい芳香族基」 における 「置換基」 および 「芳香 10 族基」 としては、 前記 Rで示される 「置換基を有していてもよい環状基」 に おいて例示した 「置換基」 および「芳香族基」 が用いられる。 置換基の数は、 例えば 1ないし 5個、 好ましくは 1ないし 3個である。 置換基数が 2個以上 の場合、 各置換基は同一であっても異なっていてもよい。
該 「芳香族基」 は、 好ましくはフエニル、 ナフチル、 フリル、 ピリジル、 15 イミダゾリル、 インドリルなどである。 また、 「置換基」 は、 好ましくは _ 3アルキレンジォキシ (例、 メチレンジォキシなど)、 ハロゲン化されていて もよい C アルキル (例、 トリフルォロメチルなど) 、 ハロゲン化されてい てもよい (^ _ 6アルコキシ (例、 メトキシなど) 、 ハロゲン原子 (例、 塩素な ど) などである。
20
R 1および R 2で示される 「置換基を有していてもよい複素環基」 としては、 前記 R 3として例示したものが用いられる。
該 「置換基を有していてもよい複素環基」 における 「複素環基」 は、 好ま しくは 5ないし 10員非芳香族複素環基であり、さらに好ましくはピロリジニ
25 ル、 ピペリジニルなどである。 また、. 「置換基を有していてもよい複素環基」 における 「置換基」 は、好ましくはハロゲン化されていてもよい C ェ アルキ ル (例、 メチルなど) 、 C 7_ 1 97ラルキル (例、 ベンジルなど) などである。 置換基の数は、 例えば 1ないし 5個である。
R 1と R 2とが隣接する窒素原子とともに形成する 「置換基を有していても よい含 a素複素環」 における 「含窒素複素環」 としては、 例えば、 炭素原子 以外に少なくとも 1個の窒素原子を含み、 窒素原子、 硫黄原子および酸素原 子から選ばれる 1ないし 3個のへテロ原子をさらに含んでいてもよい 3ない し 10員 (好ましくは 3ないし 8員) 含窒素複素環が挙げられる。 具体例とし ては、 例えば、 アジリジン、 ァゼチジン、 モルホリン、 チオモルホリン、 ピ ペリジン、 ピぺラジン、 ピロリジン、 へキサメチレンィミン、 ヘプタメチレ ンィミン、 へキサヒドロピリミジン、 1 , 4—ジァゼパン、 ジヒドロイソキノリ ン、 およびこれらの不飽和環状アミン(例、 1, 2, 5, 6—テトラヒドロピリジン、 1 , 4—ジァゼピン、 ォクタヒドロイソキノリンなど)などが挙げられる。 なか でもモルホリン、 ピぺリジン、 ピぺラジン、 ピロリジンなどが好ましい。 該 「置換基を有していてもよい含窒素複素環」 における 「置換基」 として は、 例えば、 前記 「置換基を有していてもよい 5ないし 7員飽和環状ァミノ」 における 「置換基」 として例示したものが用いられる。 置換基の数は、 例え ば 1ないし 5個、 好ましくは 1ないし 3個である。 置換基数が 2個以上の場 合、 各置換基は同一であっても異なっていてもよい。
該「置換基」 は、 好ましくは、 ヒドロキシ;ハロゲン化されていてもよい C ト 6アルキル (例、 メチル、 ェチルなど) ;ハロゲン原子、 ハロゲン化されて いてもよい C 6アルキルおよびハロゲン化されていてもよい —6アルコキ シから選ばれる 1ないし 3個の置換基を有していてもよい C 6_ 1 4ァリール
(例、 フエニル、 ナフチルなど) ;力ルバモイル;ヒドロキシー Cい 6アルキ ル; Cト 6アルコキシ一カルボニル— C 6アルキル (例、 エトキシカルポ二 ルメチルなど) ; C ^ 3アルキレンジォキシ (例、 メチレンジォキシなど) で 置換されていてもよい C 7 ^ 9ァラルキル (例、 ベンジル、 ジフエ二ルメチル など) ;5ないし 10員芳香族複素環基(例、 ピリジル、 ピリミジニルなど) ; 5ないし 8員の単環式非芳香族複素環基(例、 ピロリジニル、 ピベリジエルな ど) ; C 8— 1 9ァリールアルケニル (例、 3 —フエ二ルー 2—プロブー 2—ェ ニルなど) ; C アルキル一力ルポキサミド (例、 メチルカルポキサミドな ど) ; (N— C i— 6アルキル) 一 C 6アルキル一力ルポキサミド (例、 (N
ーェチル) メチルカルボキサミドなど) ;ジ— — 6アルキルアミノ(例、 ジ メチルァミノなど); 5ないし 8員の単環式非芳香族複素環基一 C i _ 6アルキル (例、 ピロリジニルメチルなど) ; 1ないし 3個の Cェ アルキルで置換され
N
ていてもよ ,んい C6_14ァリール一アミノー C 6アルキル (例、 2, 6-ジメチル フエニルァミノメチルなど) などである。
1^ぉょび112は、 Z隣接する窒素原子とともに置換基を有していてもよい含 窒素複素環を形成することが好ましい。
R
とりわけ、 R 1と R 2とが隣 b接する窒素原子と共にピペリジノ、 ピロリジン 一 1ーィルなどを形成する場合が好ましい。
R 1および R 2が隣接する窒素原子とともに形成する 「置換基を有していて もよい含窒素複素環」 は、 好ましくは
[式中の記号は、 前記と同意義を示す] である。
ここで、 Rbで示される 「置換基を有していてもよい炭ィ匕水素基」 として は、 例えば前記 R 3として例示したものが挙げられる。 Rbは、好ましくは置 換基を有していてもよい炭化水素基であり、 その具体例としては、 例えばハ ロゲン化されていてもよい C ^6アルキル (例、 メチル、 ェチルなど) ;ハロ ゲン原子 (例、 フッ素、 塩素など) 、 ハロゲン化されていてもよい C r_6アル キル(例、 メチルなど)および八ロゲン化されていてもよい C ^6アルコキシ (例、 メトキシなど) から選ばれる 1ないし 3個の置換基を有していてもよ い C 6_14ァリール (例、 フエニル、 ナフチルなど) ; ヒドロキシ一C !_67 ルキル; C アルコキシ一力ルポ二ルー C i_6アルキル (例、 エトキシカル ポニルメチルなど) ;Cト 3アルキレンジォキシ(例、 メチレンジォキシなど) で置換されていてもよい C 7^ 9ァラルキル (例、 ベンジル、 ジフエ二ルメチ ルなど) ; C 8_19ァリ一ルアルケニル (例、 3—フエ二ルー 2—プロブー 2 一ェニルなど) ; 5ないし 8員の単環式非芳香族複素環基一 C x― 6アルキル(例、 ピロリジニルメチルなど) ; 1ないし 3個の C ^6アルキルで置換されていて
もよい C 6_14ァリール一アミノー C 6アル宁ル (例、 2,6 -ジメチルフエ二 ルァミノメチルなど) などが挙げられる。 Rbは、 さらに好ましくは置換基 を有していてもよい C 6— 14ァリールである。
Zは、 好ましくは CHである。
式 (1",") 中、 Rcで示される 「置換基を有していてもよい炭化水素基」 としては、 前記 Rbとして例示したものが挙げられる。 Rcは、 好ましくは 置換基を有していてもよい C 6— 14ァリールである。
R 2が瞵接する窒素原子および Yとともに形成する 「置換基を有していても よい含窒素複素環」 としては、 前記 R1と R 2とが隣接する窒素原子と共に形 ' 成する 「置換基を有していてもよい含窒素複素環」 と同様のものが挙げられ る。 式(I)で表される化合物の好適な例としては、式(1,) (Γ')、 (Γ")、 ( I "") ( I '"") などで表される化合物が挙げられる。
式( I )で表される化合物のうち、式( I,) . ( I ") (I ",')または ( I "") で表される化合物は新規化合物である。
式 (1,) で表される化合物の好適な例としては、 以下の化合物が挙げられ る。
(Ε)- 3- [1- [4- [(4 -メトキシベンジル)ォキシ]ベンゾィル ]-2, 3-ジヒドロ- 1H - ィンドール- 5-ィル] -Ν,Ν-ジメチル- 2-プロペン-卜ァミン;
(Ε) -3-[1- [4- [ (4-メチルベンジル)ォキシ]ベンゾィル] -2, 3 -ジヒド口- -ィ ンドール- 5-ィル] Ν-ジメチル -2-プロペン-卜アミン;
(Ε) -3- [1- [4- [ (4—クロロベンジル)ォキシ]ベンゾィル] -2, 3 -ジヒドロー 1H -ィ ンドール- 5-ィル] -Ν,Ν-ジメチル- 2-プロペン- 1-ァミン;
1_ [ [6- (4-クロロフェニル) -3-ピリジニル]力ルポニル] -6- [ (Ε) -3- (卜ピロリ ジニル )-1-プロぺニル ]ニ1, 2, 3, 4-テトラヒドロキノリン;
卜 [[6- (4-フルオロフェニル )-3-ピリジニル]力ルポニル] -6- [(E)- 3- (卜ピロ リジニル)-1 -プロべニル] - 1, 2, 3 ·4-テトラヒドロキノリン;
1 - [ [6 - (4-メチルフエニル) -3-ピリジニル]力ルポニル] -6- [ (E) - 3 - (1 -ピロリ ジニル) -卜プロぺニル ]-1, 2, 3, 4 -テトラヒドロキノリン;
1-[[6- (4-ク口口フエニル) -3-ピリジニル]カルボニル] -6- [ (E) - 3-ジメチル ァミノ- 1-プロぺニル ]-1, 2, 3, 4-テトラヒドロキノリン;
1- [ [6- (4-フルオロフェニル) -3-ピリジニル]力ルポニル] -6- [ (E) -3-ジメチ ルァミノ-卜プロぺニル ]-1,2, 3, 4-テトラヒドロキノリン;
卜 [ [6- (4 -メチルフエ二ル)- 3-ピリジニル]カルボ二ル]- 6- [ (E) -3-ジメチル ァミノ- 1-プロぺニル ]-1,2, 3, 4 -テトラヒドロキノリン;
1 - [ [6- (4-クロ口フエニル) -3-ピリジニル]力ルポニル] -6- [ (E) - 4- (トビ口リ ジニル )-1-ブテニル]- 1,2, 3, 4-テ卜ラヒドロキノリン; ,
1 - [ [6- (4 -フルオロフェニル) -3 -ピリジニル]力ルポニル] -6- [(B) -4- (卜ピロ リジニル) -卜ブテエル]- 1,2, 3, 4 -テトラヒドロキノリン;
1-[[6- (4-メチルフエニル) -3-ピリジニル]力ルポ二ル]- 6- [ (E) + (1 -ピロリ ジニル) -1 -ブテニル] - 1, 2, 3, 4-テ卜ラヒドロキノリン;
1一 [ [6- (4—クロ口フエエル) -3-ピリジニル]カルボニル] -6- [ (E) -4 -ジメチル ァミノ- 1-ブテニル]- 1, 2, 3, 4-テトラヒドロキノリン;
1 - [ [6 - (4-フルオロフェニル) - 3 -ピリジニル]力ルポニル] -6- [ (E) - 4 -ジメチ ルァミノ-卜ブテニル]- 1,2, 3, 4 -テトラヒドロキノリン;'
1 - [ [6- (4-メチルフエニル) -3-ピリジニル]力ルポ二ル]- 6- [ (E) -4 -ジメチル ァミノ- 1-ブテニル]- 1, 2, 3, 4-テトラヒドロキノリン;
(E) -N, N-ジメチル -3- [1-[[4- (4-メチルフエニル) -卜ピぺリジニル]力ルポ二 ル]- 1, 2, 3, 4-テトラヒド口- 6 -キノリニル] -2-プロペン-卜ァミン;
(E) -N, N-ジメチル -3- [1- [ [4- (4-フルォ口フエニル) -卜ピぺリジニル]力ルポ ニル] - 1, 2, 3, 4-テ卜ラヒド口- 6 -キノリニル] - 2 -プロべン- 1 -ァミン;
(E) -N, N-ジメチル -3- [卜 [ [4- (4-クロ口フエニル) -卜ピペリジニル]力ルポ二 ル] -1, 2, 3, 4 -テ卜ラヒド ΰ - 6 -キノリニル] -2 -プロペン -1-ァミン;
卜 [[4- (4-メチルフエ二ル)-卜ピベリジニル]力ルポエル]- 6- [(E)- 3- (卜ピロ リジニル) -卜プロぺニル 2, 3, 4 -テトラヒドロキノリン;
1-[[4- (4 -フルォ口フエニル) -1-ピぺリジニル]力ルポニル] -6- C (Ε) -3- (卜ピ'
口リジニル) - 1 -プロべニル] - 1, 2, 3, 4-テトラヒドロキノリン;
1 - [ [4- (4-クロ口フエニル) - 1 -ピぺリジニル]力ルポニル] -6- [ (E) -3- (卜ピロ リジニル プロぺニル ] -1, 2, 3, 4 -テトラヒドロキノリン;
(E) -3- [1- [ [4- (4 -クロロフェニル) -卜ピペラジニル]カルボニル] -1, 2, 3, 4- テ.トラヒドロ -6-キノリニル] - Ν, Ν-ジメチル -2-プロペン-卜ァミン;
(Ε) -3- [1- [ [4- (4-メチルフエニル) -1 -ピぺラジニル]力ルポニル] -1 , 2, 3, 4 - テトラヒドロ- 6 -キノリニル] - Ν,Ν -ジメチル- 2-プロペン - 1-ァミン; (Ε) -3- [卜 [ [4- (4-フルオロフェニル ) -1 -ピペラジニル]カルボニル] - 1, 2, 3, 4-テトラヒドロ - 6 -キノリニル] -Ν, Ν -ジメチル- 2 -プロべン -1 -ァミ ン;
1 - [ [5 - (4 -フルォ口フエニル) -2-ピリジニル]力ルポニル] -6- [ (Ε) -3- α -ピ口 リジニル) -卜プロぺニル ] _1, 2, 3, 4 -テトラヒドロキノリン;
1- [ [5- (4-メチルフェニル) -2-ピリジニル]力ルポニル] -6- [ (Ε) - 3- (1 -ピロリ ジニル) -卜プロぺニル ] - 1, 2, 3, 4 -テトラヒドロキノリン;
卜 [ [6- (4-クロ口フエニル) -3-ピリジニル]カルボニル] -6- [ (卜メチル- 3-ピ ペリジニリデン)メチル ] -1, 2, 3, 4 -テトラヒドロキノリン;
卜 [5- (4—クロ口フエニル)—2—フロイル]—6 - [ (Ε) -3- (4-フェ二ル-卜ピぺリジ ニル) -卜プロぺニル ] -1, 2, 3, 4-テトラヒドロキノリン。 式 (Γ') で表される化合物の好適な例としては、 以下の化合物が挙げられ る。
4 - [4 -(4-クロ口フエ二ル) - 1-ピペリジニル ]-4-ォキソ - 1- (1, 2, 3, 4 -テトラヒ ドロ- 7-イソキノリニル) - 1-ブタノン;
4 - [4- (4-クロ口フエニル) -1-ピペリジニル ] -4-ォキソ -卜(2, 3, 4, 5 -テトラヒ ドロ- 1H- 3-ベンズァゼピン- 7-ィル) -卜ブ夕ノン;
4 - [4- (4-クロ口フエニル) -卜ピペリジニル] -4-ォキソ- 1 - (3-メチル- 2, 3, 4, 5 -テトラヒドロ- 1H-3-ベンズァゼピン- 7-ィル) -卜ブ夕ノン; 4 - [4- (4 -クロロフェニル ) - 1-ピぺリジニル] -1- (3-ェチル- 2, 3, 4, 5 -テトラヒ ドロ- 1H- 3-ベンズァゼピン- 7-ィル) -4 -ォキソ -1-ブタノン;
4 - [4- (4-クロロフェニル) -卜ピぺリジニル] -4 -ォキソ -卜(3-プロピル- 2, 3, 4, 5-テトラヒドロ- 1H-3-ベンズァゼピン - 7 -ィル) -1-ブ夕ノン; 1- (3 -ベンジル- 2, 3, 4, 5-テトラヒド口- 1H- 3_ベンズァゼピン- 7-ィル) -4- [4- (4-クロ口フエニル) -卜ピペリジニル ]-4-ォキソ -卜ブ夕ノン;
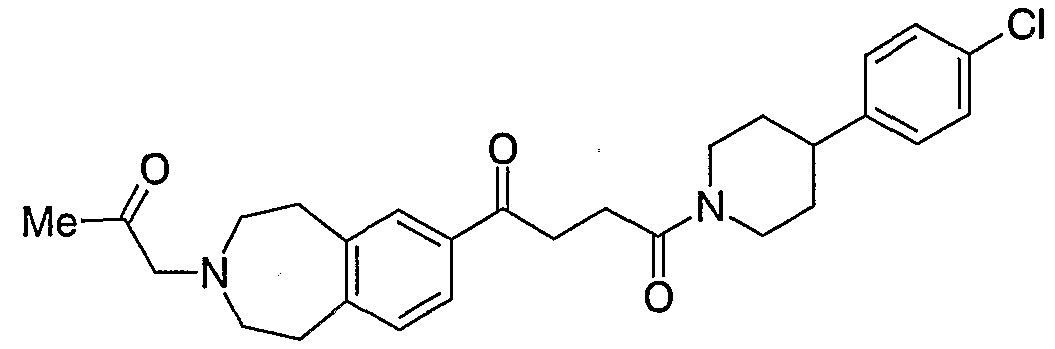
1 -(3-ァセチル- 2,3, 4, 5 -テトラヒドロ- 1H- 3 -ベンズァゼピン- 7 -ィル) -4- [4- (4-ク口口フエニル) -卜ピペリジニル ] -4-ォキソ -1-ブ夕ノン;
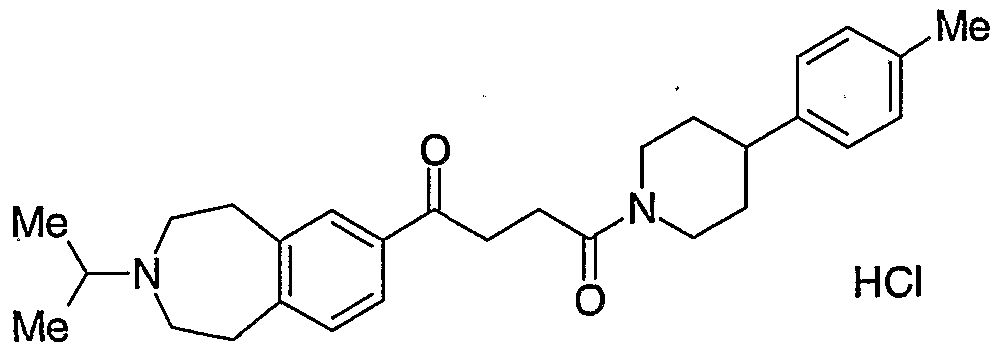
4- [4- (4-クロロフェニル)ピぺリジン-トイル] -1- (3 -ィソプロピル- 2, 3, 4, 5- テトラヒドロ- 1H- 3-ベンズァゼピン- 7-ィル) -4-ォキソブタン- 1-オン; 4- [4- (4-クロ口フエニル) -1-ピペリジニル ] -4-ォキソ -卜(2, 3, 4, 5-テ卜ラヒ ドロ- 1H- 2-ベンズァゼピン- 8-ィル) -卜ブタノン;
4- [4- (4 -ク口口フエ二ル) - 1 -ピぺリジニル] -1- (2-メチル- 2, 3, 4, 5-テトラヒ ドロ- 1H- 2-ベンズァゼピン- 8-ィル) -4-ォキソ -卜ブ夕ノン; · 4- [4- (4-ク口口フエニル) - 1-ピぺリジニル] -卜(2, 3 -ジヒド口- 1H-ィソイン ドール- 5-ィル) -4-ォキソ -1-ブ夕ノン。 上記した式 (1,) または (1 ") で表される化合物以外に、 式 (I ) で表さ れる化合物の好適な例としては、 以下の化合物が挙げられる。
(E) -3- [1- [ (4' -クロ口 [1, Γ -ビフエニル] -4 -ィル)力ルポニル] - 1 , 2, 3, 4-テ トラヒドロ- 6 -キノリニル] - Ν, Ν -ジメチル- 2-プロペン- 1-ァミン;
1- [ (4' -クロ口 [1, Γ _ビフェニル] - 4-ィル)力ルポニル] -6 - [ (Ε) -3-ピぺリジ ノ-卜プロぺニリレ] -1, 2, 3, 4-テトラヒドロキノリン;
(Ε) -3- [卜 [ ( [1 , -ビフエニル] -4-ィル)力ルポニル] -2, 3-ジヒドロ- 1H -イン ドール- 5 -ィル] -Ν, Ν-ジメチル- 2 -プロペン-卜ァミン;
(Ε) - 3 - [卜 [ (4' -クロ口 [1 , 1 ' -ピフエニル] -4-ィル)力ルポニル] -2, 3 -ジヒド ロ- 1H-ィンドール- 5-ィル] -Ν, Ν -ジメチル- 2-プロペン-卜ァミン;
(Ε) - 4- [1 _ [ (4' -クロ口 [1, Γ -ビフエニル] -4-ィル)力ルポニル] -1, 2, 3, 4- - トラヒドロ- 6 -キノリニル] - Ν, Ν-ジメチル- 3-ブテン- 1 -ァミン;
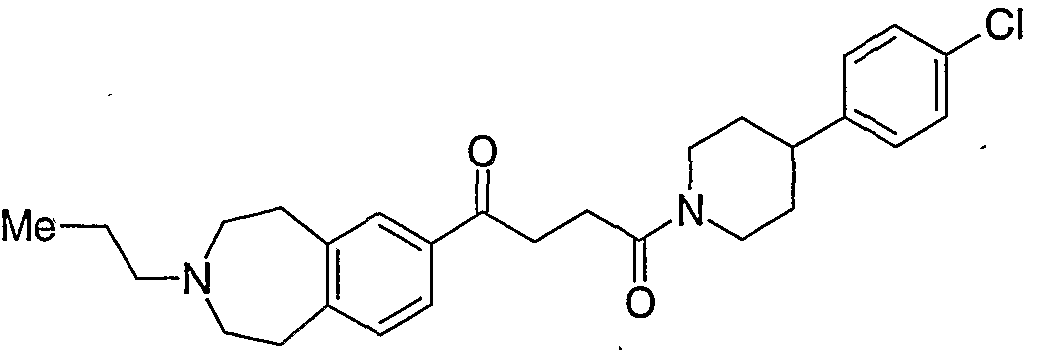
1_ (3-ァセチル- 2, 3, 4, 5-テトラヒドロ- 1H- 3 -ベンズァゼピン- 7-ィル) -4- [4-
(4-クロ口フエニル) -卜ピぺリジニル] -卜ブ夕ノン;
4- [4- (4 -クロ口フエニル) -卜ピペリジニリレ] - 1- (2, 3, 4, 5 -テトラヒドロ- 1H -
3-ベンズァゼピン- 7-ィル) -卜ブ夕ノン; '
4- [4- (4 -クロ口フエニル) - 1-ピぺリジニル] -卜(3-メチル -2, 3, 4, 5-テトラヒ ドロ- 1H-3-ベンズァゼピン- 7-ィル) -卜ブタノン;
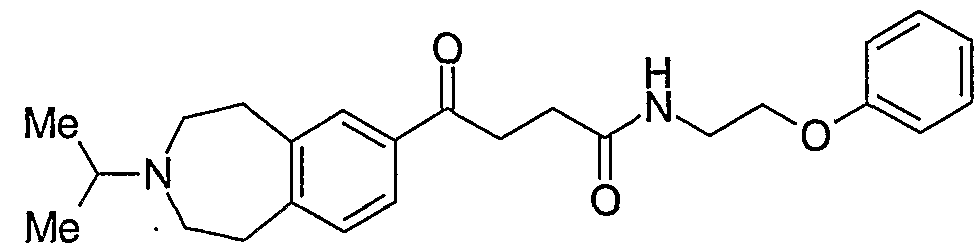
4-ォキソ -N- (2-フエネチル ) - 4- (2, 3,4, 5-テトラヒドロ- 1H- 3-ベンズァゼピ ン- 7-ィル)ブタンアミド;
4 -ォキソ -N- (3-フエニルプロピル) - 4- (2, 3, 4, 5-テトラヒドロ _1Η- 3-ベンズ ァゼピン- 7-ィル)ブタンアミド;
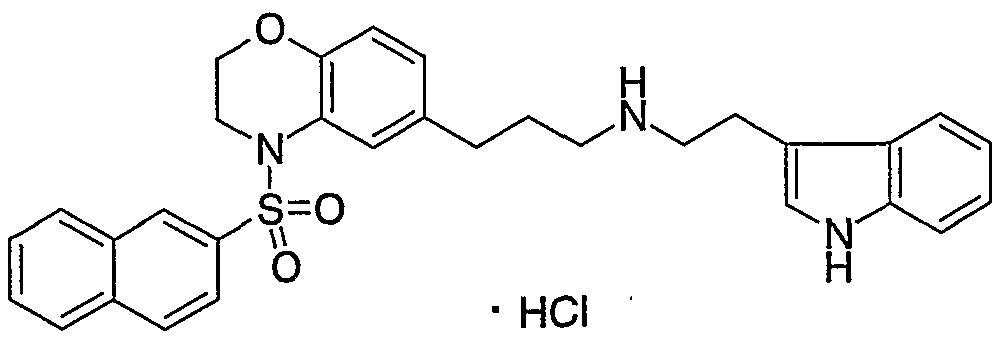
Ν - [2- ( 1 Η -ィンドール - 3 -ィル)ェチル] -4-ォキゾ - 4_ (2 , 3, 4, 5-テ卜ラヒドロ -1H-3-ベンズァゼピン- 7-ィル)ブタンアミド。
また、 式 (I ) で表される化合物の好適な例としては、 以下の化合物も挙 げられる。
7- [3- [4- (4 -クロ口フエニル)ピぺリジン-トイル]プロポキシ ] -2, 3, 4, 5 -テト ラヒドロ- 1H-3-ベンズァゼピン、
7- [3- [4- (4-ク口口フエニル) -卜ピぺリジニル]プロボキシ] -3-メチル- 2, 3, 4, 5-テトラヒド口- 1H- 3-ベンズァゼピン、
7- [3- [4- (4-ク口口フエニル) -1-ピぺリジニル]プロボキシ] -3-ィソプロピル -2, 3, 4, 5-テトラヒド口- 1H- 3-ベンズァゼピン、
7- [3- [4- (4-クロ口フエニル) -卜ピペリジニル]プロボキシ] -3-シク口ペンチ ル- 2,3, 4,5-テトラヒドロ- 1H- 3-ベンズァゼピン、
3 -ベンジル- 7- [3- [4- (4-クロ口フエニル) -卜ピペリジニル]プロボキシ] - 2, 3, 4, 5-テトラヒド口- 1H-3-ベンズァゼピン、
3 -ァセチル- 7- [3- [4- (4-ク口口フエニル) -卜ピぺリジニル]プロボキシ] - 2, 3, 4, 5 -テトラヒド口- 1H-3 -ベンズァゼピン、
7- [3- [4- (4-クロ口フエニル) -卜ピペリジニル]プロボキシ] -3-ィソプチリル - 2, 3, 4, 5-テトラヒドロ- 1H-3-ベンズァゼピン、
3-ベンゾィル- 7 - [3- [4- (4-クロ口フエニル) -卜ピぺリジニル]プロポキシ] - 2, 3, 4, 5 -テトラヒド口- 1H - 3-ベンズァゼピン、.
ter t-プチル 7- [3- [4- (4-クロ口フエニル) -卜ピペリジニル]プロ.ポキシ] -
1, 2, 4, 5-テトラヒドロ- m_3 -ベンズァゼピン- 3 -力ルポキシレート、 7- [3 - [4- (4 -クロ口フエエル) -1 -ピペリジニル]プロポキシ] -3- (メチルスル フォニル) -2, 3, 4, 5 -テトラヒドロ- 1H-3-ベンズァゼピン、
7- [3- [4- (4-クロ口フエニル) -卜ピぺリジニル]プロポキシ] - N-ェチル- 1, 2, 4, 5 -テトラヒドロ - 3H-3-ベ ズァゼピン- 3-力ルポキサミド、
7- [3- [4- (4-フルオロフェニル) - 1 -ピペリジニル]プロポキシ] -3-ィソプロピ ル- 2, 3, 4, 5-テトラヒドロ- 1H- 3-ベンズァゼピン、
7- [3- [4- (2, 4 -ジフルオロフェニル) -卜ピペリジニル]プロポキシ] - 3-ィソプ 口ピル - 2, 3, 4, 5-テトラヒド口- 1H- 3-ベンズァゼピン、
7- [3- [4- (4-メチルフエニル) -卜ピぺリジニル]プロポキシ] -3-ィソプロピル -2, 3, 4, 5-テトラヒド口- 1H- 3_ベンズァゼピン、
3 -ィソプロピル- 7- [3- [4- (3-メチルフエニル) -1-ピぺリジニル]プロポキ シ] - 2, 3, 4, 5-テトラヒド口- 1H- 3-ベンズァゼピン、
3 -ィソプロピル- 7- [3- [4- (2-メチルフエニル) -卜ピペリジニル]プロポキ シ] -2, 3, 4, 5-テトラヒドロ- 1H- 3 -ベンズァゼピン、
3-ィソプロピル- 7- [3- [4- (4 -メトキシフエ二ル) -卜ピぺリジニル]プロポキ シ] - 2, 3, 4, 5-テトラヒドロ - 1H- 3_ベンズァゼピン、
3-ィソプロピル- 7- [3- [4- (3-トリフルォロメチルフエニル) -1-ピぺリジニ ル]プロポキシ ] -2, 3, 4, 5-テトラヒド口- 1H- 3-ベンズァゼピン、
3-ァセチル- 7- [3- [4- (4-メチルフエニル) -卜ピぺリジニル]プロポキシ〕 - 2, 3, 4, 5-テトラヒドロ- 1H- 3-ベンズァゼピン、
3 -ァセチル- 7- [3- [4- (4-メトキシフエニル) -卜ピベリジニル]プロボキシ] - 2, 3, 4, 5-テトラヒドロ- 1H - 3-ベンズァゼピン、
3-ィソプチリル -7- [3- [4- (4-メチルフェニル) -卜ピペリジニル]プロポキ シ] -2, 3, 4, 5-テトラヒドロ- 1H-3-ベンズァゼピン、
3 -ィソプチリル -7- [3- [4- (4-メトキシフエ二ル) - 1-ピぺリジニル] 'プロポキ シ] -2, 3, 4, 5-テトラヒドロ- 1H-3-ベンズァゼピン、
7- [3- [4- (4 -メチルフエニル) -1-ピぺリジニル]プロボキシ] -3- (メチルスル フォニル) -2, 3, 4, 5-テトラヒドロ- 1H-3-ベンズァゼピン、
7 - [3- [4- (4-メトキシフエ二ル) -卜ピベリジニル]プロポキシ ] -3- '(メチルス ルフォニル) - 2, 3,4,5-テトラヒドロ- 1H- 3 -ベンズァゼピン、
3 -ァセチル- 7- [3- [4- (4-フルォ口フエニル) -1-ピぺリジニル]プロボキシ] - 2, 3, 4, 5-テトラヒドロ- 1H-3-ベンズァゼピン、
3-ァセチル- 7- [3- [4- (3-フルオロフェニル) -卜ピベリジニル]プロボキシ] - 2, 3, 4, 5 -テトラヒドロ- 1H- 3 -ベンズァゼピン、
3 -ァセチル- 7- [3- [4- (2, 4-ジフルォロフェニル) -1-ピぺリジニル]プロポキ シ] - 2, 3, 4, 5 -テトラヒド口- m_3-ベンズァゼピン、
3 -ァセチル- 7 - [3- [4 - (4-メチルフエニル) - 1-ピぺリジニル]プロポキシ]― 2, 3, 4, 5 -テトラヒドロ- 1H - 3-ベンズァゼピン、
3 -ァセチル -7- [3- [4- (3-メチルフエニル) -卜ピぺリジニル]プロポキシ] - 2, 3, 4, 5-テトラヒド口- 1Η- 3-ベンズァゼピン、
3-ァセチル- 7- [3- [4- (2-メチルフエ二ル) - 1-ピぺリジニル]プロボキシ] - 2, 3, 4, 5 -テトラヒド口- 1H- 3-ベンズァゼピン、
3 -ァセチル- 7- [3- [4- (4 -メトキシフエ二ル) - 1 -ピペリジニル]プロボキシ] - 2, 3, 4, 5 -テトラヒド口- 1H - 3-ベンズァゼピン、
3 - [ (3 -ィソプロピル- 2, 3, 4, 5-テトラヒドロ- 1H-3 -ベンズァゼピン- 7 -ィル) ォキシ] -N- [3- (4-メチルフエニル)プロピル]プロパンアミド、
N - [3- (4-クロロフエ二ル)プロピル] -3- [ (3-ィソプロピル- 2, 3, 4, 5-テトラヒ ドロ- 1H-3 -ベンズァゼピン- 7-ィル)ォキシ]プロパンアミド、
N- [3- (3 -ク口口フエニル)プロピル] -3- [ (3 -ィソプロピル- 2, 3, 4, 5 -テトラヒ ド口- 1 H- 3-ベンズァゼピン -7-ィル)ォキシ]プロパンアミド、
N- [3- (2-クロ口フエニル)プロピル] -3- [ (3-ィソプロピル -2, 3, 4, 5-テトラヒ ドロ- 1H- 3 -ベンズァゼピン- 7-ィル)ォキシ]プロパンアミド、
3 -(4-ク口口フエニル) - N- [3- [ (3-ィソプロピル -2, 3, 4, 5-テトラヒド口- 1H - 3-ベンゾァゼピン -7 -ィル)ォキシ]プロピル] - 1 -プロパンァミン、
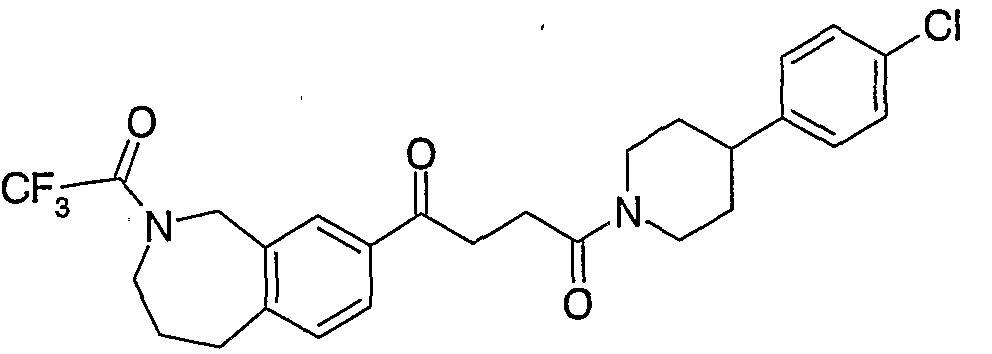
(E) - 4- [4- (4-クロ口フエニル) - 1-ピペリジニル] - 4-ォキソ -1- [3 - (トリフル ォロアセチル ) -2, 3, 4, 5-テトラヒドロ- 1H- 3-ベンズァゼピン- 7-ィル] -2-ブ テン- 1-オン、
(E)_4 - [4_ (4-クロ口フエニル) -1 -ピペリジニル ] -4-ォキソ _1 -(2, 3, 4, 5-テト ラヒドロ -1H- 3-ベンズァゼピン- 7-ィル) -2-ブテン-卜オン、
(E) - 4- [4- (4-クロ口フエ二ル) - 1-ピペリジニル ] -1- (3-イソプロピル- , 2, 3, 4, 5-テトラヒドロ- 1H- 3 -ベンズァゼピン- 7-ィル) -4-ォキソ -2-ブテン - 1-オン、
8_ [3- [4- (4-クロロフエ二ル) - 1 -ピペリジニル]プロポキシ ] -3-ィソプロピル -2, 3, 4, 5 -テトラヒドロ- 1H-2-ベンズァゼピン、
8 - [3- [4- (4-クロ口フエニル) -1-ピペリジニル]プロポキシ ] -3-シクロペンチ ル -2, 3, 4, 5 -テトラヒド口- 1H- 2 -ベンズァゼピン、
2-ベンジル -8- [3- [4- (4-クロロフェニル) - 1-ピぺリジニル]プロポキシ] - 2, 3, 4, 5 -テトラヒドロ- 1H-2-ベンズァゼピン、
8- [3- [4- (4 -クロ口フエニル) - 1 -ピぺリジニル]プロボキシ] -2-ィソプチリル -2, 3, 4, 5 -テトラヒドロ- 1H-2-ベンズァゼピン、
2 -べンゾィル- 8- [3- [4- (4-クロ口フエニル) -卜ピペリジニル]プロポキシ] - 2, 3, 4, 5 -テ'トラヒドロ- 1H - 2 -ベンズァゼピン、
8- [3- [4- (4-クロ口フエニル) -1-ピぺリジニル]プロボキシ] -2- (メチルスル フォニル) -2, 3, 4, 5 -テトラヒドロ- 1H- 2-ベンズァゼピン、
8- [3- [4- (4-ク口口フエ二ソレ) -1-ピぺリジニノレ]プロポキシ] - N-ェチル- 1, 3, 4, 5 -テトラヒドロ- 2H- 2 -ベンズァゼピン- 2-力ルポキサミド、
8- [3- [4- (4-フルオロフェニル) -卜ピペリジニル]プロボキシ] :2 -イソプロピ ル -2, 3, 4, 5-テトラヒド口- 1H - 2-ベンズァゼピン、
8- [3- [4- (2, 4-ジフルオロフェエル) -卜ピぺリジニル]プロポキシ] -2 -ィソプ 口ピル- 2, 3, 4, 5-テトラヒドロ- 1H-2-ベンズァゼピン、
8 - [3- [4- (4-メチルフエ二ル) - 1-ピペリジニル]プロポキシ ] -2-ィソプロピル -2, 3, 4, 5 -テトラヒドロ- 1H- 2 -ベンズァゼピン、
2-ィソプロピル- 8- [3- [4- (3-メチルフエ二ル) -卜ピぺリジニル]プロポキ シ] -2, 3, 4, 5-テトラヒド口- 1H- 2-ベンズァゼピン、
2-ィソプロピル- 8- [3- [4- (2-メチルフエニル) -1-ピペリジニル]プロポキ シ] - 2, 3, 4, 5-テトラヒドロ- 1H - 2-ベンズァゼピン、
2 -イソプロピル- 8- [3- [4- (4-メトキシフエニル) -1-ピベリジニル]プロポキ シ]一 2, 3, 4, 5 -テトラヒドロ- 1H - 2-ベンズァゼピン、
2 -ィソプロピレ- 8- [3- [4- (3-トリフルォロメチルフエニル) -1-ピぺリジニ ル]プロポキシ ] -2, 3, 4, 5-テトラヒド口- 1H- 2-ベンズァゼピン、
2-ァセチル- 8- [3- [4- (4-メチルフエ二ル) - 1-ピベリジニル]プロボキシ] - 2, 3, 4, 5-テトラヒド口- 1H - 2-ベンズァゼピン、
2 -ァセチル- 8- [3- [4- (4-メトキシフエ二ル) - 1-ピベリジニル]プロボキシ] - 2, 3, 4, 5 -テトラヒド口- 1H- 2-ベンズァゼピン、
2 -ィソプチリル- 8- [3- [4- (4-メチルフエニル) - 1-ピぺリジニル]プロポキ シ] - 2, 3, 4, 5 -テトラヒドロ- 1H- 2-ベンズァゼピン、
2 -ィソプチリル- 8- [3- [4- (4 -メトキシフエ二ル) -卜ピぺリジニル]プロポキ シ] - 2, 3, 4, 5-テトラヒドロ- 1H- 2-ベンズァゼピン、
8 - [3- [4- (4-メチルフエ二ル) - 1-ピベリジニル]プロポキシ ] -2- (メチルスル フォニル) -2, 3, 4, 5 -テトラヒドロ- 1H-2-ベンズァゼピン、
8- [3- [4- (4-メトキシフエニル) -卜ピペリジニル]プロボキシ] - 2- (メチルス ルフォニル) -2, 3, 4, 5 -テトラヒドロ- 1H-2 -ベンズァゼピン、
2 -ァセテル- 8- [3- [4- (4-フルオロフェニル) -卜ピぺリジニル]プロポキシ] - 2, 3, 4, 5-テトラヒドロ- 1H-2-ベンズァゼピン、
2 -ァセチル -8 - [3- [4- (3 -フルォ口フエニル) -卜ピぺリジニル]プロボキシ] - 2, 3, 4, 5-テトラヒドロ- 1H-2-ベンズァゼピン、
2 -ァセチル- 8- [3- [4- (2, 4-ジフルオロフェニル) -卜ピペリジニル]プロポキ シ] - 2, 3, 4, 5 -テトラヒドロ- 1H- 2 -ベンズァゼピン、
2 -ァセチル -8- [3- [4- (4-メチルフエニル) - 1-ピぺリジニル]プロボキシ] -
2, 3, 4, 5-テトラヒドロ 2-ベンズァゼピン、
2-ァセチル -8- [3- [4- (3-メチルフエニル) -1-ピぺリジニル]プロボキシ] -
2, 3, 4, 5-テトラヒドロ- 1H- 2 -べンズァゼピン、
2 -ァセチル -8- [3- [4- (2-メチルフエニル) -1-ピぺリジニル]プロボキシ] - 2, 3, 4, 5-テトラヒド口- 1H- 2 -ベンズァゼピン、
2 -ァセチル- 8- [3- [4- (4-メトキシフエ二ル) -卜ピぺリジニル]プロボキシ] -
2, 3, 4, 5-テトラヒドロ- 1H-2-ベンズァゼピン、
3- [ (2 -ィソプロピル- 2, 3, 4, 5-テトラヒドロ- 1H- 2-ベンズァゼピン -8-ィル) ォキシ] - N- [3- (4-メチルフヱニル)プロピル]プロパンアミド、
N- [3- (4-クロロフェニル)プロピル] -3- [ (2-ィソプロピル - 2 3, 4, 5 -テトラヒ ドロ- 1H- 2-ベンズァゼピン- 8-ィル)ォキシ]プロパンアミド、
N- [3- (3 -クロロフェニル)プロピル] -3- [ (2-ィソプロピル- 2, 3, 4, 5 -テトラヒ ド口- m- 2-ベンズァゼピン- 8-ィル)ォキシ]プロパンアミド、
N- [3- (2 -クロロフェニル)プロピル] -3- [ (2 -ィソプロピル _2, 3, 4, 5 -テトラヒ ド口- 1H- 2-ベンズァゼピン- 8-ィル)ォキシ]プロパンアミド、
3 - (4 -ク口口フエニル) -N- [3- [ (2 -ィソプロピル- 2, 3, 4, 5-テトラヒド Π-1Η- 2-ベンゾァゼピン- 8 -ィル)才キシ]プロピル] -卜プロパンァミン。 化合物 ( I ) 、 ( I,) 、 ( I ") 、 (I "り 、 ( I,,,,) または ( I,,,") の塩 としては、 例えば、 無機塩基との塩、 アンモニゥム塩、 有機塩基との塩、 無 機酸との塩、 有機酸との塩、 塩基性または酸性アミノ酸との塩などが挙げら れる。 .
無機塩基との塩の好適な例としては、 例えば、 ナトリウム塩、 カリウム塩 などのアルカリ金属塩;カルシウム塩、 マグネシウム塩、 バリウム塩などの アルカリ土類金属塩;アルミニウム塩などが挙げられる。
有機塩基との塩の好適な例としては、 例えば、 トリメチルァミン、 トリエ チルァミン、 ピリジン、 ピコリン、 エタノールァミン、 ジエタノールァミン、 トリエタノールァミン、 ジシクロへキシルァミン、 Ν, Ν—ジベンジルエチレン ジアミンなどとの塩が挙げられる。
無機酸との塩の好適な例としては、 例えば、 塩酸、 臭化水素酸、 硝酸、 硫 酸、 リン酸などとの塩が挙げられる。
有機酸との塩の好適な例としては、 例えば、 ギ酸、 酢酸、 トリフルォロ酢 酸、 フマル酸、 シユウ酸、 酒石酸、 マレイン酸、 クェン酸、 コハク酸、 リン ゴ酸、 メタンスルホン酸、 ベンゼンスルホン酸、 Ρ—トルエンスルホン酸など との塩が挙げられる。
塩基性アミノ酸との塩の好適な例としては、 例えば、 アルギニン、 リジン、 オル二チンなどとの塩が挙げられ、酸性アミノ酸との塩の好適な例としては、 例えば、 ァスパラギン酸、 グルタミン酸などとの塩が挙げられる。
これらの塩のなかでも、 薬学的に許容し得る塩が好ましい。 例えば、 化合 物 (I ) 、 ( 1 ') 、 U ") 、 ( I '") 、 ( I "") または ( I '"") は、 酸性官 能基を有する場合、アルカリ金属塩 (例えば、ナトリウム塩、カリウム塩など)、 アルカリ土類金属塩 (例えば、 カルシウム塩、 マグネシウム塩、 バリウム塩な ど)などの無機塩、 アンモニゥム塩などを形成していてもよい。 また、 化合物 ( 1 ) 、 (Ι,) 、 (Γ') 、 (Γ") 、 (Γ",) または (1 ""') は、 塩基性官 能基を有する場合、塩酸塩、硫酸塩、 リン酸塩、臭化水素酸塩などの無機塩; または酢酸塩、 マレイン酸塩、 フマル酸塩、 コハク酸塩、 メタンスルホン酸 塩、 ρ—トルエンスルホン酸塩、 クェン酸塩、 酒石酸塩などの有機塩を形成し ていてもよい。
化合物 (I ) 、 (1,) 、 (Γゥ 、 ( I "0 、 ( I "") および ( I ""') (以 下、 本発明化合物と略記することがある) は、 無水物、 水和物のいずれであ つてもよい。 水和物の場合、 0. 5ないし 3個の水分子を有していてもよい さらに、 本発明化合物は、 同位元素 (例、 3H、 1 4 C、 3 5 Sなど) で標識 されていてもよい。 本発明化合物が、 光学異性体、 立体異性体、 位置異性体、 回転異性体を含 有する場合には、 これらも本発明化合物.として含有されるとともに、 自体公 知の合成手法、 分離手法によりそれぞれを単品として得ることができる。 例 えば、 本発明化合物に光学異性体が存在する場合には、 該化合物から分割さ れた光学異性体も本発明化合物に包含される。
該光学異性体は、 自体公知の方法により製造することができる。 具体的に は、 光学活性な合成中間体を用いる、 または、 最終物のラセミ体の混合物を 常法に従つて光学分割することにより光学異性体を得る。
光学分割法としては、 自体公知の方法、 例えば、 以下に詳述する分別再結 晶法、 キラルカラム法、 ジァステレオマー法等が用いられる。
1)分別再結晶法 .
ラセミ体と光学活性な化合物 (例えば、 (+)—マンデル酸、 (一)—マンデル 酸、 (+)—酒石酸、 (―)—酒石酸、 (+)—1—フエネチルァミン、 (―)ー1—フ エネチルァミン、 シンコニン、 (―)一シンコニジン、 ブルシンなど)と塩を形 成させ、 これを分別再結晶法によって分離し、 所望により、 中和工程を経て フリ一の光学異性体を得る方法。
2)キラルカラム法
ラセミ体またはその塩を光学異性体分離用カラム(キラルカラム)にかけて 分離する方法。例えば液体クロマトグラフィの場合、 ENANTIO— 0VM (トーソ一 社製)あるいは、 ダイセル社製 CHIRALシリーズなどのキラルカラムに光学異 性体の混合物を添加し、 水、 種々の緩衝液 (例えば、 リン酸緩衝液)、 有機溶 媒 (例えば、 エタノール、 メタノール、 イソプロパノール、 ァセトニトリル、 トリフルォロ酢酸、ジェチルァミンなど)を単独あるいは混合した溶液として 展開させることにより、 光学異性体を分離する。 また、 例えば、 ガスクロマ トグラフィ一の場合、 CP— Chi ras i l _DeX CB (ジーエルサイエンス社製)など のキラルカラムを使用して分離する。
3)ジァステレオマ一法
ラセミ体の混合物を光学活性な試薬と化学反応によってジァステレオマ一 の混合物とし、 これを通常の分離手段 (例えば、 分別再結晶、 クロマトグラフ ィ法等)などを経て単一物質とした後、加水分解反応などの化学的な処理によ り光学活性な試薬部位を切り離すことにより光学異性体を得る方法。例えば、 本発明化合物が分子内にヒドロキシまたは 1, 2級ァミノを有する場合、 該化 '合物と光学活性な有機酸 (例えば、 MTPA 〔0!—メトキシ— α _ (トリフルォロ メチル)フエニル酢酸〕 、 (一)ーメントキシ酢酸等)などとを縮合反応に付す ことにより、 それぞれエステル体またはアミド体のジァステレオマーを得る ことができる。 一方、 本発明化合物がカルボン酸基を有する場合、 該化合物 と光学活性アミンまたはアルコール試薬とを縮合反応に付すことにより、 そ れぞれアミド体またはエステル体のジァステレオマーが得られる。 分離され たジァステレオマーは、 酸加水分解あるいは塩基性加水分解反応に付すこと
により、 元の化合物の光学異性体に変換される。 化合物 (1,) または (1 ") のプロドラッグは、 生体内における生理条件下 で酵素や胃酸等による反応により化合物 (1,) または(Γ') に変換する化合 物、 すなわち酵素的に酸化、 還元、 加水分解等を起こして化合物 (1,) また は( I ")に変化する化合物、胃酸等により加水分解などを起こして化合物( I,) または (1 ") に変化する化合物をいう。 化合物 (1,) または (1 ") のプロ ドラッグとしては、 化合物 (1,) または (1 ") のァミノ基がァシル化、 アル キル化、 りん酸ィ匕された化合物 [例、 化合物 (1,) または (1 ") のァミノ基 がエイコサノィル化、 ァラニル化、 ペンチルァミノカルポニル化、 ( 5—メ チル— 2—ォキソ一 1, 3一ジォキソレン一 4一ィル) メトキシカルポニル ィ匕、 テトラヒドロフラニル化、 ピロリジルメチル化、 ビバロイルォキシメチ ル化、 t e r t _ブチル化された化合物など] ;化合物 (1,) または (1 ") の水酸基がァシル化、 アルキル化、 りん酸化、 ほう酸化された化合物 (例、 化合物 (1,) または (1 ") の水酸基がァセチル化、 パルミトイル化、 プロパ. ノィル化、 ビバロイル化、 サクシ二ル化、 フマリル化、 ァラニル化、 ジメチ ルアミノメチルカルポニル化された化合物など) ;化合物(1 ')または(1 ") の力ルポキシル基がエステル化、 アミド化された化合物 [例、 化合物 (1,) または (1 ") の力ルポキシル基がェチルエステル化、 フエニルエステル化、 カルポキシメチルエステル化、 ジメチルァミノメチルエステル化、 ピパロイ ルォキシメチルエステル化、 エトキシカルポニルォキシェチルエステル化、 フタリジルエステル化、 (5—メチル— 2—ォキソ— 1, 3一ジォキソレン 一 4一ィル) メチルエステル化、 シクロへキシルォキシ力ルポニルェチルェ ステル化、 メチルアミド化された化合物など] などが挙げられる。 これらの 化合物は自体公知の方法によって化合物 (1,) または(1 ") から製造するこ とができる。
また、 化合物 (1 ') または (1 ") のプロドラッグは、 広川書店 1 9 9 0年 刊 「医薬品の開発」 第 7巻分子設計 1 6 3頁から 1 9 8頁に記載されている ような、 生理的条件で化合物 (1,) または(Γ') に変化するものであっても
よい。
なお、 化合物 (I) 、 ( I "0 、 ( I "") および ( I '"") もプロドラッグと して用いてよい。 これらの化合物のプロドラッグとしては、前記化合物(1,) または (Γ') のプロドラッグと同様のものが挙げられる。 本発明化合物は、 以下に詳述する [製造法 1] ないし [製造法 10] 、 あ るいはこれに準ずる方法によって製造することができる。
なお、 原料化合物として用いられる化合物 (II) 、 化合物 (III) 、 化合物 (V) 、 化合物 (VI) 、 化合物 (Ila) 、 化合物 (lib) 、 化合物 (Ilia) 、 化 合物 (Illaa) 、 化合物 (Illab) 、 化合物 (Iliac) 、 化合物 (Illb) 、 化合 物 (IIIc) 、 化合物 (IVa) 、 化合物 (IVb) 、 化合物 (IVc) 、 化合物 (IVd) 、 化合物 (Va)、化合物 (Via)、化合物 (Vlaa)、化合物 (Vila)、化合物 (Vlld)、 化合物 (Vllg) 、 化合物 (Vllle) 、 化合物 (IXa) 、 化合物 (1 ) 、 化合物 (IXe) 、 化合物 (IXg) 、 化合物 (Xa) 、 化合物 (Xb) 、 化合物 (Xf) 、 化 合物 (Xla) 、 化合物 (ΧΠ) 、 化合物 (Xlg) は、 それぞれ塩として用いても よい。 このような塩としては、 前記した化合物 (I) などの塩として例示し たものが用いられる。 下記の [製造法 1] ないし [製造法 10] において、 アルキル化反応、 加 水分解反応、 アミノ化反応、 エステル化反応、 アミド化反応、 エステル化反 応、 エーテル化反応、 酸化反応、 還元反応などを行う場合、 これらの反応は、 自体公知の方法にしたがって行われる。 このような方法としては、 例えばォ —ガニック ファンクショナル グループ プレパレーションズ (ORGA N I C FUNCT I ONAL GROUP PREPARAT I ONS) 第 2版、アカデミックプレス社(ACADEMI C PRESS, INC. ) 1989年刊;コンプリへンシブ ·オーガニック · トランスフォーメ一ショ ン (Comprehensive Organic Transformations) VCH Publishers Inc. , 1989 年刊等に記載の方法などが挙げられる。 . '
[製造法 1 ]
式 (I ) において Xが—(CH 2) w 3 C0 (w 3は前記と同意義を示す) で ある化合物 (l a ) は、 例えば下記アミド化反応によって製造される- (アミド化反応)
( l a) ·'·....."
[式中の記号は前記と同意義を示す]
該 「アミド化反応」 には、 下記の 「脱水縮合剤を用いる方法」 と 「力ルポ キシの反応性誘導体を用いる方法」 が含まれる。 '
i) 脱水縮合剤を用いる方法
化合物(111)、 1ないし 5当量の化合物(11)、 および 1ないし 2当量の脱水 縮合剤を、 不活性溶媒中で反応させる。 必要に応じ、 1ないし 1. 5当量の 1一 ヒドロキシベンゾトリアゾール (H0BT)および(または)触媒量ないし 5当量の 塩基の共存下に反応を行ってもよい。
該「脱水縮合剤」 としては、 例えばジシクロへキシルカルポジイミド (DCC)、 1一ェチル—3— (3—ジメチルァミノプロピル)カルポジイミド 塩酸塩 (WSC) などが挙げられる。 なかでも WSCが好ましい。
「不活性溶媒」 としては、 例えば、 二トリル系溶媒 (好ましくはァセトニト リル)、 アミド系溶媒 (好ましくは DMF)、 ハロゲン化炭化水素系溶媒 (好まし くはジクロロメタン)、 エーテル系溶媒 (好ましくは THF)などが挙げられる。 これらは、 二種以上を適宜の割合で混合して用いてもよい。
「塩基」 としては、 例えば
1 ) 例えばアルカリ金属またはアルカリ土類金属の水素化物 (例、 水素化 リチウム、 水素化ナトリウム、 水素化カリウム、 水素化カルシウムなど) 、
アルカリ金属またはアルカリ土類金属のアミド類 (例、 リチウムアミド、 ナ
ラジド、 カリウムへキサメチルジシラジドなど) 、 アルカリ金属またはアル カリ土類金属の低級アルコキシド (例、 ナトリウムメトキシド、 ナトリウム エトキシド、 カリウム t e r t—ブトキシドなど) などの強塩基;
2 ) 例えば、 アルカリ金属またはアルカリ土類金属の水酸ィヒ物 (例、 水酸 化ナトリウム、 水酸化カリウム、 水酸化リチウム、 水酸化バリウムなど) 、 アルカリ金属またはアルカリ土類金属の炭酸塩 (例、 炭酸ナトリウム、 炭酸 カリウム、 炭酸セシウムなど) 、 アルカリ金属またはアルカリ土類金属の炭 酸水素塩 (例、 炭酸水素ナトリウム、 炭酸水素カリウムなど) などの無機塩
¾;あよひ
3 ) 例えば、 トリェチルァミン、 ジイソプロピルェチルァミン、 N—メチ ルモルホリン、 ジメチルァミノピリジン、 D B U ( 1 , 8—ジァザビシクロ 〔5 . 4 . 0〕 ゥンデス一 7—ェン) 、 D B N ( 1, 5—ジァザビシクロ 〔4. 3 . 0〕 ノン一 5—ェン) などのアミン類;例えばピリジン、 イミダゾール、 2 , 6—ルチジンなどの塩基性複素環化合物などの有機塩基などが挙げられ る。
上記した塩基のなかでも、 トリェチルァミン、 4—ジメチルァミノピリジン などが好ましい。
反応温度は、 通常室温 (0ないし 30°C、 以下同様) である。 反応時間は、 例えば 10ないし 24時間である。
i i)カルボキシの反応性誘導体を用いる方法
化合物(I I)の反応性誘導体と 1ないし 5当量 (好ましくは 1ないし 3当量) の化合物(I I I)とを、 不活性溶媒中で反応させる。 必要に応じ、 1ないし 10 当量、 好ましくは 1ないし 3当量の塩基の共存下に反応を行ってもよい。 化合物(I I)の 「反応性誘導体」 としては、 例えば酸八ライド (例、 酸クロリ ド、 酸プロミドなど)、 混合酸無水物 (例、 C アルキル一力ルボン酸、 C 6_ 1 0ァリ一ルーカルボン酸または Cト6アルキル炭酸との酸無水物など)、活性
エステル (例、 置換基を有していてもよいフエノ一ル、 1ーヒドロキシベンゾ トリァゾ一ルまたは N—ヒドロキシスクシンイミドとのエステルなど)などが 挙げられる。
該 「置換基を有していてもよいフエノール」 における 「置換基」 としては、 例えばハロゲン原子 (例、 フッ素、 塩素、 臭素、 ヨウ素など) 、 ニトロ、 ノ、 ロゲン化されていてもよい C卜 6アルキル、 ハロゲン化されていてもよい C 1 —6アルコキシが挙げられる。 置換基の数は、 例えば 1ないし 5個である。 該「ハロゲン化されていてもよい C 3_ _ 6アルキル」 、 「ハロゲン化されてい てもよい C i - 6アルコキシ」 としては、前記「置換基を有していてもよい環状 基」 における 「置換基」 として例示したものが用いられる。
「置換基を有していてもよいフエノール」 の具体例としては、 例えばフエ ノール、 ペン夕クロ口フエノール、 ペン夕フルオロフエノ一ル、 p—ニトロフ ェノールなどが挙げられる。反応性誘導体は、好ましくは酸ハライドである。
「不活性溶媒」 としては、 例えばエーテル系溶媒、 ハロゲン化炭化水素系 溶媒、 芳香族系溶媒、 二トリル系溶媒、 アミド系溶媒、 ケトン系溶媒、 スル ホキシド系溶媒、 水などが挙げられる。 これらは、 二種以上を適宜の割合で 混合して用いてもよい。 なかでも、 ァセトニトリル、 TH 、 ジクロロメ夕 ン、 クロ口ホルムなどが好ましい。
「塩基」 としては、 前記と同様のものが用いられる。 該塩基は、 好ましく は、 水素化ナトリゥム、 炭酸力リゥム、 炭酸ナトリゥム、 水酸化ナトリゥム、 水酸化カリウム、 炭酸水素ナトリウム、 炭酸水素カリウム、 トリェチルアミ ン、 ピリジンなどである。
反応温度は、 通常— 20°Cないし 50°C、 好ましくは室温である。 反応時間は、 通常 5分間ないし 40時間、 好ましくは Iないし 18時間である。 また、 式: R_ (CH 2) w 3— S0 2 0H (記号は前記と同意義を示す) で表され るスルホン酸、 または式: R— (CH 2) w 3— S00H (記号は前記と同意義を示す) で表されるスルフィン酸を、 上記「力ルポキシの反応性誘導体を用いる方法」 と同様の方法に付すことによって、 それぞれ式 (I ) において Xが—(CH 2) W
3S02—または一(CH2)w3S0_ (記号は前記と同意義を示す)である化合物を 製造することができる。 化合物 (II) は、 自体公知の方法あるいはそれに準じた方法により製造す ることができる。
化合物 (III) は、 自体公知の方法、 例えば、 ケミカル ファーマシューテ ィカル ブレティン(Chem. Pharm. Bull.), 36, 4377 (1988)、特表平 9-506885、 特表平 10- 504315等に記載の方法あるいはそれに準じた方法により製造する ことができる。
[式中、 Wはァミノ基の保護基を、 その他の記号は前記と同意義を示す]で表 される化合物を脱保護反応に付し、 wを除去することにより製造することがで きる。
Wで示されるァミノ基の保護基としては、 例えば、 ホルミル、 (^_6アルキ ルーカルポニル(例、 ァセチル、 プロピオニルなど)、 Cぃ6アルコキシ一カル ポニル (例、 メトキシカルポエル、 エトキシカルポニル、 tert—ブトキシカル ポニルなど)、 ベンゾィル、 C 7_1Qァラルキル—カルポニル (例、 ベンジルカ ルポニルなど)、 C 7_14ァラルキルォキシ一力ルポニル (例、 ベンジルォキシ カルボニル、 9—フルォレニルメトキシカルポニルなど)、 トリチル、 フタ口 ィル、 N,N—ジメチルアミノメチレン、 シリル (例、 トリメチルシリル、 トリ ェチルシリル、ジメチルフエニルシリル、 tert—プチルジメチルシリル、 tert 一プチルジェチルシリルなど)、 C 2— 6アルケニル (例、 1—ァリルなど)などが 用いられる。 これらの基は、 1ないし 3個のハロゲン原子 (例、 フッ素、 塩素、 臭素、 ヨウ素など)、 (^_6アルコキシ (例、 メトキシ、 エトキシ、 プロポキシ など)または二ト口などで置換されていてもよい。
脱保護反応は、 例えば化合物(Ilia)を、 鉱酸 (例えば塩酸、 硫酸、 臭化水素 酸、 ヨウ素酸、 過ヨウ素酸等)等の酸またはアルカリ金属水酸化物(例えば水
酸化ナトリウム、 水酸化カリウム、 水酸化リチウム等)等の塩基の水溶液中、 好ましくは 20°Cないし 140°Cに保持することにより行われる。 該酸または塩 基の使用量は、 化合物(Ilia)に対して通常 1ないし 100当量、 好ましくは 1- ないし 40当量である。酸または塩基の強さは、通常、 0.1規定ないし 18規定、 好ましくは 1規定ないし 12規定である。反応時間は、通常 0.5時間ないし 48 時間、 好ましくは 1時間ないし 24時間である。
また、 Wが t-ブトキシカルポニル基等の場合、脱保護反応は、化合物(Ilia) を有機酸 (例えばトリフルォロ酢酸、 ぎ酸、 酢酸、 メタンスルホン酸、 ベンゼ ンスルホン酸、 トリフルォロメタンスルホン酸等)に溶解し、 通常- 20°Cない し 200°C、好ましくは 0°Cないし 100°Cに保持することにより行うこともでき る。 該有機酸の使用量は、 化合物(Ilia)に対して 1ないし 100当量、 好まし くは 1ないし 40当量である。
脱保護反応は、 パラジウム、 パラジウム一炭素、 ラネ一ニッケル、 ラネ一 コバルト、 酸化白金等を触媒として、 例えばエタノール等のアルコール系溶 媒ゃ酢酸等の溶媒中で、 常圧あるいは必要に応じて加圧下に、 化合物(Ilia) を接触還元反応に付すことにより行うこともできる。 化合物(Ilia)は、 自体公知の方法あるいはそれに準じた方法により製造す ることができる。 例えば、 化合物(Ilia)のうち、 Yが C2_6アルケニレン [例 えば、 -CH=CH- (CH2) w4— (w 4は前記と同意義を示す) ] であ る化合物(Illaa)は、 例えば以下の [反応式 1一 1] にしたがって製造するこ とができる。
(IVa) (Va) o -R1 (ab)
W -N B [I A J— C-CH2- (C^ ,一 N、
R2
(Vila)
(Illaa)
[式中、 Lは脱離基を、 その他の記号は前記と同意義を示す]
工程 (a a) では、 化合物 (IVa) と化合物 (Va) との縮合反応によ り、 化合物 (V I a) を製造する。
Lで示される 「脱離基」 としては、 例えばハロゲン原子 (例、 塩素、 臭素、 ヨウ素など)、ハロゲン化されていてもよい Cェ アルキルスルホニルォキシ
(例、 メタンスルホニルォキシ、 ェ夕ンスルホニルォキシ、 トリフルォロメ タンスルホ二 ォキシなど) 、 置換基を有していてもよい C 6^。ァリールス ルホニルォキシ、 ヒドロキシなどが挙げられる。
該 「置換基を有していてもよい C 6^。ァリ一ルスルホニルォキシ」 におけ る 「置換基」 としては、 例えば八ロゲン原子 (例、 塩素、 臭素、 ヨウ素など) 、 ハロゲン化されていてもよい C i— 6アルキルまたは C _ 6アルコキシなどが挙 げられる。 置換基の数は、 例えば 1ないし 3個である。 「置換基を有してい てもよい C 6^ 0ァリ一ルスルホニルォキシ」 の具体例としては、 ベンゼンス ルホニルォキシ、 p一トルエンスルホニルォキシ、 1—ナフ夕レンスルホニ ルォキシ、 2—ナフ夕レンスルホニルォキシなどが挙げられる。
該 「脱離基」 は、 好ましくは、 ハロゲン原子 (例、 塩素、 臭素、 ヨウ素な ど) 、 メタンスルホニルォキシ、 トリフルォロメタンスルホニルォキシ、 P 一トルエンスルホニルォキシなどである。
本縮合反応は、 通常不活性溶媒中で行われる。
該 「不活性溶媒」 としては、 例えば、 アルコール系溶媒、 エーテル系溶媒、 ハロゲン化炭化水素系溶媒、 芳香族系溶媒、 二トリル系溶媒、 アミド系溶媒、 ケトン系溶媒、 スルホキシド系溶媒、 水などが挙げられる。 これらは、 二種 以上を適宜の割合で混合して用いてもよい。 なかでも、 ァセトニトリル、 N, N—ジメチルホルムアミド (D M F ) 、 アセトン、 ェタノ一ル、 ピリジンな どが好ましい。
化合物 (Va)の使用量は、 化合物(IVa)に対し、 1ないし 100当量である。 ま た、 化合物 (Va)を反応溶媒量用いてもよい。
反応温度は約一 2 0 °Cないし 2 0 0 °C、好ましくは室温ないし 100°Cである c 反応時間は、 例えば約 0. 5時間ないし 1日である。
本縮合反応は、 塩基の存在下に行ってもよい。 該塩基は、 好ましくは、 水 素化ナトリウム、 炭酸カリウム、 炭酸ナトリウム、 水酸化ナトリウム、 水酸 化カリウム、 炭酸水素ナトリウム、 炭酸水素カリウム、 トリェチルァミン、 ピリジンなどである。 塩基の使用量は、 化合物(IVa)に対し、 0. 1ないし 100 当量、 好ましくは 1ないし 10当量である。 化合物 (I V a ) は、 自体公知の方法あるいはそれに準じた方法により製 造することができる。 化合物 (I V a ) は、 例えば特開平 6— 166676等に記 載の方法あるいはそれに準じた方法により製造することができる。
また、 化合物 (V a ) は、 自体公知の方法あるいはそれに準じた方法によ り製造することができる。
工程 (a b ) では、 化合物 (V I a ) を還元反応に付すことにより、 化合 物 (V I I a) を製造する。
本還元反応は、 例えば水素化ホウ素ナトリウム、 水素化リチウムアルミ二 ゥム、 卜リエチルシラン等の還元剤を用いて行うことができる。
還元反応は、 例えば、 リダクション ウイズ コンプレックス メタル · ヒドリドズ (Reduction with Complex Metal Hydrides; 'Interscience, New York (1956)、 ケミカル ソサイエティー レビューズ (Chem. Soc. Rev.), 5, 23 (1976) 、 シンセシス(Synthesis), 633 (1974)、 ジャーナル ォプ ジ アメリカン ケミカル ソサイエティー(J. Am. Chem. Soc.) 91, 2967 (1969)、 ジャーナル ォブ ォ一ガニック ケミストリ一(J. Org. Chem.), 29, 121 (1964)、 ォ一ガニック リアクションズ (Org. Reactions), 1, 155 (1942)、 アンゲバンテ へミー(Angew. Chei. ) , U, 726 (1956)、 シ ンセシス(Synthesis), 633 (1974)、 ジャーナル ォブ ジ アメリカン ケ ミカル ソサイエティー(J. Am. Chem. Soc.) , 80, 2896 (195.8)、 オーガ二 ック リアクションズ (Org. Reactons), 4, 378 (1948)、 ジャーナル ォブ ジ アメリカン ケミカル ソサイエティ一(J. Am. Chem. Soc.) , 108, 3385 (1986)等に記載の方法あるいはそれに準じた方法等にしたがって行うことが できる。
工程 (a c) では、 化合物 (V II a) を脱水反応に付すことにより、 化合 物 (Illaa) を製造する。
本脱水反応は、 加熱条件下あるいは室温下に、 必要に応じ酸触媒 (例、 硫 酸、 リン酸、 硫酸水素カリウム、 p—トルエンスルホン酸、 三フッ化ホウ素 ェ一テル錯体、 ヨウ素など) を用いることによって行うことができる。 また、 脱水反 は、 塩化チォニル-ピリジン、 ォキシ塩化リン-ピリジンなどの活性 化剤を用いて行うこともできる。
脱水反応は、 例えばオーガニック シンセシス (Org. Synth.), 丄, 183
(1941)、 オーガニック シンセシス (Org. Synth.),'丄, 430 (1941)、 ォー ガニック シンセシス (Org. Synth.), HI, 204 (1955)、 オーガニック シ ンセシス (Org: Synth.), VI, 307 (1988)、シンセシス (Synthesis), , H59
(1980)、ジャーナル ォブ ジ アメリカン ケミカル ソサイエティー(J.
Am. Chem. Soc.) , 106, 6690 (1984)、 テトラへドロン レターズ
(Tetrahedron Lett.), 599 (1971) 等に記載の方法あるいはそれに準じた方 法にしたがって行うことができる。
また、 [反応式 1一 1] で用いられる化合物 (VI a) のうち、 w4が 1 である化合物 (V I a a) は、 例えば以下の [反応式 1一 2] に従い、 化合 物 (I Xa) 、 化合物 (Va) およびホルムアルデヒドをマンニッヒ反応に付 すことにより製造することができる。
[式中の記号は前記と同意義を示す]
工程 (ae) におけるマンニッヒ反応は、 例えばオーガニック リアクシ ヨンズ (Org. Reactons), 1_, 303 (1942) 、 テトラへドロン レ夕一ズ
(Tetrahedron Lett.), ]8, 1299 (1977) 等に記載の方法あるいはそれに準じ た方法にしたがって行うことができる。
化合物(I Xa) は、 自体公知の方法あるいはそれに準じた方法により製造 することができる。化合物(I X a)は、例えばジャーナル ォプ ケミカル ソサイエティー パーキン トランスダクシヨン 1 (J. Chem. Soc.,
Perkin Trans. 1), 2993 (1994)等に記載の方法あるいはそれに準じた方法に より製造することができる。 化合物 (V l a a) は、 以下の [反応式 1一 3] によっても製造すること ができる。
(ag) O /
W— N B I A■ -C-CHj-CH,— N
ヽ ノ
(Vlaa)
[式中、 R9は C アルキルを、 その記号は前記と同意義を示す]
R9で示される 「(^-6アルキル」 としては、 前記 R4で示される 「(^_6ァ Jレキル」 と同様のものが挙げられる。
すなわち、
工程 (a f) :化合物 (I Xa) と化合物 (Xa) との縮合反応、 および 工程 (ag) :化合物 (X I a) の還元反応を、 順次行うことにより、 化合 物 (V I a a) を製造することができる。
工程 (a f) は、 自体公知の縮合反応を用いて行うことができる。 縮合反 応は、 例えばジャーナル ォブ ヘテロサイクリック ケミストリ一 (J. Heterocyclic Chem.), 30, 23 (1993) 、 ヘテロサイクルス (Heterocycles)、 22, 195 (1984)等に記載の方法あるいはそれに準じた方法にしたがって行う ことができる。
化合物 (Xa) は、 自体公知の方法あるいはそれに準じた方法により製造 すること できる。
工程 (ag) は、 自体公知の還元反応 (例、 Pd/C等の遷移金属触媒を用い た接触還元反応、 Et3SiHなどの金属水素化物を用いた還元反応、 NaBH(0Ac)3 などの金属水素錯化合物を用いた還元反応等) を用いて行うことができる。 還元反応は、 例えばジャーナル ォブ ジ アメリカン ケミカル ソサイ エティ一(J. Am. Chem. Soc), 76, 5014 (1954)、 ブレティン ォブ ジ ケミカル ソサイエティー ォブ ジャパン (Bull. Chem. Soc. Jpn.), 45, 3506 (197.2) 等に記載の方法あるいはそれに準じた方法にしたがって行うこ とができる。 化合物 (Ilia) のうち、 Yが— 0_ (CH2) w2— (w2は前記と同意義 を示す) である化合物 (Illab) は、 以下の [反応式 2— 1] に従い、 化合物 (I Xb) と化合物 (Xb) とを、 例えば光延 (Mitsunobu)反応の条件下、 脱 水反応に付すことにより製造することができる。
(lllab)
[式中の記号は前記と同意義を示す]
工程(b a)における脱水反応は、例えばシンセシス (Synthesis), 1 (1981)、 ブレティン ォブ ジ ケミカル ソサイエティ一 ォブ ジャパン (Bull. Chem. Soc. Jpn.), 49, 510 (1976) 等に記載の方法あるいはそれに準じた方 法にしたがつて行うことができる。
化合物(I Xb)は、 自体公知の方法あるいはそれに準じた方法により製造 することができる。
化合物 (Xb) は、 自体公知の方法あるいはそれに準じた方法により製造 することができる。 化合物 (Ilia) のうち、 Yがー C〇— (CH2) W7-CO- (W7は前記と 同意義を示す) である化合物 (Iliac) は、 以下の [反応式 2 _ 2] に従い、 化合物 (I Vd) と化合物 (Va) とを、 前述の 「アミド化反応」 に付すこと により合成することができる。 ,
(Iliac)
[式中の記号は前記と同意義を示す]
化合物 (IVd) は、 自体公知の方法あるいはそれに準じた方法により製造す ることができる。
[製造法 2 ]
式(I) において Xがー(CH2)w3C00(CH 2)w4— (記号は前記と同意義を 示す) である化合物 (l b) は、 例えば下記エステル化反応によって製造さ れる。
(エステル化反応)
·-、.
R-(CH2)W3— C00H + HO— (CH2)w4-N B || AJ-Y
(IVb)
[式中の記号は前記と同意義を示す]
本反応では、化合物(II)の反応性誘導体と 1ないし 5当量 (好ましくは 1な いし 3当量)の化合物(IVb)とを、 通常、 1ないし 10当量、 好ましくは 1ない し 3当量の塩基の共存下に、 不活性溶媒中で反応させる。
化合物(II)の 「反応性誘導体」 としては、 前記 [製造法 1] において例示 したものが用いられる。 なかでも、 酸ハライドが好ましい。
「不活性溶媒」 としては、 例えばエーテル系溶媒、 ハロゲン化炭化水素系 溶媒、 芳香族系溶媒、 二トリル系溶媒、 アミド系溶媒、 ケトン系溶媒、 スル ホキシド系溶媒などが挙げられる。 これらは、 二種以上を適宜の割合で混合 して用いてもよい。 なかでも、 ァセトニトリル、 ジクロロメ夕ン、 クロロホ ルムなどが好ましい。
「塩基」 としては、 前記 [製造法 1] において例示したものが用いられる。
該塩基は、 好ましくは、 永素化ナトリウム、 炭酸カリウム、 炭酸ナトリウム、 水酸化ナトリウム、 水酸化カリウム、 炭酸水素ナトリウム、 炭酸水素力リウ ム、 トリェチルァミン、 ピリジンなどである。
反応温度は、 通常一 20°Cないし 50°C、 好ましくは室温である。 反応時間は、 通常 5分間ないし 40時間、 好ましくは 1ないし 18時間である。
[製造法 3 ]
式(I ) において Xがー(CH 2) w l 0 (CH 2) w 2— (記号は前記と同意義を示 す) である化合物 (I c ) は、 例えば下記エーテル化反応によって製造され る。
(エーテル化反応)
[式中の記号は前記と同意義を示す]
本反応では、 化合物.(IVc) と約 1ないし 5当量 (好ましくは 1ないし 2当 量) の化合物 (V)とを、 塩基の共存下、 不活性溶媒中で反応させる。
「塩基」 としては、 [製造法 1 ] において例示したものが用いられる。 該 塩基は、 好ましくは、 炭酸カリウム、 炭酸水素ナトリウム、 トリェチルアミ ン、 N—メチルモルホリン、 ピリジンなどである。
塩基の使用量は、 通常化合物 (V) に対して約 1ないし 5当量である。
「不活性溶媒」 としては、 例えば、 アルコール系溶媒、 エーテル系溶媒、 八ロゲン化炭化水素系溶媒、 芳香族系溶媒、 二トリル系溶媒、 アミド系溶媒、 ケトン系溶媒、 スルホキシド系溶媒、 水などが挙げられる。 これらは、 二種 以上を適宜の割合で混合して用いてもよい。 なかでも、 ァセトニトリル、 N,
N—ジメチルホルムアミド (DMF) 、 アセトン、 エタノール、 ピリジンな どが好ましい。
反応温度は約— 20 °Cないし 100 °C、 好ましくは室温ないし 80 °Cであ る。 反応時間は、 例えば約 0. 5時間ないし 1日である。 化合物 (V)において Lで示される脱離基がヒドロキシである場合、 化合物 (I c) は、 光延反応を用いて製造することができる。
該光延反応は、 化合物 (V)と 0.5ないし 5当量 (好ましくは 1ないし 1.5当 量)の化合物(IVc)とを、 0.5ないし 5当量 (好ましくは 1ないし 1.5当量)のァ セチルジカルボン酸ェチルの共存下に、 不活性溶媒中で反応させることによ つて行われる。
不活性溶媒としては、 例えばエーテル系溶媒、 ハロゲン化炭化水素系溶媒、 芳香族系溶媒、 二トリル系溶媒、 アミド系溶媒、 ケトン系溶媒、 スルホキシ ド系溶媒などが挙げられる。 これらは、 二種以上を適宜の割合で混合して用 いてもよい。 なかでも、 ァセトニトリル、 ジクロロメタン、 クロ口ホルムな どが好ましい。
反応温度は、 通常— 20°Cないし 50°C、 好ましくは室温である。 反応時間は、 通常 5分間ないし 40時間、 好ましくは 1ないし 18時間である。
化合物(IVc)は、 自体公知の方法により製造することができる。
[製造法 4]
式(I) において Xがー(CH2)w3NR8aC0(CH2)w4— (記号は前記と同意 義を示す) である化合物 (I d) は、 例えば下記アミド化反応によって製造 される。 .
(アミド化反応)
8 a
R- (CH2)W3— NH + H00C-(CH2)W4-N B }| A"J-Y— :
(VI) (VI Id)
[式中、 R8aは水素原子またはハロゲン化されていてもよい C ^6アルキルを、 その他の記号は前記と同意義を示す]
R8aで示される 「ハロゲン化されていてもよい C ^6アルキル」 としては、 前記 R8として例示したものが挙げられる。
本反応は、 前記した [製造法 1] に準じて行われる。
化合物 (V I )は、 自体公知の方法により製造することができる。
化合物 (VI Id)は、 自体公知の方法により製造することができる。 [製造法 5]
式(I) にぉぃて がー((¾2 5?«¾0^83(012 2) w6 (式中の記号は前 記と同意義を示す) である化合物 (I e) は、 例えば下記ウレァ化反応によ つて製造される。
(ゥレア化反応)
、8 a -(CH ,,2)wW55—— N NHH,2 + — (CH2)W6 -N B f AJ-Y— I N:
(VI l ie) (IXe)
,8 a
R-(CH2)W5—— HCON— (CH2)w6-N B A- -Y— N:
(le)
[式中の記号は前記と同意義を示す]
本反応では、化合物(IXe)と 1ないし 5当量 (好ましくは 1ないし 1.5当量) 化合物 (Vllle) とを、 塩基の共存下、 不活性溶媒中で反応させる。
「塩基」 としては、 前記 [製造法 1] において例示したものが用いられる。 該塩基は、 好ましくは、 炭酸カリウム、 炭酸ナトリウム、 水酸化ナトリウム、 水酸化カリウム、 炭酸水素ナトリウム、 炭酸水素カリウム、 トリェチルアミ ン、 ピリジンなどである。
「不活性溶媒」 としては、 例えば、 アルコール系溶媒、 ェ一テル系溶媒、 ハロゲン化炭化水素系溶媒、 芳香族系溶媒、 二トリル系溶媒、 アミド系溶媒、 ケトン系溶媒、 スルホキシド系溶媒、 水などが挙げられる。 これらは、 二種 以上を適宜の割合で混合して用いてもよい。 なかでも、 ァセトニトリル、 D MF、 アセトン、 エタノール、 ピリジンなどが好ましい。
反応温度は、通常約一 20 °Cないし 1ひ 0 °C、好ましくは室温ないし 80 °C である。 反応時間は、 例えば約 0.5時間ないし 1日である。
化合物 (Vllle)は、 自体公知の方法により製造することができる。
化合物(IXe)は、 自体公知の方法により製造することができる。
[製造法 6 ]
式 (I) において Rが置換基を有していてもよい環集合芳香族基 (Ar 2'
Ar 3) である化合物 (I f ) は、 例えば下記ァリールカップリング反応によ つて製造する-こともできる。
(ァリールカップリング反応)
[式中、 Ar 2および Ar 3は、'それぞれ置換基を有していてもよい単環式芳香 族基または縮合芳香族基を; L 1はヒドロキシあるいは C 6アルキルを; L 2 はハロゲン (好ましくは塩素、 臭素)あるいはトリフルォロメタンスルホニル ォキシを;その他の記号は前記と同意義を示す]
Ar 2および Ar 3で示される 「置換基を有していてもよい単環式芳香族基ま たは縮合芳香族基」 において、 「置換基」 、 「単環式芳香族基」 、 「縮合芳 香族基」 としては、 前記 Rまたは Ar 1として例示したものが用いられる。 と りわけ、 Ar 2および Ar 3が、 ともに置換基を有していてもよいフエニルであ り、 Ar 2— Ar 3が置換基を有していてもよいピフエ二リルである場合が好まし い。
ァリールカップリング反応は、 自体公知の方法、 例えば、 ァクタ ケミカ スカンジナビア (Acta. Chemica Scandinavia) , 2 2 1— 2 3 0頁、 1 9 9 3年等に記載の方法、あるいはこれに準ずる方法に従って行うことができる。 本反応では、 化合物 (X f) と 1ないし 3当量 (好ましくは 1ないし 1. 5当 量)の化合物 (ΧΠ)とを、 塩基および遷移金属触媒の存在下、 不活性溶媒中で 反応させる。
該 「塩基」 としては、 前記 [製造法 1 ] において例示したものが用いられ る。 該塩基は、 好ましくは、 炭酸ナトリウム、 炭酸水素ナトリウムなどであ る。
「塩基」 の使用量は、 例えば化合物 (Xlf) に対して、 約 1ないし 10当量 である。 .
「遷移金属触媒」 としては、 例えば、 パラジウム触媒、 ニッケル触媒など が挙げられる。 該 「パラジウム触媒」 としては、 例えば、 テトラキス (トリ フエニルホスフィン) パラジウム (0) 、 酢酸パラジウム、 ビス (トリフエ ニルホスフィン) パラジウム (I I) クロリド、 パラジウム—炭素などが挙 げられる。 該 「ニッケル触媒」 としては、 例えば、 テトラキス (トリフエ二 ルホスフィン) ニッケル (0) などが挙げられる。
該 「遷移金属触媒」 の使用量は、 化合物 (ΧΠ) に対して、 約 0. 01ない し 1当量、 好ましくは約 0. 01ないし 0. 5当量である。
反応温度は、 室温ないし 150 °C、 好ましくは約 80 °Cないし 150 °Cで ある。 反応時間は、 例えば約 1ないし 48時間である。
該 「不活性溶媒」 としては、 例えば、 水、 アルコール系溶媒、 芳香族系溶 媒などが挙げられる。 これらは、 二種以上を適宜の割合で混合して用いても よい。 なかでも、 水、 エタノール、 トルエンなどの単独またはこれら二種以 上の混合溶媒が好ましい。
化合物 (Xf)は、 自体公知の方法により製造することができる。
化合物 a I f)は、 '自体公知の方法により製造することができる。 [製造法 7]
式 (I) において、 Yが C 2 6アルケニレン (例えば、 CH=CHCH2) である化合物 (I g) は、 以下の [反応式 3— 1] によって製造することがで きる。 ,
すなわち、
工程 (Aa) :化合物 ( I Xg) と化合物 (Xa) との縮合反応、 工程 (Ab) :化合物 (X I g) の還元反応、 および
工程 (Ac) :化合物 (V I I g) の脱水反応を順次行うことにより、 化合物
(I g) を製造することができる。
(ixg) (Xa)
Ar— x—
(xig)
Ar—— x —
(VHg)
Ar
(ig)
[式中の記号は前記と同意義を示す]
工程 (Aa) における縮合反応は、 例えば、 前記工程 (a f) と同様にし て行うことができる。
工程 (Ab) における還元反応は、 自体公知の方法 (例えば、 Pd/C等の遷 移金属触媒を用いた接触還元反応、 Et3SiHなどの金属水素化物を用いた還元 反応、 NaBH4などの金属水素錯化合物をもちいた還元反応等) を用いて行う ことができる。
また、 本反応は、 2段階で行うこともでき、 例えば、 前述の工程 (ag) で述べた還元反応と同様の条件で二重結合を還元した後、 NaM 4などの金属 水素錯化合物を用いて力ルポ二ル基を還元してもよい。 .
工程 (Ac) における脱水反応は、 例えば、 前記工程 (a c) と同様にし て行うことができる。
化合物(1½)は、 自体公知の方法により製造することができる。
化合物 (I) は、以下の [製造法 8] に従い、化合物 (Ila) と化合物 (III) とを縮合反応に付すことによつても製造することができる。 該 「縮合反応」 は、 前述の工程 (a a) における縮合反応と同様にして行うことができる。
[製造法 8 ]
R— X— L + H : > (I)
(Ila)
[式中の記号は前記と同意義を示す]
化合物 (Ila) は、 自体公知の方法あるいはそれに準じた方法により製造す ることができる。 化合物 (1') は、 例えば以下の [製造法 9] に従い、 化合物 (lib) と化 合物(Illb) とを縮合反応に付すことによって製造することができる。該「縮 合反応」 は、 前述の工程 (a a) における縮合反応と同様にして行うことが できる。
[式中の記号は前記と同意義を示す]
化合物 (lib) は、 自体公知の方法あるいはそれに準じた方法により製造す ることができる。
化合物 (Illb) は、 前記化合物 (III) と同様にして製造することができる。 化合物 (1") は、 例えば以下の [製造法 10] に従い、 化合物 (Ila) と 化合物 (IIIc) とを縮合反応に付すことによって製造することができる。 該
「縮合反応」 は、 前述の: ή程 (a a) における縮合反応と同様にして行うこ とができる。
[製造法 10 ]
R X一 L +
( Ha )
( III c)
[式中の記号は前記と同意義を示す]
化合物 (I I Ic) は、 前記化合物 (I I I) と同様にして製造することができる。 前記 「アルコール系溶媒」 としては、 例えば、 メタノール、 エタノール、 ィソプロパノ一ル、 t er t—ブ夕ノ一ルなどが用いられる。
前記 「エーテル系溶媒」 としては、 例えば、 ジェテルエ一テル、 テトラヒ ドロフラン(THF)、 1, 4一ジォキサン、 1,2—ジメトキシェタンなどが用いられ る。
前記 「ハロゲン化炭化水素系溶媒」 としては、 例えば、 ジクロロメタン、 クロ口ホルム、 1, 2—ジクロロエタン、 四塩化炭素などが用いられる。
前記 「芳香族系溶媒」 としては、 例えば、 ベンゼン、 トルエン、 キシレン、 ピリジンなどが用いられる。
前記 「炭化水素系溶媒」 としては、 例えば、 へキサン、 ペンタン、 シクロ へキサンなどが用いられる。
前記「アミド系溶媒」 としては、例えば、 Ν, Ν—ジメチルホルムアミド(DMF)、 Ν, Ν—ジメチルァセトアミド、 Ν—メチルピロリドンなどが用いられる。
前記 「ケトン系溶媒」 としては、 例えば、 アセトン、 メチルェチルケトン などが用いられる。
前記「スルホキシド系溶媒」としては、例えば、ジメチルスルホキシド(DMS0) などが用いられる。
前記 「二トリル系溶媒」 としては、 例えば、 ァセトニトリル、 プロピオ二 トリルなどが用いられる。 かくして得られた本発明化合物において、 分子内の官能基は、 自体公知の 化学反応を組み合わせることにより目的の官能基に変換することもできる。 該化学反応の例としては、 酸化反応、 還元反応、 アルキル化反応、 加水分解
反応、 アミノ化反応、 エステル化反応、 ァリールカップリング反応、 脱保護 反応などが挙げられる。 前記の各反応において、 原料化合物が置換基としてァミノ、 力ルポキシ、 'ヒドロキシ、 力ルポニルを有する場合、 これらの基にペプチド化学などで一 般的に用いられるような保護基が導入されていてもよく、 反応後に必要に応 じて保護基を除去することにより目的化合物を得ることができる。
ァミノの保護基としては、 前記 Wとして例示したアミノ基の保護基が用い られる。
力ルポキシの保護基としては、 例えば、 C卜6アルキル (例、 メチル、 ェチ ル、 プロピル、 イソプロピル、 プチル、 tert—ブチルなど)、 C 7— ァラルキ ル (例、 ベンジルなど)、 フエニル、 トリチル、 シリル (例、 トリメチルシリル、 トリェチルシリル、 ジメチルフエニルシリル、 tert—プチルジメチルシリル、 tert—プチルジェチルシリルなど)、 C 2— 6アルケニル (例、 1—ァリルなど)な どが用いられる。 これらの基は、 1ないし 3個のハロゲン原子 (例、 フッ素、 塩素、 臭素、 ヨウ素など)、 (^_6アルコキシ (例、 メトキシ、 エトキシ、 プロ ポキシなど)またはニトロなどで置換されていてもよい。
ヒドロキシの保護基としては、 例えば、 (^_6アルキル (例、 メチル、 ェチ ル、 プロピル、 イソプロピル、 プチル、 tert—ブチルなど)、 フエニル、 トリ チル、 C 7_i。ァラルキル (例、 ベンジルなど)、 ホルミル、 C 6アルキル一力 ルポニル (例、 ァセチル、 プロピオニルなど)、 ベンゾィル、 C 7_10ァラルキ ルーカルポニル (例、 ベンジルカルポニルなど)、 2—テトラヒドロピラニル、 2—テトラヒドロフラニル、 シリル (例、 トリメチルシリル、 トリェチルシリ ル、 ジメチルフエニルシリル、 tert—プチルジメチルシリル、 tert—ブチル ジェチルシリルなど)、 C 2_6アルケニル (例、 1ーァリルなど)などが用いられ る。 これらの基は、 1ないし 3個のハロゲン原子 (例、 フッ素、 塩素、 臭素、 ヨウ素など)、 C ^6アルキル (例、 メチル、 ェチル、 n—プロピルなど)、 Cト 6アルコキシ (例、 メトキシ、 エトキシ、 プロポキシなど)またはニトロなどで 置換されていてもよい。
カルボニルの保護基としては、 例えば、 環状ァセ夕一ル (例、 1,3—ジォキ サンなど)、 非環状ァセ夕一ル (例、 ジー C卜6アルキルァセタールなど)など が用いられる。
上記した保護基の除去方法は、 自体公知の方法、 例えば、 プロテクティブ グループス イン オーガニック シンセシス(Protect ive Groups in Organic Synthes i s) , John Wi ley and Sons 刊(198Q)に記載の方法などに準じて行う ことができる。 例えば、 酸、 塩基、 紫外光、 ヒドラジン、 フエニルヒドラジ ン、 N—メチルジチォ力ルバミン酸ナトリウム、 テトラプチルアンモニゥムフ ルオリド、 酢酸パラジウム、 トリアルキルシリル八ライド(例えば、 トリメチ ルシリルョージド、 トリメチルシリルプロミドなど)などを使用する方法、 還 元法などが用いられる。 本発明化合物は、 公知の手段、 例えば、 溶媒抽出、 液性変換、 転溶、 晶出、 再結晶、 クロマトグラフィーなどによって単離精製することができる。 また、 本発明化合物の原料化合物またはその塩は、 前記と同様の公知の手段などに よつて単離精製することができるが、 単離することなくそのまま反応混合物 として次の工程の原料として供されてもよい。 . 本発明化合物は、優れた MCH受容体拮抗作用を有するため、 MCHに起因する 疾患の予防'治療剤として有用である。 また、 本発明化合物は、 毒性も低く、 経口吸収性および脳内移行性に優れている。
したがって、 本発明化合物を含有するメラニン凝集ホルモン拮抗剤は、 哺 乳動物 (例えば、 ラット、 マウス、 モルモ,ット、 ゥサギ、 ヒッジ、 ゥマ、 ブ夕、 ゥシ、サル、 ヒトなど)に対し、 MCHに起因する疾患の予防'治療剤などとして 安全に投与される。
ここで、 MCHに起因する疾患としては、 例えば肥満症 [例、 悪性肥満細胞症 Uiial ig腿 t mas tocytos is)、 夕因性肥満 exogenous obes i ty) , 過インシュ リン性肥満症(hyperinsul inar obes i ty).、 過血漿性肥満 (hyperpl asmic obes i ty) , 下垂体性肥満 (hypophyseal adipos i ty) , 減血漿性肥満症
(hypoplasmic obesity), 甲状腺機能低下肥満症 (hypothyroid obesity), 視 床下部性肥満(hypothalamic obesity), 症候性肥満症(symptomaUc obesity), 小児肥満 (infantile obesity), 上半身肥満(upper body obesity), 食事性 ' 肥満症 (alimentary obesity), 性機能低下性肥満 (hypogonadal obesity), 全身性肥満細胞症(systemic mastocytosis), 単純性肥満(simple obesity), 中心性肥満(central obesity)など] 、 摂食亢進症 (hyperphagia)、 情動障害、 性機能障害などが挙げられる。 ' '
本発明化合物は、 糖尿病、 糖尿病合併症 (例、 糖尿病性網膜症、 糖尿病性神 経症、 糖尿病性腎症など)、 動脈硬化症、 膝関節炎などの生活習慣病の予防- 治療薬としても有用である。
さらに、 本発明化合物は、 摂食抑制薬としても有用である。
本発明の MCH拮抗剤および医薬組成物は、 食事療法 (例、糖尿病の食事療法 など)、 運動療法と併用することもできる。 本発明の MCH拮抗剤および医薬組成物は、 それぞれ本発明化合物を、 その ままあるいは薬理学的に許容される担体とともに、 自体公知の手段に従って 製剤化することによって製造される。
ここで、 薬理学的に許容される担体としては、 製剤素材として慣用の各種 有機あるいは無機担体物質、 例えば、 固形製剤における賦形剤、 滑沢剤、 結 合剤、 崩壊剤;液状製剤における溶剤、 溶解補助剤、 懸濁化剤、 等張化剤、 緩衝剤、 無痛化剤などが挙げられる。 また、 製剤化の際に、 必要に応じて、 防腐剤、 抗酸化剤、 着色剤、 甘味剤、 吸着剤、 湿潤'剤などの添加物を用いる こともできる。
賦形剤としては、 例えば、 乳糖、 白糖、 D—マンニトール、 デンプン、 コー ンス夕一チ、 結晶セルロース、 軽質無水ケィ酸などが挙げられる。
滑沢剤としては、 例えば、 ステアリン酸マグネシウム、 ステアリン酸カル シゥム、 タルク、 コロイドシリカなどが挙げられる。
結合剤としては、 例えば、 結晶セルロース、 白糖、 D—マンニトール、 デキ ストリン、 ヒドロキシプロピルセルロース、 ヒドロキシプロピルメチルセル
ロース、 ポリビニルピロリドン、 デンプン、 ショ糖、 ゼラチン、 メチルセル ロース、 カルボキシメチルセルロースナトリゥムなどが挙げられる。
' 崩壊剤としては、 例えば、 デンプン、 カルポキシメチルセルロース、 カル ポキシメチルセルロースカルシウム、 クロスカルメロースナトリウム、 カル ポキシメチルスターチナトリウム、 低置換度ヒドロキシプロピルセルロース (L - H P C ) などが挙げられる。
溶剤としては、 例えば、 注射用水、 アルコール、 プロピレングリコール、 マクロゴール、 ゴマ油、 トウモロコシ油などが挙げられる。
溶解補助剤としては、 例えば、 ポリエチレングリコール、 プロピレンダリ コール、 D—マンニ! ^一ル、 安息香酸ベンジル、 エタノール、 トリスアミノメ タン、 コレステロール、 トリエタノールァミン、 炭酸ナトリウム、 クェン酸 ナ卜リゥムなどが挙げられる。
懸濁化剤としては、 例えば、 ステアリルトリエタノールァミン、 ラウリル 硫酸ナトリウム、 ラウリルアミノプロピオン酸、 レシチン、 塩化ベンザルコ 二ゥム、 塩化べンゼトニゥム、 モノステアリン酸グリセリンなどの界面活性 剤;例えばポリビニルアルコール、 ポリビニルピロリドン、 カルポキシメチ ルセルロースナトリウム、 メチルセルロース、 ヒドロキシメチルセルロース、 ヒドロキシェチルセルロース、 ヒドロキシプロピルセルロースなどの親水性 高分子などが挙げられる。
等張化剤としては、 例えば、 ブドウ糖、 D—ソルビトール、 塩ィ匕ナトリウム、 グリセリン、 D—マンニトールなどが挙げられる。
緩衝剤としては、 例えば、 リン酸塩、 酢酸塩、 炭酸塩、 クェン酸塩などの 緩衝液などが挙げられる。
無痛化剤としては、 例えば、 ベンジルアルコールなどが挙げられる。
防腐剤としては、 例えば、 パラォキシ安息香酸エステル類、 クロロブタノ —ル、 ベンジルアルコール、 フエネチルアルコール、 デヒドロ酢酸、 ソルビ ン酸などが挙げられる。
抗酸化剤としては、 例えば、 亜硫酸塩、 ァスコルビン酸などが挙げられる。
本発明の MCH拮抗剤および医薬組成物の剤型としては、 例えば、 錠剤 (糖衣 錠、 フィルムコ一ティング錠を含む)、 散剤、 顆粒剤、 カプセル剤(ソフト力 プセルを含む)、 液剤などの経口剤;注射剤 (例、 皮下注射剤、 静脈内注射剤、 筋肉内注射剤、 腹腔内注射剤など) 、 外用剤 (例、 経鼻投与製剤、 経皮製剤、 軟膏剤など) 、 坐剤 (例、 直腸坐剤、 膣坐剤など) 、 徐放剤 (例、 徐放性マ イク口カプセルなど) 、 ペレット、 点滴剤などの非経口剤などとして、 経口 的または非経口的 (例、 局所、 直腸、 静脈投与等)に安全に投与することがで きる。
本発明の MCH拮抗剤中の本発明化合物の含有量、 および本発明の医薬組成 物中の本発明化合物の含有量は、 例えば、 それぞれ MCH拮抗剤または医薬組 成物全体の約 0. 1ないし 100重量%である。 .
本発明の MCH拮抗剤および医薬組成物の投与量は、 投与対象、 投与ルート、 疾患などにより適宜選択される。
例えば、 本発明の MCH拮抗剤または医薬組成物を、 肥満症の成人患者 (体重 約 60kg)に経口投与する場合の 1日当たりの投与量は、それぞれ有効成分であ る本発明化合物として、約 0. 1ないし約 500mg、好ましくは約 1ないし約 100mg、 さらに好ましくは約 5ないし約 l OOmgであり、 この量を 1日 1ないし数回に 分けて投与することができる。 本発明の MCH拮抗剤および医薬組成物は、 例えば 「肥満症の治療効果の増 強」 、 「MCH拮抗剤の使用量の低減」 などを目的として、 本発明の MCH拮抗剤 および医薬組成物に悪影響を及ぼさない併用用薬剤を用いることができる。 このような併用用薬剤としては、 例えば 「糖尿病治療薬」 、 「糖尿病合併症 治療薬」 、 '「MCH拮抗剤以外の抗肥満薬」 、 ' 「高血圧治療薬」 、 「高脂血症治 療薬」 、 「関節炎治療'薬」 、 「抗不安薬」 、 「抗うつ薬」 などが挙げられる。 これらの併用用薬剤は、 2種以上を適宜の割合で組合わせて用いてもよい。 上記 「糖尿病治療薬」 としては、 例えばインスリン抵抗性改善薬、 インス リン分泌促進薬、 ビグアナイド剤、 インスリン、 一ダルコシダ一ゼ阻害薬、 i3 3アドレナリン受容体作動薬などが挙げられる。
ィンスリン抵抗性改善薬としては、例えばピオダリ夕ゾンまたはその塩(好 ましくは塩酸塩) 、 トロダリ夕ゾン、 ロシグリタゾンまたはその塩 (好まし くはマレイン酸塩) 、 JTT—501、 G I— 262570, MCC— 55 5、 YM— 440、 DRF - 2593、 BM— 13— 1258、 KRP- 2 97、 R— 1 19702などが挙げられる。
インスリン分泌促進薬としては、例えばスルフォニル尿素剤が挙げられる。 該スルフォニル尿素剤の具体例としては、 例えばトルプタミド、 クロルプロ パミド、 トラザミド、 ァセトへキサミド、 グリクロビラミドおよびそのアン モニゥム塩、 ダリベンクラミド、 ダリクラジド、 グリメピリドなどが挙げら れる。
上記以外にも、 インスリン分泌促進剤としては、 例えばレパグリニド、 ナ テグリニド、 ミチグリニド (KAD— 1229) 、 J TT— 608などが挙 げられる。
ビグアナイド剤としては、 例えばメトホルミン、 ブホルミン、 フェンホル ミンなどが挙げられる。
インスリンとしては、 例えばゥシ, ブ夕の滕臓から抽出された動物インス リン;ブタの滕臓から抽出されたインスリンから酵素的に合成された半合成 ヒトインスリン;大腸菌, ィ一ストを用い遺伝子工学的に合成したヒトイン スリンなどが挙げられる。 インスリンとしては、 0. 45から 0. 9 (wZ w) %の亜鉛を含むインスリン亜鉛;塩化亜鉛, 硫酸プロ夕ミンおよびイン スリンから製造されるプロ夕ミンインスリン亜鉛なども用いられる。さらに、 インスリンは、 そのフラグメントあるいは誘導体 (例、 INS-1など) であって もよい。
なお、 インスリンには、 超速効型、 速効型、 二相型、 中間型、 持続型など 種々のものが含まれるが、 これらは患者の病態により適宜選択できる。
一ダルコシダ一ゼ阻害薬としては、 例えばァカルボ一ス、 ポグリポース、 ミグリトール、 エミグリテ一トなどが挙げられる。
|33アドレナリン受容体作動薬としては、 例えば AJ— 9677、 BMS 一 196085、 SB— 226552、 AZ40140などが挙げられる。
上記以外にも、 「糖尿病治療薬」 としては、 例えばェルゴセット、 プラム リン夕イド、 レプチン、 BAY- 27- 9955などが挙げられる。
上記「糖尿病合併症治療薬」 としては、 例えばアルドース還元酵素阻害薬、 グリケーション阻害薬、 プロティンキナーゼ C阻害薬などが挙げられる。
ルドース還元酵素阻害剤としては、 例えばトルレスタツト;ェパルレス タツ卜;イミレスタツト;ゼナレスタツト; S N K - 8 6 0 ;ゾポルレス夕 ット; A R 1— 5 0 9 ; A S— 3 2 0 1などが挙げられる。
グリケーション阻害薬としては、 例えばピマゲジンなどが挙げられる。 プロテインキナ一ゼ C阻害薬としては、 例えば NGF、 LY- 333531などが挙げ られる。 - '
上記以外にも、 「糖尿病合併症治療薬」 としては、 例えばアルプロス夕ジ ル、 塩酸チアプリド、 シロスタゾール、 塩酸メキシレチン、 ィコサベント弊 ェチル、 メマンチン (memant ine) 、 ピマゲドリン (pimagedl ine; ALT-711) などが挙げられる。
上記.「MCH拮抗剤以外の抗肥満薬」 としては、 例えばリパーゼ阻害薬、 食欲 抑制薬などが挙げられる。
リパーゼ阻害薬としては、 例えばオルリスタツトなどが挙げられる。
食欲抑制薬としては、 例えばマジンドール、 デクスフェンフラミン、 フル ォキセチン、 シブトラミン、 パイァミンなどが挙げられる。
上記以外にも、 「MCH拮抗剤以外の抗肥満薬」 としては、 例えばリブスタチ ンなどが挙げられる。
上記「高血圧治療薬」 としては、 例えばアンジォテンシン変換酵素阻害薬、 カルシウム拮抗薬、 カリウムチャンネル開口薬、 アンジォテンシン I I拮抗薬 などが挙げられる。
アンジォテンシン変換酵素阻害薬としては、 例えばカプトプリル、 ェナラ プリル、 ァラセプリル、 (塩酸) デラプリル、 リジノプリル、 イミダブリル、 べナゼプリル、 シラザプリル、 テモカプリル、 トランドラプリル、 (塩酸) マニジピンなどが挙げられる。
カルシウム拮抗薬としては、 例えば二フエジピン、 アムロジピン、 エホ二
ジピン、 二カルジピンなどが挙げられる。
カリウムチャンネル開口薬としては、 例えばレブクロマカリム、 L- 27152、 AL 0671、 ΝΠ5- 121などが挙げられる。
アンジォテンシン I I拮抗薬としては、 例えば口サルタン、 カンデサルタン シレキシチル、 バルサルタン、 ィルベサルタン、 CS- 866、 E4177などが挙げら れる。
上記 「高脂血症治療薬 (動脈硬化症治療薬) 」 としては、 例えば HM G— C o A還元酵素阻害薬、 フィブラ一ト系化合物などが挙げられる。
HM G— C o A還元酵素阻害薬としては、 例えばプラバス夕チン、 シンパ スタチン、 口パスタチン、 ァトルパスタチン、 フルバス夕チン、 リパンチル、 セリバス夕チン、 イタバス夕チン、 Z D— 4 5 2 2またはそれらの塩 (例、 ナトリウム塩など) などが挙げられる。
フイブラート系化合物としては、 例えばべザフイブラート、 クリノフイブ ラート、 クロフイブラート、 シンフイブラートなどが挙げられる。
上記 「関節炎治療薬」 としては、 例えばイブプロフェンなどが挙げられる。 上記 「抗不安薬」 としては、 例えばクロルジァゼポキシド、 ジァゼバム、 ォキサゾラム、 メダゼパム、 クロキサゾラム、 プロマゼパム、 ロラゼパム、 アルブラゾラム、 フルジァゼバムなどが挙げられる。
上記 「抗うつ薬」 としては、 例えば、 フルォキセチン、 フルポキサミン、 イミブラミン、 パロキセチン、 サ一トラリンなどが挙げられる。 前記した併用用薬剤の投与時期は限定されず、 MCH拮抗剤または医薬組成物 と併用用薬剤とを、 投与対象に対し、 同時に投与してもよいし、 時間差をお いて投与してもよい。 併用用薬剤の投与量は、 臨床上用いられている投与量 に準ずればよく、 投与対象、 投与ルー卜、 疾患、 組み合わせ等により適宜選 択することができる。
併用用薬剤の投与形態は、特に限定されず、投与時に、 MCH拮抗剤または医 薬組成物と併用用薬剤とが組み合わされていればよい。 このような投与形態 としては、例えば、 1 ) MCH拮抗剤または医薬組成物と併用用薬剤とを同時に
製剤化して得られる単一の製剤の投与、 2) MCH拮抗剤または医薬組成物と併 用用薬剤とを別々に製剤化して得られる 2種の製剤の同一投与経路での同時 投与、 3) MCH拮抗剤または医薬組成物と併用用薬剤とを別々に製剤化して得 られる 2種の製剤の同一投与経路での時間差をおいての投与、 4) MCH拮抗剤 または医薬組成物と併用用薬剤とを別々に製剤化して得られる 2種の製剤の 異なる投与経路での同時投与、 5) MCH拮抗剤または医薬組成物と併用用薬剤 とを別々に製剤化して得られる?種の製剤の異なる投与経路での時間差をお いての投与(例えば、 MCH拮抗剤または医薬組成物;併用用薬剤の順序での投 与、 あるいは逆の順序での投与) などが挙げられる。
MCH拮抗剤または医薬組成物と併用用薬剤との配合比は、投与対象、投与ル —ト、 疾患等により適宜選択することができる。 発明を実施するための暈良の形態
本発明は、 さらに以下の参考例、 実施例、 製剤例、 実験例によって詳しく 説明されるが、 これらは本発明を限定するものではなく、 また本発明の範囲 を逸脱しない範囲で変化させてもよい。
以下の参考例、 実施例中の 「室温」 は 0ないし 30°Cを示し、 有機層の乾 燥には無水硫酸マグネシウムまたは無水硫酸ナトリウムを用いた。 「%」 は 特記しない限り重量パーセントを意味する。 ' 赤外吸収スペクトルは、 フーリエ変換形赤外分光光度計を用い、 拡散反射 法で測定した。
FABMS (pos) は、 高速原子衝撃質量分析法 (Fast Atom Bombardment Mass Spectrometry) における (+ ) 法で測定した質量スペクトルである。
MS (APCI) および MS(ESI)は、それぞれ大気圧科学イオン化法(Atmospheric Pressure Chemical Ionization : APCI) あるいは電子衝撃イオン化法
(Electron Spray Ionization : ESI) により測定した質量スペクトルである。 • 本文中で用いられているその他の略号は下記の意味を示す。
s : シングレツ卜 (s i ng l e t)
d : ダブレツト (doub l e t)
t . : 卜リブレツト (t r i p l e t)
q : クァ レテット 、qu a r t e t)
m : マルチプレツト (mu 1 t i p 1 e t )
b r : ブロード (b r o ad)
J : カップリング定数 (c oup 1 i n g c on s t a n t ) H z : ヘルツ (He r t z)
CDC 13: 重クロ口ホルム
DMSO— d6:重ジメチルスルホキシド
THF : テトラヒドロフラン
DMF : N, N—ジメチルホルムアミド
DMSO : ジメチルスルホキシド
WSCD : 1ーェチルー 3— (3—ジメチルァミノプロピル) カル ポジイミド
WS C : 1ーェチルー 3— (3—ジメチルァミノプロピル) カルボ ジィミド 塩酸塩
XH-NMR :プロトン核磁気共鳴
(通常フリー体を CD C 13中で測定した。 )
I R : 赤外吸収スぺクトル
Me : メチル
E t : ェチル
HOB t : 1—ヒドロキシー 1H—ベンゾトリアゾール
I P E:ジィソプロピルエーテル
DMAP : 4-ジメチルァミノピリジン 本明細書および図面において、塩基やアミノ酸などを略号で表示する場合、 I UP AC— I UB Co mm i s i on on B i o c h emi c a l Nome n c 1 a t u r eによる略号あるいは当該分野における慣用略号に 基づくものであり、 その例を下記する。 またアミノ酸に関し光学異性体があ り得る場合は、 特に明示しなければ L体を示すものとする。
DNA デォキシリポ核酸
cDNA 相補的デォキシリポ核酸
A アデニン
T チミン
G グァニン
C
RNA リポ核酸
mRNA メッセンジャーリポ核酸 dATP デォキシアデノシン三リン酸 dTTP デォキシチミジン三リン酸 dGTP デォキシグァノシン三リン酸 d CTP デォキシシチジン三リン酸 ATP アデノシン三リン酸
EDTA エチレンジァミン四酢酸 SDS ドデシル硫酸ナトリウム E I A ェンザィ
G 1 y グリシン
A 1 a ァラニン
Va 1 バリン
Le u ロイシン
I 1 e
S e r セリン
Th r スレオニン
Cy s
Me t メチォニン
G 1 u グルタミン酸
As p ァスパラギン酸
L y s リジン
A r g アルギニン
H i s ヒスチジン
Ph e フエ二ルァラニン
Ty r チロシン
T r p トリプトファン
P r o
A s n ァスパラギン .
G 1 n グルタミン
pG 1 ピログルタミン酸
M e メチル基
E t ェチル基
B u フ:チル基
Ph フエニル基
TC チアゾリジン— 4 (R) 一力ルポキサミド基 また、 本明細書中で繁用される置換基、 保護基および試薬を下記の記号で 表記する。
To s : ρ—トルエンスルホニル
CHO :ホルミル
B z 1 :ベンジル
C 12B z 1 : 2, 6—ジクロロべンジル
Bom :ベンジルォキシメチル
Z :ベンジルォキシカルポニル
C 1 -Z : 2—クロ口べンジルォキシカルポニル
B r -Z : 2—プロモベンジルォキシカルポニル
B 0 c : t一ブトキシカルポニル
DNP :ジニトロフエノール
T r t : トリチル
Bum : t一ブトキシメチル
Fmo c : N— 9 _フルォレニルメトキシカルポニル
HOOB t 3, 4—ジヒド g— 3—ヒドロキシ一 4—ォキソ一 1, 2, 3—べンゾ卜リアジン
HONB 1—ヒドロキシ— 5—ノルポルネン一 2, 3ージカル ポジイミド
DCC 本願明細書の配列表の配列番号は、 以下の配列を示す。
〔配列番号: 1〕 '
ラット SLC- 1をコ一ドする cDNAのスクリーニングに使用した合成 DNAを示す。 〔配列番号: 2〕
ラット SLC- 1を i—ドする cDNAのスクリーニングに使用した合成 DNAを示す。 〔配列番号: 3〕
ラット SLC - 1の全アミノ酸配列を示す。
〔配列番号: 4〕
5' 側に Sal I認識配列が付加され、 また 3' 側に Spe I認識配列が付加され たラッ卜 SLC-lcDNAの全塩基配列を示す。
〔配列番号: 5〕
ラット SLC- 1発現 CH0細胞の各クローンにおける SLC- lmRNAの発現量を測定 するために使用したリポプローブ (riboprobe) を示す。
〔配列番号: 6〕
ヒト SLC- 1をコ一ドする cDNAを取得するために使用した合成 DNAを示す。 〔配列番号: 7〕
ヒト SLC-1をコードする cDNAを 2本鎖にするために使用したプライマーを示 す。 ,
〔配列番号: 8〕
ヒト SLC- 1をコ一ドする cDNA全塩基配列を示す。
〔配列番号: 9〕
ヒト SLC-1の全アミノ酸配列を示す。
〔配列番号: 1 0〕
ヒト SLC- 1 (S)をコードする cDNAのスクリ一二ングに使用した合成 DNAを示す。 〔配列番号: 11〕
ヒト SLC- 1 (S)をコードする cDNAのスクリーニングに使用した合成 DNAを示す。 〔配列番号: 12〕
ヒト SLC- 1 (L)をコードする cDNAのスクリ一エングに使用した合成 DNAを示す。 〔配列番号: 13〕
ヒト SLC-1 (L)をコードする cDNAのスクリ一二ングに使用した合成 DNAを示す。 〔配列番号: 14〕
5' 側に Sal I認識配列が付加され、 また 3' 側に Spe I認識配列が付加され たヒト SLC-1 (S) cDNAの全塩基配列を示す。
〔配列番号: 15〕
5' 側に Sal I認識配列が付加され、 また 3' 側に Spe I認識配列が付加され たヒト SLC-1 (L) cDNAの全塩基配列を示す。
〔配列番号: 16〕
ヒト SLC- 1(S) 発現 CH0細胞およびヒト SLC- 1(L) 発現 CH0細胞の各クローン における SLC- lmRNAの発現量を測定するために使用したリポプローブ
(riboprobe を示す。
参考例 1一 6で得られた配列番号: 9で表される塩基配列をコ一ドする DNA を含むプラスミドによる形質転換体 Escherichia coli DH10B/phSLClL8は、 平成 11年 2月 1日から通商産業省工業技術院生命工学工業技術研究所 (N I B H) に寄託番号 F ERM BP— 6632として、 平成 11年 1月 21 日から財団法人 ·発酵研究所 (I FO) に寄託番号 I FO 16254とし て寄託されている。 実施例 ェチル 6 -(3-クロ口プロパノィル) -3, 4 -ジヒドロ- 2H)-キノリンカルポキ シレー卜
ェチル 3, 4 -ジヒドロ- 1(2H)-キノリンカルポキシレート (14.5g,
70.4mmol) と 3—クロ口プロピオニルクロリド (7.39ml, 77.4mmol) のジク ロロメタン溶液に塩ィ匕アルミニウム (23.5g, 176mmol) を水冷下で加えた後、 室温で 14時間攪拌した。反応液を氷水に注ぎ、 ジクロロメタンで抽出した。 抽出液を飽和食塩水で洗浄し、 無水硫酸ナトリウムで乾燥後、 溶媒を減圧下 留去した。 得られた残査をシリカゲルカラムクロマトグラフィー (展開溶 媒;へキサン:酢酸ェチル =3 : 1) により精製して、 へキサンから結晶化 することにより表題化合物 (15.6g) を mp. 78_79°Cの無色粉末として得た。 ¾ NMR (CDC13) δ 1.35 (3Η, t, J = 7.0 Hz), 1.93 (2H, m), 2.83 (2H, t, J = 6.2 Hz), 3.42 (2H, t, J = 7.0 Hz), 3.81 (2H, t, J = 6.2 Hz), 3.92 (2H, t, J = 7.0 Hz), 4.28 (2H, q, J = 7.0 Hz), 7.74 (2H, m), 7.92 (1H, d, J = 8.8 Hz).
元素分析値 C15H18C1N03として
計算値: C, 60.91; H, 6.13; N, 4.74.
実験値: C, 61.20; H, 6.05; N, 4.74.
参考例 2
ェチル 6- [3- -3,4-ジヒドロ- 2H)-キノリ ンカルボキシレート
参考例 1で得られたェチル 6- (3-クロ口プロパノィル) -3, 4-ジヒドロ- K2H)-キノリンカルポキシレ一ト (15. Og, 50.7醒01) のジクロロメタン溶液 に 50%ジメチルァミン水溶液 (51mL) を室温で加えた後、 2時間攪拌した。
反応液を分離後、 有機層を飽和食塩水で洗浄し、 無水硫酸ナトリウムで乾燥 後、 溶媒を減圧下留去した。 得られた残査をアルミナカラムクロマトグラフ ィー (展開溶媒;へキサン:酢酸ェチル =1 : 1) により精製して、 表題化 合物 (16.3g) を淡黄色油状物として得た。
' Ή NMR (CDC13) δ 1.34 (3Η, t, J = 7.0 Hz) , 1.96 (2H, m), 2.29 (6H, s), 2.79 (4H, m), 3.11 (2H, m), 3.79 (2H, m), 4.24 (2H, q, J = 7.0 Hz), 7.72-7.78 (2H, m), 7.78 (1H, d, J = 8.4 Hz).
参考例 3
,ェチル 6- [3- (ジメチルァミノ)プロピル]- 3, 4-ジヒドロ- 1 (2Η)-キノリンカ ルポキシレート 塩酸塩
参考例 2で得られたェチル 6 - [3- (ジメチルァミノ )プロパノィル] -3, 4-ジ ヒドロ- 1 (2H)-キノリンカルポキシレ一ト (15.4g, 50.7匪 ol) のトリフルォ 口酢酸溶液にトリエ^ルシラン (64.8ml, 406匪 ol) を窒素雰囲気下で加えた 後、 室温で 5日間攪拌した。 溶媒を減圧下留去した後、 エーテルを加えて水 で抽出した。 水層に 8規定水酸化ナトリゥム水溶液を加えアル力リ性にした 後、 酢酸ェチルで抽出した。 抽出液を飽和食塩水で洗浄し、 無水硫酸ナトリ ゥムで乾燥後、 溶媒を減圧下留去した。 得られた残査をアルミナカラムクロ マトグラフィー (展開溶媒;へキサン:酢酸ェチル =3 : 1) により精製し た。 得られた油状物のエーテル溶液に 4規定塩化水素一酢酸ェチルを加え、 生じた固体をジェチルェ一テルで洗浄することにより表題化合物 (14.8g) を吸湿性の無色粉末として得た。
'H觀 R (CDC13, フリ一塩基) δ 1.32 (3Η, t, J - 7.0 Hz), 1.78 (2H, m), 1.83 (2H, in), 2.22 (6H, s), 2.29 (2H, m), 2.56 (2H, m), 2.75 (2H, t, J = 6.6 Hz), 3.74 (2H, m), 4.24 (2H, q, J = 7.0 Hz), 6.98 (2H, m), 7.59 (1H, d, J = 8.4 Hz).
参考例 4
N, N -ジメチル- 3- (1,2,3, 4-テトラヒドロ- 6 -キノリニル) - 1 -プロパンァミン 2塩酸塩
参考例 3で得られたェチル 6 - [3- (ジメチルァミノ)プロピル] -3, 4-ジヒド ロ- 1 (2Η)-キノリンカルボキシレ一ト 塩酸塩 (14.5g, 44.4mmol) の濃塩酸 (200 mL) 溶液を 120°Cで 1 6時間攪拌し、 溶媒を減圧下留去し減圧乾燥す ることにより表題化合物 (12.8g) を mp. 250°C(decomp.) の吸湿性粉末とし て得た。
¾ NMR (D20) δ 1.78 (4Η, m), 2.41 (2H, t - like), 2.54 (6H, s), 2.60 (2H, 卜 like), 2.81 (2H, ), 3.22 (2H, m), 6.93 (3H, m).
元素分析値 C14H22N2 · 2HCIとして
計算値: C, 57.73; H, 8.31; N, 9.62.
実験値: C, 57.44; H, 8.22; N, 9.47.
参考例 5
1-[1-[(4' -クロ口 [1, -ビフエ二ル]- 4-ィル)力ルポニル] - 1, 2, 3, 4 -テトラ ヒド口- 6 -キノリニル]エタノン
4- (4—クロ口フエニル) 安息香酸 (1.05 g) のテトラヒドロフラン懸 濁液 (15 mL) に、 塩化オギザリル (0.39 mL) と N, N—ジメチルホルムァ ミド (1滴) を順次加えた。 室温で 1時間攪拌した後、 溶媒を減圧下留去し た。 得られた残查をテトラヒドロフラン (10mL) に溶解し、 氷冷下、 6—ァ セチルー 1, 2, 3, 4ーテトラヒドロキノリン (0.7g) 、 水酸化ナトリウ ム粉末' (0.31 g) と硫酸水素テトラプチルアンモニゥム (12 mg) のテトラヒ
ドロフラン (15 mL) 懸濁液に加えた。 混合物を室温で 3時間攪拌したのち、 水を加え、 酢酸ェチルで抽出した。 抽出液を飽和食塩水で洗浄し、 無水硫酸 マグネシウムで乾燥後、 溶媒を減圧下留去した。 得られた残査をジェチルェ —テルから結晶化して、 表題化合物 (l.lg) を mp 149- 151°Cの無色結晶とし て得た。
匪 R (CDC13) δ 2.03-2.15 (2Η, m), 2.53 (3H, s), 2.94 (2H, t, J=6.4Hz), 3.95 (2H, t, J=6.3 Hz), 6.87 (1H, d, J=8.6 Hz), 7.38-7.61 (9H, m) 7.79 (1H, s).
元素分析値 C24 。C1N02として
計算値: C, 73.94; H, 5.17; N, 3.59.
実験値: C, 73.79; H, 5.13; N, 3.57.
参考例 6
¾)-1-[1-[(4'-クロロ[1,1'-ビフェニル]-4-ィル)カルポニル]-1,2,3,4-テ トラヒドロ -6-キノリニル] -3- (ジメチルァミノ)-2-プロペン - 1-オン
参考例 5で得た卜 [1 - [ (4' -クロ口 [1, Γ -ビフエニル] -4-ィル)力ルポ二 ル]- 1,2, 3, 4 -テトラヒドロ- 6 -キノリニル]エタノン (0.65 g) と N, N—ジ メチルホルムアミド ジメチルァセ夕一ル (8 ml) の混合物を 110°C で 16 時間攪拌した。 室温まで冷却後、 反応液を減圧下濃縮し、 アルミナカラムク 口マトグラフィー (展開溶媒;酢酸ェチル) により精製した。 得られた残査 をジェチルエーテルから結晶化して、 表題化合物 (l.l g) を即 168- 170°Cの 無色結晶として得た。
'H R (CDC13) δ 2.00-2.15 (2Η, m), 2.75-3.20 (8H, m), 3.95 (2H, t, J=6.4 Hz), 5.64 (1H, d, J=12.3 Hz), 6.76 (1H, d, J=8.4 Hz), 7.37-7.53 (9H, m) 7.75-7.82 (2H, m) ..
元素分析値 C27H25C 1 N202として
計算値: C, 72.88; H, 5.66; N, 6.30.
実験値: C, 72.58; H, 5.84; N, 6.20.
参考例 7
卜(卜ァセチル- 2, 3, 4, 5-テトラヒドロ- 1H-卜ベンズァゼピン- 8-ィル) -3 -ク ロロ-卜プロパノン
卜ァセチル- 2, 3, 4, 5 -テトラヒドロ- 1H-卜ベンズァゼピン (17.5g,
92.5腿 ol) と 3—クロ口プロピオニルクロリド (13.2ml, 139miol) のジクロ 口ェタン溶液に塩化アルミニウム (30.8g, 231匪 ol) を水冷下で加えた後、 50°Cで 1日間攪拌した。反応液を氷水に注ぎ、 ジクロロメタン 抽出した。 抽出液を飽和食塩水で洗浄し、 無水硫酸ナトリウムで乾燥後、 溶媒を減圧下 留去した。 得られた残査をシリカゲルカラムクロマトグラフィー (展開溶 媒;へキサン:酢酸ェチル = 1 : 1) により精製して、 へキサンから結晶化 して表題化合物 (8.47g) を mp. 106- 107°Cの無色粉末として得た。
'HNMR (CDC13) δ 1.41 (1Η, m), 1.87 (3H, s), 1.87-2.08 (3H, m), 2.54-2.83 (3H, m), 3.44 (2H, m), 3.93 (2H, m) , 4.74 (1H, m), 7.38 (1H, d, J = 8.0 Hz), 7.76 (1H, s), 7.84 (1H, d, J = 8.0 Hz).
参考例 8
1 -(卜ァセチル- 2, 3, 4, 5 -テトラヒドロ- 1Η-卜ベンズァゼピン- 8-ィル) -3- (ジ メチルァミノ) -卜プロパノン
参考例 7で得られた 1 -(1-ァセチル- 2, 3, 4, 5 -テトラヒドロ- 1H-卜べンズァ ゼピン- 8 -ィル) -3-クロ口-卜プロパノン (7.10g, 25.4mmol) のジクロロメ夕
ン溶液に 50%ジメチルァミン水溶液 (27ml) を室温で加えた後、 4時間攪 拌した。 反応液を分離後、 有機層を飽和食塩水で洗浄し、 無水硫酸ナトリウ ムで乾燥後、 溶媒を減圧下留去した。 得られた残査をアルミナカラムクロマ トグラフィー (展開溶媒;へキサン:酢酸ェチル = 1 : 1) により精製し、' へキサンから結晶化して表題化合物 (5.38g) を mp. 68- 70°Cの無色粉末とし て得た。
■H MR (CDC13) δ 1.40 (1Η, m), 1.86 (3H, s), 1.81-2.07 (3H, m), 2.29 (6H, s), 2.59 (1H, m), 2.77 (4H, m), 3.13 (2H, m), 4.69 (1H, m), 7.36 (1H, d, J = 8.0 Hz) , 7.75 (1H, d, J = 1.8 Hz), 7.83 (1H, dd, J = 1.8, 8.0 Hz). 元素分析値 C17H24N202として
計算値: C, 70.80; H, 8.39; N, 9.71.
実験値: C, 70.87; H, 8.16; N, 9.44.
参考例 9
(E) -3- α -ァセチル -2, 3, 4, 5 -テ卜ラヒド口- 1H-1 -べンズァゼピン- 8-ィル) - Ν,Ν-ジメチル- 2-プロペン- 1-ァミン
参考例 8で得られた 1- (1-ァセチル - , 3, 4, 5-テトラヒド口- 1H- 1-ベンズァ ゼピン - 8-ィル) -3- (ジメチルァミノ)- 1 -プロパノン (5.00g, 17.3mmol) のト リフルォロ酢酸溶液にトリエヂルシラン (22·2ιηΙ, 139匪 ol) を窒素雰囲気下 で加えた後、 室温で 5日間攪拌した。 溶媒を減圧下留去した後、 エーテルを 加えて水で抽出した。 水層に 8規定水酸化ナトリゥム水溶液を加え塩基性に した後、 酢酸ェチルで抽出した。 抽出液を飽和食塩水で洗浄し、 無水硫酸ナ トリウムで乾燥後、 溶媒を減圧下留去した。 得られた残査をアルミナカラム クロマトグラフィー (展開溶媒;へキサン:酢酸ェチル =1 : 1) により精 製し、 表題化合物 (2.74g) を油状物として得た。
Ή NMR (CDC13) δ 1.39 (1Η, ni), 1.73-2.05 (5H, m), 2.28 (6H, s), 2.53-2.75 (4H, m), 3.08 (2H, dd, J = 0.8, 6.6 Hz), 4.69 (1H, m), 6.24 (1H, dt, J
= 6.6, 16.0 Hz), 6.48 (1H, d, J = 16.0 Hz), 7.12-7.27 (3H, m).
参考例 10
(E) -N, N -ジメチル- 3 -(2, 3, 4, 5 -テ卜ラヒドロ- 1H-卜べンズァゼピン _8-ィ ル )- 2_プロペン-卜アミン
参考例 9で得られた (E) - 3 - α -ァセチル- 2, 3, 4, 5-テトラヒドロ- 1H-卜ベン ズァゼピン- 8 -ィル)- Ν,Ν-ジメチル -2-プロペン-卜ァミン (2.73g, 9.95mmol) の濃塩酸溶液を 120°Cで 1 2時間攪拌した。 溶媒を減圧下留去した後、 8 規定水酸化ナトリゥム水溶液を加えアル力リ性にした後、 酢酸ェチルで抽出 した。 抽出液を飽和食塩水で洗浄し、 無水硫酸ナトリウムで乾燥後、 溶媒を 減圧下留去して、へキサンから結晶化することにより表題ィヒ合物 (1.49g) を mp. 87- 88°Cの 色粉末として得た。
'H MR (CDC13) δ 1.63 (2Η, m), 1.78 (2H, m), 2.26 (6H, s), 2.74 (2H, m), 3.04 (4H, m), 3.78 (1H, br), 6.18 (1H, dt, J = 6.6, 16.0 Hz), 6.42 (1H, d, J = 16.0 Hz), 6.75 (1H, d, J = 1.6 Hz), 6.85 (1H, dd, J = 1.6, 7.8 Hz), 7.04 (1H, d, J = 7.8 Hz).
元素分析値 C15H22N2として ' 計算値: C, 78.21; H, 9.63; N, 12.16.
実験値: C, 78.15; H, 9.73; N, 12.23.
参考例 1 1
(Ε)-1-[1-[(4' -クロロ [1, -ビフエ二ル]- 4 -ィル)力ルポニル] - 1, 2, 3, 4-テ トラヒドロ- 6-キノリエル]- 3 -ピペリジノ- 2 -プロペン-卜オン
参考例 6で得た (Ε) -1-[1-[(4' -クロ口 [1, Γ -ビフエニル]—4-ィル)力ルポ
ニル] -1 , 2, 3, 4 -テトラヒドロ- 6. -キノリニル] -3- (ジメチルァミノ ) -2 -プロぺ ン -1-オン (0.29 g) とピペリジン (3ml) の混合物を 110°C で 2時間攪拌し た。 室温まで冷却後、 反応液を減圧下濃縮し、 アルミナカラムクロマトダラ フィー (展開溶媒;酢酸ェチル) により精製した。 得られた残查をジェチル ェ一テルから結晶化して、 表題化合物 (0.28 g) を mp 167- 170°Cの無色結晶 として得た。
Ή NMR (CDC13) δ (6Η, m), 2.03-2.15 (2H, m), 2.92 (2H, t, J=6.6
. Θ
Hz), 3.25-3.45' (4H, m), 3.95 (2H, t, J=6.4 Hz), 5.74 (1H, d, J=12.5 Hz), 6.74 (1H, d, J=8.4 Hz), 7.37-7.61 (9H, m) 7.72-7.78 (2H, m).
参考例 12
1 -(1-ァセチル- 2, 3 -ジヒドロ- 1H -ィンドール - 5 -ィル) -3- (ジメチルァミノ) - 1-プロパノン
卜ァセチルインドリンを用いて、 参考例 1および参考例 2と同様の操作を 順次行うことにより、 表題化合物を粘ちゆうな油状物として得た。
Ή NMR (CDC13) δ 2.21-2.33 (9Η, m), 2.74 (2H, t, J=7.2 Hz), 3.11 (2H, t, J=7.2 Hz), 3.23 (2H, i, J=8.6 Hz), 4.12 (2H, t, J=8.6 Hz), 7.78-7.97 (2H, m) 8.24 (1H, d, J=8.4 Hz).
参考例 13
(E)- 3- [2, 3-ジヒドロ- 1H-インド一ル _5_ィル] - N, N-ジメチル- 2-プロペン -卜 ァミン
、
I
H
1) 参考例 12で得た卜(卜ァセチル- 2, 3-ジヒドロ- 1H-インドール- 5 - ィル) - 3- (ジメチルァミノ)-卜プロパノン (4.3g) のメタノール溶液 (40ml)
に、 氷冷下に水素化ホウ素ナトリウム (0.75 g) を加え、 混合物を 0-5°C で 30分間攪拌した。反応液に水-氷を加えた後、溶媒を減圧下留去し、酢酸ェチ ルで抽出した。 抽出液を飽和食塩水で洗净し、 無水硫酸マグネシウムで乾燥 後、 溶媒を減圧下留去した。 得られた残査をアルミナカラムクロマトグラフ ィ一 (展開溶媒;酢酸ェチル) により精製して、 3 - [1-ァセチル- 2,3-ジヒド ロ- 1H-インド一ル- 5-ィル] -3-ヒドロキシ- Ν,Ν-ジメチル- 1-プロパンァミン (3.3 g) を無色粉末として得た。
2) 上記 1 ) で得た 3- [1-ァセチル -2, 3-ジヒドロ- 1H-ィンド一ル- 5 -ィ ル]- 3-ヒドロキシ -N,N-ジメチル-卜プロパンァミン (3.3 g) と濃塩酸 (20 il) の混合物を 16時間加熱還流した。室温まで冷却後、 反応液を減圧下濃縮し、 水で希釈した後、 2規定水酸化ナトリウム水溶液でアルカリ性にし、 酢酸ェ チルで抽出した。 抽出液を飽和食塩水で洗浄し、 無水硫酸マグネシウムで乾 燥後、 溶媒を 圧下留去して、 表題化合物 (2.3 g) を油状物として得た。 Ή腿 (CDC13) δ 2.25 (6Η, s), 2.97-3.04 (4H, m), 3.55 (2H, t, J=8.2Hz), ca. 3.8 (1H, br.s, NH), 5.98-6.09 (lH, m), 6.41 (1H, d, J=16.2 Hz), 6.56 (1H, d, J-8.1 Hz), 7.02 (1H, dd, J=1.5, 8.1 Hz), 7.19 (1H, s).
参考例 14
1 -(1 , 2, 3, 4 -テトラヒドロ- 6 -キノリニル) -4- (ジメチルァミノ ) - 1-ブ夕ノン
ェチル 3, 4-ジヒドロ- 1(2H)-キノリンカルポキシレートを用いて、 参考例 1、 参考例 2および参考例 4と同様の操作を順次行うことにより、 表題化合 物を油状物として得た。
¾ NMR (CDC13) δ 1.87-2.00 (4Η, m), 2.33 (6H, s), 2.48 (2H, t, J = 7.4 Hz), 2.78 (2H, t, J = 6.3 Hz), 2.91 (2H, t, J = 7.2 Hz), 3.37 (2H, t, J = 5.6 Hz), 4.4,(1H, br, NH), 6.39 (1H, d, J = 9.2 Hz), 7.60-7.64 (2H, m).
参考例 15
4 -ォキソ -4- [2- (トリフルォロアセチル )-1, 2, 3, 4—テトラヒドロ- 7 -ィソキ ノリニル]ブ夕ン酸
1) 無水トリフルォロ酢酸 (47.5 ml, 336誦 ol)を 1, 2, 3, 4-テトラヒド 口イソキノリン (25 g, 188匪 ol)の THF溶液 (100 ml) に 0°Cで滴下し、 2 時間室温で撹拌した後、 溶媒を減圧留去した。 残さに水に注ぎ、 酢酸ェチル で抽出し、 1N塩酸で洗浄後、 無水硫酸マグネシウムで乾燥した。 溶媒を減圧 留去して、 2- (トリフルォロアセチル) - 1, 2, 3, 4 -テトラヒドロイソキノリン 43.5 gを油状物として得た。
Ή-NMR (CDC13) δ: 3.00-2.93 (2Η, m), 3.92-3.80 (2H, m), 4.77 (2H, m), 7.28-7.13 (4H, m).
2) 上記 1 )で得た 2- (トリフルォロアセチル) -1, 2, 3, 4 -テトラヒドロイ ソキノリン (10 g, 43.6 mmol)と無水コハク酸 (4.8 g, 48 ramol) のジクロ ロェタン混合物に、 室温で塩化アルミニウム(26 g, 200 mmol)を少量ずつ加 え、 45°Cで 1時間撹拌した。 反応液を氷水に注ぎ、 酢酸ェチルで抽出し、 飽 和食塩水で洗浄し、 無水硫酸マグネシウムで乾燥した。 溶媒を減圧留去し、 シリカゲルカラムクロマトグラフィー (展開溶媒;へキサン:酢酸ェチル = 1 : 1) で精製し、 表題化合物 7.5 gを無色粉末として得た。
Ή-NM (D S0-d6) δ 2.58 (2Η, m), 3.00 (2H, m), 3.23 (2H, m), 3.83 (2H, m), 4.84 (2H, m), 7.38 (1H, m), 7.84 (1H, m), 7.93 (1H, m), 12.17 (1H, s).
参考例 16 '
4-ォキソ _4- [3- (トリフルォロアセチル) -2, 3, 4, 5 -テ卜ラヒドロ- 1H- 3 -ベン ズァゼピン- 7-ィル]ブタン酸
2, 3, 4, 5-テトラヒドロ- 1H-3-ベンズァゼピンを用いて、 参考例 15と同様 の操作を行うことにより、 表題化合物を無色粉末として得た。
'H-NMR (CDC13) δ: 2.81 (2Η, t, J=6.4Hz), 2.90-3.15 (4H, m), 3.29 (2H, t, J=6.4Hz), 3.65-3.85 (4H, m), 7.20-7.33 (1H, m), 7.75-7.85 (2H, in), ca. 10 (1H, br).
参考例 17
N,N-ジプロピル- (4-エトキシカルポニルメトキシ- 3-ニトロフエニル)ァセト
1) (4-ヒドロキシフヱニル)酢酸 (50.4 g, 330 mmol)の酢酸溶液 (230 ml)に、 氷冷下に硝酸 (24.5 ml, 398匪 ol)の酢酸溶液 (20 ml)を、 反応液の 温度が 1(TCを越えないようにゆっくり滴下した。 反応液を 2時間撹拌後、 水 (1L)を滴下し、 析出した結晶をろ取した。 得られた結晶を水洗後、 乾燥し、 (4 -ヒドロキシ- 3-ニトロフエニル)酢酸 (49 g)を nip 144- 146°Cの結晶として 得た。
'H-NMR (CDC13) δ 3.76 (2Η, s), 7.16 (1H, d, J = 8:8 Hz), 7.53 (1H, dd, J = 8.8, 2.2 Hz), 8.04 (1H, d, J = 2.2 Hz).
2) 上記 1) で得た(4-ヒドロキシ- 3-ニトロフエニル)酢酸 (25 g, 127 mmol)の THF溶液 (100 ml)に塩化チォニル (50 ml, 680 mmol)を室温で滴下 し、 2時間加熱還流した。反応液を濃縮し、得られた残渣をクロ口ホルム(250 ml)に溶解し、 ジプロピルアミン(35 ml, 255 mmol)のクロ口ホルム溶液(300 ml)に、 氷冷下 1時間かけて滴下した。 滴下後、 反応液を水および飽和重曹水 で洗浄し、 有機層を無水硫酸ナトリウムで乾燥、 濃縮した。 残渣を酢酸ェチ ル-へキサンより再結晶し、 N,N-ジプロピル-(4-ヒドロキシ- 3-二トロフエ二 ル)ァセトアミド(26'.5 g)を mp 55-57°Cの結晶として得た。
Ή—画 R (CDC13) δ: 0.8-1.0 (6Η, m), 1.4-1.7 (4H, m), 3.2-3.4 (4H, m), 3.67
(2H, s), 7.12 (1H, d, J = 8.6 Hz), 7.53 (1H, dd, J = 8.6, 2.2 Hz), 7.96 (1H, d, J - 2.2 Hz).
3) 上記 2) で得た N,N-ジプロピル- (4-ヒドロキシ -3-ニトロフエニル) ァセトアミド (3, 5 g, 17.8 mmol)およびブロモ酢酸ェチル (3.0 ml, 26.7 匪 ol)の DMF溶液 (40 ml)に、 炭酸カリウム(7.4 g, 53 mmol)を加えた。 反応 液を室温で終夜撹拌後、 反応液に水を加え、 酢酸ェチルで抽出した。 抽出液 を水洗し、 無水硫酸ナトリウムで乾燥、 濃縮した。 残渣を酢酸ェチル -へキサ ンより再結晶し、 表題化合物 (4.9 g, 75 %)を即 79- 80°Cの結晶として得た。 Ή-NMR (CDC13) δ: 0.8-1.0 (6Η, m), 1.29 (3H, t, J = 7.0 Hz), 1.4-1.7 (4H, m), 3.1-3.4 (4H, i), 3.68 (2H, s), 4.27 (2H, q, 7.0 Hz), 4.76 (2H, s), .6· 96 (1H, d, J = 8.6 Hz) , 7.38 (1H, dd, J = 8.6, 2.2 Hz) , 7.77 (1H, d, J = 2.2 Hz).
元素分析値 C18H26N206として
計算値: C, 59.00; H, 7.15; N, 7.65. ·
実験値: C, 58.92; H, 7.15; N, 7.85.
参考例 18
3- (4-エトキシカルポニルメトキシ- 3-ニトロフェニ^/)プロピオン酸メチル
1) 3- (4-ヒドロキシフエニル)プロピオン酸を用いて、 参考例 17の 1) と同様の操作を行うことにより、 3- (4-ヒドロキシ- 3-ニトロフエニル)プロピ オン酸を粉末として得た。
Ή-NMR (CDC13) δ: 2.70 (2Η, t, J = 7.4 Hz), 2.95 (2H, t, J = 7.4 Hz), 7.10 (1H, d, J = 8.8 Hz), 7.46 (1H, dd, J = 8.8, 2.0 Hz), 7.96 (1H, d, J = 2.0 Hz).
融点: 80-82 °C (結晶化溶媒:酢酸ェチル -へキサン)
2) 上記 1)で得た 3- (4-ヒドロキシ -3-ニトロフエニル)プロピオン酸(49
g, 232腿 ol)のメタノ-ル溶液(500 ml)に塩化チォニル(15 ml)を滴下し、 終 夜室温で撹拌した。 反応液を濃縮後、 水 (500 ml)を加え、 酢酸ェチルで抽出' した。 抽出液を水および飽和重曹水で洗浄後、 硫酸マグネシウムで乾燥、 濃 縮して、 3- (4-ヒドロキシ -3-二トロフエニル)プロピオン酸メチル (47 g)を粉 末として得た。
Ή -画 R (CDC13) δ: 2.64 (2Η, t, い 7.4Hz), 2.95 (2H, t, J = 7.4Hz), 3.68 (3H, s), 7.10 (1H, d, J = 8.6Hz), 7.46 (1H, dd, J = 8.6, 2.2Hz), 7.95 (1H, d, J = 2.2 Hz).
融点: 60- 62°C (結晶化溶媒:酢酸ェチル -へキサン)
3) 上記 2)で得た 3- (4-ヒドロキシ- 3-ニトロフエニル)プロピオン酸メ チルを用いて、 参考例 17の 3) と同様の操作を行うことにより、 表題化合 物を粉末として得た。
Ή-NMR (CDC13) δ: 1.28 (3Η,, t, J = 7.0Hz), 2.64 (2H, t, J = 7.4Hz) , 2.95 (2H, t, J = 7.4Hz), 3.67 (3H, s), 4.26 (2H, q, J = 7.0Hz), 4.75 (2H, s), 6.93 (1H, d, J = 8.6Hz), 7.38 (1H, dd, J = 8.6, 2.2Hz), 7.72 (1H, d, J = 2.2Hz).
融点: 70- 72°C (結晶化溶媒:酢酸ェチル -へキサン)
参考例 19
3, 4 -ジヒドロ- 6- (3-ョ-ドプロピル) -4- (2-ナフ夕レンスルホニル) -2H-1 , 4- ベンズォキサジン
1) 参考例 18で得た 3- (4-エトキシカルポニルメトキシ- 3-ニトロフエ ニル)プロピオン酸メチルを用いて、実施例 133と同様の操作を行うことに より、 3- (3, 4 -ジヒドロ- 2H- 1, 4-ベンズォキサジン -3-ォキソ - 6-ィル)プロピ オン酸メチルを粉末として得た。
Ή-NMR (CDC13) δ: 2.60 (2Η, t, J = 7· 4 Hz), 2.88 (2Η, t, J = 7.4 Hz),
3.68 (3H, s), 4.59 (2H, s), 6.7-7.0 (3H, m).
融点: 131- 132°C (結晶化溶媒:酢酸ェチル -へキサン)
2) 上記 1) で得た 3- (3, 4-ジヒドロ- 2H- 1,4-ベンズォキサジン- 3-ォキ ソ- 6-ィル)プロピオン酸メチル (24 g, 102 mmol)の THF (400 ml)溶液に、 1 規定のポラン ZTHF溶液 (150 ml, 150 mmol)を氷冷下加えた。 反応液を室温 で終夜撹拌後、 6規定塩酸' (50 ml, 300匪 ol)を加え 2時間撹拌後、 6規定水 酸化ナトリウム水溶液で中和し、 酢酸ェチルで抽出した。 抽出液を水および 飽和食塩水で洗浄後、 硫酸マグネシウムで乾燥し濃縮した。 残渣のァセトニ トリル溶液 (300 ml)にトリエチルァミン (25g, 250 mmol)を加えた後、 2-ナ フタレンスルホニルクロリド (56 g, 250 mmol)のァセトニトリル溶液 (100 ml)を氷冷下加え、 室温で 4時間撹拌した。 反応液を濃縮し、 残渣に水を加え、 酢酸ェチルで抽出した。 抽出液は水および飽和食塩水で洗?争後、 硫酸マグネ シゥムで乾燥、 濃縮した。 残渣のアセトン溶液 (500 ml)にヨウ化ナトリウム (37.5 g, 250 mmol)を加え室温で終夜撹拌した。反応液を濃縮し、 水 (500 ml) を加え、 酢酸ェチルで抽出した。 抽出液を、 水および飽和食塩水で洗浄後、 硫酸マグネシウムで乾燥、 濃縮して、 表題化合物 (22 g)を粉末として得た。 Ή-N R (CDC13) 6: 2.0-2.2 (2H, m), 2.71 (2H, t, J = 7.4 Hz), 3.18 (2H, t, J = 7.2 Hz), 3.72 (2H, t, J = 4.6 Hz), 3.93 (2H, t, J = 4.6 Hz), 6.70 (1H, d, J = 8.0 Hz), 6.90 (1H, dd, J = 8.0, 1.8 Hz), 7.5-7.8 (4H, m), 7.8-8, 0 (3H, m), 8.30 (1H, s).
融点: 87-88 °C (結晶化溶媒:酢酸ェチル -へキサン)
参考例 20
N, N-ジプロピル- [4- (4-メトキシフエ二ル)力ルポ二ルメトキシ -3-ニトロフ
参考例 17の 2) で得た Ν,Ν-ジプロピル-(4-ヒドロキシ- 3-ニトロフエ二
ル)ァセトアミドを用いて、 参考例 17の 3) と同様の操作を行うことにより、 表題化合物を粉末として得た。 ' Ή-NMR (CDC13) δ: 0.8-1.0 (6Η, m), 1.4-1.7 (4H, m), 3.1-3.4 (4H, m), 3.65 (2H, s), 3.89 (3H, s), 5.34 (2H, s), 6.9-7.1 (3H, m), 7.40 (1H, dd, J = 8.6, 2.2 Hz), 7.76 (1H d, J = 2.2 Hz), 8.00 (2H, "d, J = 9.0 Hz). 融点: 95-97 °C (結晶化溶媒:酢酸ェチル -へキサン)
参考例 21
3 - (4-クロロフエニル)プロピルアミン
1) 3 -(4-クロ口フエニル)プロピオン酸 (5.00 g, 27.0 mmo)と塩化チォ ニル (3 ml)の混合物を 2時間還流した後、 過剰の塩ィ匕チォニルを減圧留去し た。 得られた残査をテトラヒドロフラン (200 ml)に溶角军し、 LiAlH
4のテトラ ヒドロフラン懸濁液に 0°Cでゆっくりと滴下し、 室温で 1時間攪拌した。 反 応混合物に水、 1N水酸化ナトリウム水溶液を加え、 不溶物をろ去した後、 ろ 液を無水硫酸マグネシウムで乾燥した。溶媒を減圧下留去して、 3_(4-クロ口 フエニル)プロピルアルコール 4.6 gを油状物として得た。
Ή-NMR (CDC13) δ: 1.86 (2Η, tt, J = 7.4, 7.4 Hz), 2.68 (2H, t, J = 7. Hz), 3.67 (2H, t, J = 7.4 Hz), 7.12 (2H, d, J = 8.4 Hz), 7.27 (2H, d, J = 8.4 Hz).
2) 上記 1)で得た 3-(4-クロ口フエニル)プロピルアルコール (4.6g, 27 IMOI)とトリエチルァミン (3.78 ml, 27.1匪 ol)のテトラヒドロフラン (100 ml)溶液にメシルクロリド (2.10 ml, 27.1 mmol)を 0 °Cで加え、 室温で 30分 攪拌した。反応混合物に水を加え、酢酸ェチルで抽出した。抽出液を飽和 NaCl 水溶液で洗浄後、 無水硫酸マグネシウムで乾燥した。 溶媒を減圧下に留去し た後、 反応混合物とフタルイミドカリウム (5.02 g, 27.1 画 ol)をジメチル ホルムアミドに溶解し、 80°Cで 10時間加熱攪拌した。 得られる溶液に 8N水 酸化ナトリウム水溶液を加え、 酢酸ェチルで抽出した。抽出液を飽和 NaCl水 溶液で洗浄後、 無水硫酸マグネシウムで乾燥した。 溶媒を減圧下に留去して、
2- [3- (4 -クロロフエニル)プロピル] - 1H -ィソインドール- 1, 3 (2H)-ジオン 7.47 gを固体として得た。
Ή-NMR (CDC13) δ: 2.00 (2Η, tt, J = 7.4, 7.4 Hz), 2.69 (2H, t, J = 7.4 Hz), 3.73 (2H, t, J = 7.4 Hz), 7.10-7.82 (4H, m), 7.69-7.89 (4H, m).
3) 上記 2) で得た 2- [3- (4-クロロフヱニル)プロピル] -1H-イソインド ール -1,3(2H) -ジオン (7.47 g, 24.8腿 ol) とヒドラジン一水和物 (2.4 ml, 49.7讓 ol)のエタノール溶液を 10時間加熱還流した。 溶媒を留去した後、 水 を加え、 酢酸ェチルで抽出した。 抽出液を飽和 NaCl水溶液で洗浄後、 無水硫 酸マグネシウムで乾燥した。溶媒を減圧下留去して、 表題化合物 3.66 gを油 状物として得た。
'H-NMR (CDC13) δ: 1.80 (2Η, tt, J = 7/4, 7.4 Hz), 2.63 (2H, t, J = 7.4 Hz), 2.76 (2H, t, J = 7.4 Hz), 3.08 (2H, s), 7.08-7.29 (4H, m).
参考例 22
2- [4- (4 -クロロフェニル) - 1-ピぺリジニル] -2-ォキソェチルァミン 塩酸塩
1) シアノリン酸ジェチル (1.29ml) を 4- (4-クロ口フエ二ル)- 1 -ピ ペリジン 塩酸塩 (1.80 g) 、 N- (tert-ブトキシカルポニル)グリシン (1.49 g) 、 トリェチルァミン (2.38ml) の DMF (80 ml) 溶液に加えた。 反応 混合物を室温で 4時間攪拌後、 水で希釈し、 エーテルで抽出した。 抽出液を 飽和食塩水で洗浄後、 無水硫酸マグネシウムで乾燥し、 溶媒を減圧下留去し た。 残渣をシリカゲルカラムクロマトグラフィー (n-へキサン/酢酸ェチル = 1/1) で精製して、 ter卜ブチル -2- [4- (4-クロ口フエ'ニル) -卜ピベリジ二 ル]- 2-ォキソェチルカルバメート (2.48 g) を得た。
Ή-NMR (CDC13) δ: 1.46 (9Η, s), 1.50-1.70 (2H, m), 1.80-2.00 (2H, m), 2.60-2.90 (2H, m), 3.00-3.20 (1H, m), 3.75-3.90 (1H, m), 3.99 (2H, m), 4.70-4.80 (1H, ), 5.56 (1H, m), 7.11 (2H, d, J=8.4Hz), 7.29 (2H, d,
J=8.4Hz) . ·
2) 上記 1) で得られた tert -プチル- 2- [4- (4-クロ口フエニル) -1-ピぺ リジニル] -2-ォキソェチルカルバメート (2.48 g) を 4規定塩化水素酢酸ェ チル溶液 (50m l) に溶解し、 室温で 4時間攪拌した。 溶媒を減圧下留去し て表題化合物 (2.16 g) を得た。
MS(ESI) (M+H): 253.
'H-NMR (CDC13) δ: 1.40-2.00 (4Η, m), 2.65-3.00 (2H, m), 3.05-3.20 (1H, m), 3.75-4.00 (3H, m), 4.40-4.60 (1H, m), 7.27 (2H, d, J=8.8Hz) , 7.37 (2H, d, J=8.5Hz), 8.25 (2H, m) .
参考例 23
2- [4- (2-メチルフエニル) -1-ピぺリジニル] -2-ォキソェチルァミン 塩酸塩
1) 4-(2-メチルフエ二ル)-卜ピペリジン塩酸塩を用いて、 参考例 22 の 1) と同様の操作を行うことにより、 tert-ブチル -2- [4- (2-メチルフエ二 ル)-卜ピぺリジニル] -2-ォキソェチルカルバメートを得た。
Ή-NMR (CDC13) δ 1.46 (9Η, s), 1.55-1.75 (2H, m), 1.80-1.90 (2H, m), 2.36 (3H, s), 2.60-2.80 (1H, m), 2.90-3.20 (2H, m), 3.75-3.90 (1H, m), 4.01 (2H, m), 4.70-4.85 (1H, m), 5.58 (1H, m), 7.00-7.20 (4H, m).
2) 上記 1) で得た tert-ブチル -2- [4- (2-メチルフエニル) -1-ピベリジ 二ル]- 2-ォキソェチルカルバメートを用いて、 参考例 22の 2) と同様の操 作を行うことにより表題化合物を得た。
MS (ESI) (M+H): 233.
!H-NMR (CDC13) δ 1.40-2.00 (4Η, m), 2.32 (3H, s), 2.70-2.91 (1H, m), 2.95-3.30 (2H, m), 3.75-4.00 (3H, m), 4.40-4.60 (1H, m), 7.10-7.30 (4H, m), 8.25 (2H, m).
参考例 24
2- [4- (4-フルオロフェニル) -卜ピペラジニル] -2-ォキソェチルァミン 2塩
1) 卜(4-フルオロフェニル)ピぺラジンを用いて、 参考例 22の 1) と 同様の操作を行うことにより、 tert-ブチル -2- [4- (4-フルオロフェニル )-1- ピペラジニル ]-2-ォキソェチルカルバメートを得た。 ·
Ή-NMR (CDC13) δ: 1.46 (9Η, s), 3.05-3.15 (4H, m), 3.55 (2H, t, J=5. lHz), 3.79 (2H, t, J=5.1Hz), 4.01 (2H, d, J=4.5Hz), 5.52 (1H, m), 6.85-7.05 (4H, m).
2) 上記 1) で得た ter卜ブチル - 2-[4- (4-フルオロフェニル )- 1-ピペラ ジニル ]-2-ォキソェチルカルバメ一卜を用いて、 参考例 22の 2) と同様の 操作を行うことにより表題化合物を得た。 , MS(ESI) (M+H): 238.
Ή-NMR (CDC13) δ: 3.25-3.60 (4Η, m), 3.70-4.00 (6H, m), 7.15-7.30 (3H, m), 7.30-7.50 (1H, m).
参考例 25
2- [4- (2-メトキシフエ二ル)- 1 -ピペラジニル ]-2-ォキソェチルァミン 2塩
1) 1- (2-メトキシフエエル)ピぺラジンを用いて、 参考例 22の 1) と 同様の操作を行うことにより、 tert-ブチル—2-〔4- (2 -メトキシフエニル) -1 - ピペラジニル ]-2 -ォキソェチルカルバメートを得た。
Ή-NMR (CDCL) δ: 1.46 (9Η, s), 3.00-3.07 (4H, m), 3.56 (2H, t, J=5.4Hz),
3.82 (2H, t, J=5.4Hz), 3.88 (3H, s), 4.01 (2H, d, J-4.5Hz), 5.56 (1H, m),' 6.85-7.05 (4H, m).
2) 上記 1) で得た ter卜ブチル - 2- [4_(2 -メトキシフエ二ル)- 1-ピペラ ジニル ]-2-ォキソェチルカルバメ一トを用いて、 参考例 22の 2) と同様の 操作を行うことにより表題化合物を得た。
MS (ESI) (M+H): 250.
Ή-NMR (CDC13) δ: 3.20-3.50 (4Η, m), 3.75-4.10 (6H, m), 3.87 (3H, s), 7.01 (1H, t, J=8.0Hz), 7.15 (1H, d, J=8.0Hz), 7.27 (1H, t, J=8.0Hz), 7.49 (1H, d, J=8.0Hz) .
参考例 26
2 - (4-クロロフエノキシ)ェチルァミン
1) 4 -クロ口フエノール (2 g, 15.6誦 ol)のジメチルホルムアミド(20 ml)溶液に水素化ナトリウム (60% in oil, 640 mg, 16丽 ol)を加え、 室温で 3Q分攪拌した後、 N-(2 -プロモェチル)フタルイミド (4g, 15.6imnol)を加え、 50°Cで 2時間加熱攪拌した。 溶媒を減圧下に留去した後、 水を加え、 酢酸ェ チルで抽出した。 抽出液を飽和 NaCl水溶液で洗浄後、 無水硫酸マグネシウム で乾燥した。 溶媒を減圧下に留去して 2- [3- (4-クロロフエノキシ)ェチル] - 1H -イソインドール- 1,3 (2H)-ジオン 1.00 gを粉末として得た。
'H-NMR (CDC13) 6: 4.10 (2H, t, J = 5.7 Hz), 4.18 (2H, t, J = 5.7 Hz), 7.10-7.82 (4H, m), 7.69-7.89 (4H, m).
2) 上記 1) で得た 2- [3- (4_クロロフエノキシ)ェチル]- 1H-イソインド ール -1,3(2H)-ジオンを用いて、 参考例 21の 3) と同様の操作を行うことに より、 表題化合物を得た。
Ή-NMR (CDC13) δ 3.10 (2Η, t, J = 5.4 Hz), 3.40 (2H, s), 3.98 (2H, t, J = 5.4 Hz), 6.82 (2H, d, J = 9.2 Hz), 7.24 (2H, d, J = 9.2 Hz).
参考例 27
tert -ブチル 8-ヒドロキシ- 1, 3, 4, 5 -テトラヒドロ- 2H- 2 -ベンズァゼピン - 2- カルポキシレート
2, 3, , 5 -テトラヒド口- 1H -2 -ベンズァゼピン _8-オール臭化水葶酸塩 (12. Og, 49.2匪。1) のクロ口ホルム (40ml) と水 (40ml) 溶液に 2規定水酸 化ナトリウム (40ml) と二炭酸 t-ブチルを 0°Cで加え、 室温で 16時間攪拌し た。 得られる混合液に酢酸ェチルを加え、 飽和食塩水で洗浄し、 無水硫酸ナ トリウムで乾燥した。 溶媒を減圧下濃縮後、 得られた残査を酢酸ェチルーィ ソプロピルエーテルより粉末として、 表題化合物 (7.99g) を得た。
Ή NMR (CDC13) δ: 1.40 (9Η, s), 1.73 (2H, m), 2.86 (2H, m), 3.67 (2H, m), 4.30-4.36 (2H, i), 6.61-6.70 (2H, m), 6.98 (1H, m).
参考例 28
1 - [(4-フエニル -1-ピペリジニル)カルボ二ル]- 1, 2, 3, 4-テトラヒドロキノリ ン
1) 1,2,3,4-テ卜ラヒドロキノリン (lml, 7.97麵。1)を, (20ml)に溶 解し、 ピリジン (1.58ml, 15.93腿 ol)を加え、 氷冷した。 反応液にクロ口ぎ 酸 P-ニトロフエニル (1.61g, 7.97匪 ol)を加え、 室温で 4時間攪拌した後、 水、 飽和食塩水を加え、 酢酸ェチルで抽出した。 抽出液を硫酸マグネシウム で乾燥後、 減圧下に濃縮して、 4 -ニトロフエニル 3,4-ジヒドロキノリン-
1 (2H)-カルポキシレート 2.57gを淡黄色液体として得た。
2) 上記 1) で得た 4-ニトロフエニル 3,4-ジヒドロキノリン- 1(2H)-力
ルポキシレートを DMSO (10ml)に溶解し、 4-フエ二ルビペリジン 塩酸塩 (1.58g, 7.97讓。1)、 4規定水酸化ナトリウム水溶液 (2.09ml, 8.36匪01)を 加え、 室温で 22. 5時間攪拌した。 反応液に酢酸ェチル 60mlを加え、 炭酸 カリウム水溶液、 飽和食塩水で洗浄した。 有機層を硫酸マグネシウムで乾燥 し、減圧下濃縮して得られた残さをシリカゲルカラムクロマトグラフィー(展 開溶媒;へキサン:酢酸ェチル = 2 : 1) で精製し、 淡黄色液体として表題 化合物 2.10gを得た。
Ή-NMR (CDC13) δ 1.68 (2Η, m), 1.80 (2H, m), 1.98 (2H, m), 2.65 (1H, m), 2.78 (2H, dd, J=6.6 and 6.9Hz), 2..85 (2H, m), 3.62 (2H, t, J=6.1Hz), 3.95 (2H, m), 6.90 (1H, m), 7.04-7.32 (8H, m). 実施例 1
3 - [ト([1, Γ -ビフエ二ル]- 4-ィルカルボニル) - 1, 2, 3, 4-テトラヒドロ- 6 -キ ノリニル] - Ν, Ν -ジメチル- 1-プロパンァミン
参考例 4で得た Ν, Ν -ジメチル- 3 -(1, 2, 3, 4 -テトラヒドロ- 6-キノリニル) - 卜プロパンァミン 2塩酸塩 (400mg, 1.37mmol) とトリエチルァミン (669ml, 4.81mmol) のジメチルホルムアミド溶液に塩化ビフエ二ルカルポ二 ル (327mg, 1.51皿01) を氷冷下で加えた後、 室温で 3日間攪拌した。 反応液 に酢酸ェチルを加え、飽和炭酸水素ナトリゥム水溶液と飽和食塩水で洗浄し、 無水硫酸ナトリウムで乾燥後、 溶媒を減圧下留去した。 得られた残査をアル ミナカラムクロマトグラフィー (展開溶媒;へキサン:酢酸ェチル =3: 1) により精製して、へキサンから結晶化することにより表題化合物 (113mg) を mp. 100- loreの無色粉末として得た。
Ή NMR (CDC13) δ 1.73 (2Η, ηι), 2.06 (2H, m), 2.20 (6H, s), 2.26 (2H, m),
2.54 (2H,. m), 2.83 (2H, m), 3.92 (2H, t-like), 6.72 (2H, m), 6.99 (1H, s), 7.35-7.60 (9H, m).
元素分析値 C27H3。N20として
計算値: C, 81.37; H, 7.59; , 7.03. ,
実験値: C, 81.26; H, 7.46; N, 7.05.
実施例 2
(E) -3- [卜( [1 , Γ -ビフエニル] -4 -ィルカルポニル) -2, 3, 4, 5-テトラヒドロ- 1H-卜ベンズァゼピン- 8-ィル] - Ν,Ν-ジメチル - 2_プロペン-卜アミン塩酸塩
参考例 10で得た (Ε) -Ν, Ν-ジメチル- 3- (2, 3, 4, 5 -テ卜ラヒドロ- 1H—1-ベン ズァゼピン -8-ィル) -2-プロペン-卜ァミン (300mg, 1.30腿 ol) 、 水酸化ナト リウム (130mg, 3.26mmol) と硫酸水素テトラプチルアンモニゥム(4.4mg, 13.0匪 ol) のテトラヒドロフラン溶液に塩化ビフエ二ルカルポニル (423mg, 1.95mmol) を氷冷下で加えた後、 室温で 5時間攙拌した。 反応液に酢酸ェチ ルを加え、 飽和食塩水で洗浄し、 無水硫酸ナトリウムで乾燥後、 溶媒を減圧 下留去した。 得られた残査をアルミナカラムクロマトグラフィー (展開溶 媒;へキサン:酢酸ェチル =3 : 1) により精製した。 得られた油状物に 4 規定塩化水素一酢酸ェチルを加え、 生成した結晶をジェチルェ一テルで洗浄 することにより表題化合物 (124in
g) を mp. 112-113°Cの無色粉末として得た
c Ή NMR (CDC1
3, フリ一塩基) δ 1.53 (1H, m), 1.96 (2H, m), 2.15 (6H, s), 2.77-3.07 (6H, m), 5.04 (1H, m), 5.93 (1H, dt, J = 6.6, 15.8 Hz), 6.20 (1H, d, J = 15.8 Hz), 6.68 (1H, s), 7.02-7.51 (11H, m).
元素分析値 C28H30N20 · HC1 · 1.5H20として
計算値: C, 70.94; H, 7.23; N, 5.91.
実験値: C, 71.40; H, 7.31; N, 6.11.
実施例 3
3_[1-([1,1'-ビフェニル]-4-ィルカルポニル)-2,3,4, 5—テトラヒドロ- 1H— 1- ベンズァゼピン- 8-ィル] -N,N -ジメチル- 1-プロパンアミン 塩酸塩
実施例 2で得た (E) - 3- [卜( [1, Γ -ビフェニル] -4-ィルカルポニル) - 2,3,4, 5-テトラヒドロ- 1H-1-ベンズァゼピン- 8-ィル] -Ν,Ν-ジメチル- 2-プロ ペン -1-ァミン (238mg, 0.580腿 ol) のテトラヒドロフラン溶液にパラジウム 一炭素 (200mg) を加え、 水素雰囲気下で 1. 5日間攪拌した。触媒を濾過し た後、 溶媒を減圧下留去した。 得られた残査をアルミナカラムクロマトダラ フィー (展開溶媒;へキサン:酢酸ェチル =3 : 1) により精製した。 得ら れた油状物に 4規定塩化水素一酢酸ェチルを加え、 生成した結晶をジ土チル エーテルで洗浄することにより表題化合物 (97.9mg) を即. 84- 86°Cの無色 粉末として得た。 '
1腿 R (CDC13, フリー塩基) δ 1.35-1.52 (3Η, m), 1.93-2.00 (10H, m), 2.33 (2H, m), 2.79-3.02 (4H, m), 5.04 (1H, m), 6.49 (1H, s), 6.89 (1H, m), 7.12 (1H, d, J = 7.8 Hz), 7.22-7.52 (9H, m).
元素分析値 C28H32N20 · HC1 · H20として
計算値: C, 72.01; H, 7.55; N, 6.00. - 実験値: C, 71.88; H, 7.56; N, 5.99.
実施例 4 '
3-D -.[(4' -クロ口 [1, -ビフエ二ル] - 4 -ィル)力ルポ二ル]- 1, 2, 3, 4-テトラ ヒドロ- 6-キノリニル]- 3-ヒドロキシ- Ν, Ν-ジメチル -1-プロパンァミン
参考例 6で得た (E) -卜 [卜 [ (4' -クロ口 [1, 1 ' -ビフエニル] _4 -ィル)力ルポ ニル] -1 , 2, 3, 4 -テトラヒド口- 6 -キノリニル] -3- (ジメチルァミノ ) -2 -プロべ ン- 1-オン (0.3 g) のメタノール (30 ml) 溶液に、 水素化ホウ素ナトリウム (0.6 g) を加え、 3時間加熱還流した。 溶媒を減圧下留去した後、 残查を水 —酢酸ェチルに溶かし、 酢酸ェチルで抽出した。 抽出液を水で洗浄し、 無水 硫酸マグネシウムで乾燥後、 溶媒を減圧下留去した。 得られた残查をアルミ ナカラムクロマトグラフィー (展開溶媒;酢酸ェチル) により精製して、 表 題化合物(0.1 g) を非晶状粉末として得た。
Ή NMR (CDC13) δ 1.72-1.80 (2Η, m) , 2.00-2.12 (2Η, m), 2.28 (6H, s), 2.40-2.50 (1H, m), 2.60-2.70 (1H, m), 2.87 (2H, t, J = 6.7 Hz), 3.04 (2H, d, J = 6.6 Hz), 4.83 (1H, t, J = 5.9 Hz), 6.70-6.75 (1H, m), 6.87 (1H, d, J = 8.4 Hz), 7.22 (1H, s), 7.37-7.52 (8H, m).
実施例 5
(Ε)-3-[1-[(4' -クロロ [1, 1' -ビフエニル] -4 -ィル)力ルポニル] -1, 2, 3, 4_テ トラヒドロ- 6 -キノリニル]- Ν, Ν-ジメチル- 2 -プロペン -卜ァミン
実施例 4で得た 3- [1- [ (4, _クロ口 [1 , 1 ' -ビフエニル] -4-ィル)力ルポ二 ル]- 1,2, 3, 4 -テトラヒドロ- 6 -キノリニル] - 3 -ヒドロキシ -Ν, Ν-ジメチル- 1 - プロパンァミン(0.1 g) の酢酸(1 mL)溶液に濃硫酸 (4滴) を加え、 50- 55°C で 3時間攪拌した。 溶媒を減圧下留去した後、 2規定水酸化ナトリウム水溶
液を加えアルカリ性にした後、 酢酸ェチルで抽出した。抽出液を水で洗浄し、 無水硫酸マグネシウムで乾燥後、 溶媒を減圧下留去した。 得られた残査をァ ルミナカラムクロマトグラフィー (展開溶媒;酢酸ェチル) により精製して、 ジェチルエーテルから結晶化して表題化合物 (75 mg) を mp 162- 164°Cの無 色粉末として得た。
Ή NMR (CDC13) δ 2.02-2.13 (2Η, m), 2.26 (6H, s), 2.85 ('2Η, t, J = 6.6 Hz), 3.04 (2H, d, J = 6.4 Hz), 3.93 (2H, t, J = 6.4 Hz), 6.16 (1H, dt, J = 6.4, 15.9 Hz), 6.40 (1H, d, J = 15.9 Hz), 6.68 (1H, d, J = 8.5 Hz), 6.91 (1H, d, J = 8.5 Hz), 7.19 (1H, s), 7.37-7.53 (8H, m).
元素分析値 C27H27C1N20として ■
計算値: C, 75.25; H, 6.31; , 6.50.
実験値: C, 74.90; H, 6.52; N, 6.35.
実施例 6
1 _ [ (4' -クロ口 [1 , Γ -ビフェニル] -4-ィル)力ルポニル] -6- [ (E) -3-ピぺリジ ノ -1-プロぺニル ]-1, 2, 3, 4-テ卜ラヒドロキノリン
参考例 1 1で得た(E) - 1 - [1- [ (4' -クロ口 [1, Γ -ビフエニル] -4 -ィル)力ル ポニル] - 1, 2, 3, 4-テトラヒドロ- 6-キノリ二ル]- 3-ピペリジノ -2-プロペン - 1 -オンを用いて、 実施例 4および実施例 5と同様の操作を順次行うことによ り、 表題化合物を mp U1-143°Cの無色結晶として得た。
Ή NMR (CDC13) δ 1.42-1.65 (6Η, m), 2.00-2.09 (2H, m), 2.35-2.48 (4H, m), 2.84 (2H, t, J = 6.4 Hz), 3.08 (2H, d, J = 6.7 Hz), 3.92 (2H, t, J = 6.4 Hz), 6.20 (1H, dt, J = 6.7, 15.6 Hz), 6.38 (1H, d, J = 15.6 Hz), 6.66 (1H, d, J = 8.5 Hz), 6.89 (1H, d, 8.5 Hz), 7.18 (1H, s), 7.38-7.52 (8H, m).
元素分析値 C3。H31C1N20として
計算値: C, 76.50; H, 6.63; N, 5.95.
実験値: C, 76.40; H, 6.64; N, 5.65.
実施例 7
(E)- 3- [卜 [([1,1'-ビフエ二ル]- 4-ィル)力ルポニル] - 2,3-ジヒドロ-111-ィン ドール- 5-ィル] -N,N-ジメチル- 2-プロペン- 1-ァミン '
参考例 13で得た (E)-3- [2, 3 -ジヒドロ- 1H -ィンドール- 5 -ィル]- N, N -ジメ チル -2-プロペン- 1-アミンを用いて、 実施例 2と同様の操作を行うことによ り、 表題化合物を mp 174_176°Cの無色結晶として得た。
Ή NMR (CDC13) δ 2.27 (6Η, s), 3.06 (2H, d, . J = 6.0 Hz), 3.13 (2H, t, J = 8.1 Hz), 4.15 (2H, br), 6.11-6.23 (lH,m), 6.46 (1H, d, J = 15.9 Hz), 7.06-7.28 (2H, m), 7.36-7.51 (3H, m), 7.61-7.70 (7H, m).
元素分析値 C26H26N20として
計算値: C, 81.64; H, 6.85; N, 7.32.
実験値: C, 81.31; H, 6.84; N, 7.29.
実施例 8
(E) - 3 - [1— [ (4' -クロ口 [1, -ビフエニル] -4 -ィル)力ルポニル] -2, 3 -ジヒド ロ- 1H-ィンドール- 5-ィル] -N, N-ジメチル -2-プロペン- 1-ァミン
参考例 13で得た (E) - 3 - [2, 3-ジヒドロ- 1H-ィンドール- 5 -ィル] - N, N -ジメ チル -2-プロペン- 1 -ァミンを用いて、 実施例 2と同様の操作を行うことによ
り、 表題化合物を mp 208- 21 Cの無色結晶として得た。
JH NMR (CDC13) δ 1.11 (6H, s), 3.06 (2H, d, J = 6.6 Hz), 3.12 (2H, t,
J = 8.2 Hz) , 4.14 (2H, br), 6.12-6.23 (1H, m), 6.46 (1H, d, J = 15.3 Hz),
7.06-7.28 (2H, m), 7.44 (2H, d, J = 6.6 Hz), 7.56 (2H, d, い 6.6 Hz),
7.63 (5H, s).
実施例 9
(E)_3- [1- [4- [(4-メトキシベンジル)ォキシ]ベンゾィル ]-2, 3-ジヒドロ- 1H- ィンドール- 5-ィル] -N, N-ジメチル- 2-プロペン- 1-ァミン
参考例 1 3で得た (E) -3- [2, 3-ジヒド口- 1H-ィンドール- 5-ィル] - N, N-ジメ チル -2-プロペン- 1-アミンを用いて、 実施例 2と同様の操作を行うことによ り、 表題化合物を mp 164- 166°Cの無色結晶として得た。
'HNMR (CDC13) δ 2.27 (6Η, s), 3.04-3.12 (4H, m), 3.83 (3H, s), 4.12 (2H, t,' J = 8.2 Hz), 5.04 (2H, s), 6.10-6.21 (1H, m), 6.45 (1H, d, J = 15.9 Hz), 6.90-7.30 (7H, m), 7.37 (2H, d, J = 8.7 Hz), 7.54 (2H, d, J = 8.4 Hz).
元素分析値 C28¾。N203として
計算値: C, 75.99; H, 6.83; N, 6.33.
実験値: C, 75.77; H, 6.86; N, 6.21.
実施例 1 0
1-[卜[(4'-クロロ[1,1'-ビフェニル]-4-ィル)カルポニル]-1,2,3,4-テトラ ヒドロ- 6 -キノリニル] -4- (ジメチルァミノ) - 1-ブタノン
参考例 14で得た卜(1, 2, 3, 4 -テトラヒドロ- 6 -キノリニル) -4- (ジメチル ァミノ)-卜ブ夕ノンを用いて、 参考例 5と同様の操作を行うことにより、 表 題化合物を油状物として得た。
'H MR (CDC13) δ 1.84-1.96 (2Η, m), 2.04-2.13 (2H, m), 2.21 (6H, s), 2.33 (2H, t, J = 7.1 Hz), 2.90-3.20 (4H, m), 3.95 (2H, t, J = 6.4 Hz), 6.85 (1H, d, J = 8.6 Hz), 7.38-7.62 (9H, m), 7.82 (1H, s).
実施例 11
(E) - 4- [卜 [ (4' _クロ口 [1 , Γ -ビフエニル] -4 -ィル)力ルポニル] -1,2,3, 4 -テ トラヒドロ- 6-キノリニル] - N,N-ジメチル- 3 -ブテン - 1-ァミン
実施例 10で得た 1- [1 - [ (4, -クロ口 [1, -ビフェニル] - 4 -ィル)力ルポ二 ル]- 1,2,3, 4-テトラヒドロ- 6 -キノリニル] - 4- (ジメチルァミノ) -1-プ夕ノン を用いて、 実施例 4および実施例 5と同様の操作を順次行うことにより、 表 題化合物を即 142- 144°Cの無色結晶として得た。
'HNMR (CDC13) δ 2.01-2.11 (2Η, m), 2.25 (6H, s), 2.28-2.43 (4H, m), 2.84 (2H, t, J = 6.6 Hz), 3.92 (2H, t, J = 6.4 Hz), 6.06-6.18 (1H, m), 6.32 (1H, d, J = 15.6 Hz), 6.63 (1H, brd, J = 8.1 Hz), 6.86 (1H, d, J = 8.4 Hz), 7.15 (1H, s), 7.37-7.52 (8H, m).
実施例 12
4 - [4- (4-クロ口フエニル) -卜ピペリジニル] -4-ォキソ-卜 [2- (トリフルォ口
リニル] -1-ブタノン
参考例 15で得た 4 -ォキソ -4- [2- (トリフルォロアセチル )-1, 2, 3, 4—テト ラヒドロ- 7 -イソキノリニル]ブタン酸(1.0 g, 3.04 mol), 4 -クロ口フエ二 ルピペリジン塩酸塩 (708 mg, 3.05讓 ol)とトリエチルァミン (0.85ml, 6.1 mmol)のジメチルホルムアミド (8ml) 溶液を室温で 20分撹拌した後、 0°Cに 冷却した。 シァノりん酸ジェチル (0.463 ml, 3.05 mmol)を反応混合物に加え、 0°Cで 30分撹拌した後、 水に注ぎ 酢酸ェチルで抽出した。 抽出液を飽和食 塩水で洗浄し、 無水硫酸マグネシウムで乾燥した。 溶媒を減圧留去後、 シリ 力ゲルカラムクロマトグラフィー (展開溶媒;酢酸ェチル) で精製して、 表 題化合物 1.1 gを無色結晶として得た。
Ή-NMR (CDC13) δ: 1.57 (2Η, m), 1.90 (2H, m), 2.68 (2H, m), 2.85 (2H, m), 3.00 (2H, m), 3.13 (1H, m), 3.33 (2H, m), 3.88 (2H, m), 4.13 (1H, m), 4.74 (1H, m), 4.81 (2H, m), 7.31-7.12 (5H„ m), 7.93-7.79 (2H, m). 融点: 142 °C (dec.) (結晶化溶媒: エタノール-ジイソプロピルエーテル) 実施例 13
4- [4- (4-/7ロロフエ二ル)- 1-ピペリジニル ]-4一ォキソ - 1 -(1, 2, 3, 4—テトラ ヒドロー 7-イソキノリニル) -卜ブ夕ノン
実施例 12で得た 4- [4- (4-ク口口フエニル) -1-ピぺリジニル] - 4-ォキソ- 1 - [2- (トリフルォロアセチル) - 1,2, 3, 4-テトラヒドロ- 7-ィソキノリニル] - 卜ブ夕ノン (l.l g, 2. Π匪 ol)と炭酸カリウム (900 mg, 6.5匪 ol) の水 (10 ml) 一メタノール (40ml) 混合溶液を、 室温で 2時間撹拌した後、 酢酸ェチ ルで抽出した。 抽出液を飽和食塩水で洗浄し、 無水硫酸マグネシウムで乾燥
した。 溶媒を減圧下留去して、 表題化合物 810 mg'を無色粉末として得た。 'H-NMR (CDC13) δ: 1.60 (2Η, m), 1.89 (2H, m), 2.91-2.61 (6H, m), 3.19 (2H, m), 3.33 (2H, t, J = 6.6 Hz), 3.70 (2H, q, J = 6.9 Hz), 4.10 (2H, s), 4.14 (IH, d, J = 13.2 Hz), 4.75 (IH, d, J = 13.2 Hz), 7.28-7.12 (5H, m), 7.70 (IH, s), 7.80 (IH, d, J = 8.1 Hz).
融点: 121- 122 °C (結晶化溶媒: エタノール-ジイソプロピルエーテル) 実施例 14
4- [4- (4-クロロフェニル) -1-ピぺリジニル] -4-ォキソ -1- [3- (トリフルォロ ァセチル)- 2, 3, 4, 5-テトラ.ヒド口- 1H - 3 -ベンズァゼピン- 7-ィル] -卜ブタノ ン '
参考例 16で得た 4-ォキソ -4- [3- (トリフルォロアセチル) - 2, 3, 4, 5-テト ラヒドロ- 1H- 3-ベンズァゼピン- 7-ィル]ブタン酸を用いて、 実施例 12と同 様の操作を行うことにより、 表題化合物を無色粉末として得た。
Ή-NMR (CDC13) δ: 1.45 - 2.00 (4Η, m), 2.55-2.90 (4H, m), 2.97-3.28 (5H, m), 3.34 (2H, t, J=6.4Hz), 3.64-3.84 (4H, m), 4.04-4.21 (1H, m), 4.68-4.84 (IH, m), 7.14 (2H, d, J=8.4Hz), 7.20-7.34 (3H, m), 7.80-7.90 (2H, m). 元素分析値 C27H28C1F3N203として .
計算値: C, 62.25; H, 5.42; N, 5.38.
実験値: C, 62.23; H, 5.44; N, 5.29.
融点: 131- 132 °C (結晶化溶媒: イソプロパノール-ジイソプロピルエーテ ル)
実施例 15
4一 [
4— (4-ク口口フエニル) -1-ピペリジニル ]-4-ォキソ -卜(2, 3, 4, 5-テトラヒ ドロ- 1H- 3 -ベンズァゼピン- 7 -ィル) -卜ブ夕ノン
実施例 1· 4で得た 4- [4- (4-クロ口フエ二ル)- 1-ピぺリジニル] - 4 -ォキソ- 1 - [3- (トリフルォロアセチル )-2, 3, 4, 5-テトラヒドロ- 1H- 3 -ベンズァゼピン -7 -ィル] -卜ブタノンを用いて、実施例 13と同様の操作を行うことにより、 表題化合物を無色粉末として得た。
Ή-NMR (CDClg) δ: 1.47-2.00 (4Η, m), 2.57-2.88 (5H, m), 2.98 (8H, br), 3.07-3.27 (1H, m), 3.50 (2H, t, J=6.6Hz), 4.05-4.21 (1H, in), 4.72-4.84 (1H, m), 7.10-7.34 (5H, m), 7.74-7.83 (2H, m).
元素分析値 C25H29C 1N202として
計算値: C, 70.66; H, 6.88; N, 6.59.
実験値: C, 70.22; H, 7.13; N, 6.51.
融点: 148-149 °C (結晶化溶媒: エタノール)
実施例 16
4- [4- (4-クロ口フエニル) - 1 -ピペリジニル] -4 -ォキソ -1- (3-メチル-
2,3,4, 5-テトラヒドロ- 1H- 3 -ベンズァゼピン- 7 -ィル )-1-ブタノン
実施例 15で得た 4_ [4- (4-クロ口フエ二ル)- 1-ピぺリジニル] -4-ォキソ - 1-(2, 3, 4, 5 -テトラヒドロ- 1H-3-ベンズァゼピン - 7-ィル) -1 -ブタノン (0.3g, 0.70腿 ol)、ホルムアルデヒド (0.086ml, 1.06画 1) およびギ酸 (0.9ml)の 混合物を 100°Cで 4時間加熱した後、水に注ぎ、 8規定水酸化ナトリゥム水溶 液を加えアルカリ性とし、 酢酸ェチルで抽出した。 抽出液を水、 次いで飽和 食塩水で洗浄後、 無水硫酸マグネシウムで乾燥した。 溶媒を減圧下留去した 後、 アルミナカラムクロマトグラフィ一 (展開溶媒;酢酸ェチル—メタノー ル =10 : 1) で精製して、 表題化合物 0.15gを無色粉末として得た。
'Η「匪 R (CDC 13) δ 1.47-2.00 (4H, m), 2.38 (3H, s), 2.47-2.88 (8H, m), 2.95-3.06 (4H, m), 3.08-3.28 (1H, m), 3.35 (2H, t, J=6.8Hz), 4.07-4.21 (1H, m), 4.71-4.86 (1H, m), 7.08-7.3 (5H, m), 7.75-7.85 (2H, m). 元素分析値 C26H31C1N202として
計算値: C, 71.14; H, 7.12; N, 6.38.
実験値: C, 70.92; H, 7.35; N, 6.41.
融点: 143- 145 °C (結晶化溶媒: 酢酸ェチル-ジェチルエーテル) 実施例 17
4 - [4- (4 -クロ口フエニル) -1 -ピぺリジニル] - 1_ (3 -ェチル _2, 3, 4, 5-テ卜ラヒ ドロ- 1H- 3-ベンズァゼピン- 7-ィル) -4-ォキソ -卜ブタノン
実施例 15で得た 4- [4- (4-ク口口フエ二ル)- 1-ピペリジニル ]-4-ォキソ - 1 -(2, 3, 4, 5 -テトラヒド口- 1H - 3 -べンズァゼピン- 7 -ィル) -卜ブ夕ノン (200 ig, 0.47 mmol), ョ一ドエタン (0.0376 ml, 0.47 mmol)と炭酸カリウム (138 mg, 1.0腿 ol) のァセトニトリル (5 ml) 溶液を、 室温で 12時間撹拌 した後、.水に注ぎ、 酢酸ェチルで抽出した。 抽出液を飽和食塩水で洗浄し、 無水硫酸マグネシウムで乾燥した。 溶媒を減圧下留去し、 アルミナシリカゲ ルカラムクロマトグラフィー (展開溶 ;酢酸ェチル) で精製して、 表題化 合物 101 mgを無色粉末として得た。
Ή-NMR (CDC13) (5: 1.10 (3H, t, J = 7.0 Hz), 1.62 (2H, m), 1.94 (2H, m), 2.72-2.52 (8H, m), 2.79 (2H, t, J = 6.4 Hz), 2.97 (4H, m), 3.23 (1H, m), 3.35 (2H, t, J = 6.6 Hz), 4.13 (1H, d, J = 15.6 Hz), 4.76 (1H, d, J = 12 Hz), 7.35-7.11 (5H, m), 7.79 (2H, m).
融点: 156- 157 °C (結晶化溶媒: エタノール-ジイソプロピルエーテル) 実施例 18
4- [4- (4-クロロフエニル) -卜ピペリジニル ]-4-ォキソ -卜(3-プロピル -
2, 3, 4, 5 -テトラヒド口- 1H - 3-ベンズァゼピン - 7-ィル )_1-ブ夕ノン
実施例 15で得た 4- [4- (4-ク口口フエニル) -卜ピぺリジニル] -4-ォキソ- 1- (2, 3, 4, 5-テトラヒド口 -1H - 3_ベンズァゼピン -7 -ィル) - 1-ブ夕ノンを用い て、 実施例 17と同様の操作を行うことにより、 表題化合物を無色粉末とし て得た。
Ή-NMR (CDC13) 6 0.91 (3H, t, J = 7.2 Hz), 1.62 (4H, m), 1.89 (2H, m), 2.45 (2H, i, J = 8.0 Hz), 2.72-2.66 (6H, m), 2.79 (2H, t, J = β.4 Hz), 2.97 (4H, m), 3.23 (1H, m), 3.35 (2H, t, J = 6.6 Hz), 4.13 (1H, d, J = 15.6 Hz), 4.76 (1H, d, J = 12 Hz), 7.35-7.11 (5H, m), 7.79 (2H, m). 融点: 151- 152 。C (結晶化溶媒: エタノール-ジイソプロピルエーテル) 実施例 1 9 .
卜(3-ベンジル- 2, 3, 4, 5-テトラヒドロ- 1H- 3 -ベンズァゼピン- 7-ィル) - 4- [4 -
(4-ク口口フエニル) -1 -ピぺリジニル ]-4-ォキソ -卜ブ夕ノン
実施例 15で得た 4- [4- (4-クロ口フエ二ル)-卜ピペリジニル ]-4-ォキソ- 1-(2,3, 4, 5-テトラヒドロ- 1H - 3-ベンズァゼピン- 7-ィル) -卜プ夕ノンを用い て、 実施例 17と同様の操作を行うことにより、 表題化合物を無色粉末とし て得た。
'H-NMR (CDC13) δ: 1.64 (2Η, m), 1.89 (2H, m), 2.72-2.65 (6H, m), 2.85 (2H, t, J = 6.4 Hz), 2.97 (4H, m), 3.23 (1H, m), 3.34 (2H, t, J = 6.6 Hz), 3.64 (2H, s), 4.13 (1H, d, J = 15.6 Hz), 4.76 (1H, d, J = 12 Hz), 7.35-7.11 (10H, m), 7.79 (2H, m).
融点: 133-134 °C (結晶化溶媒: エタノール-ジイソプロピルエーテル)
実施例 20
1 -(3-ベンゾィル- 2, 3, 4, 5-テトラヒド口- 1H-3-ベンズァゼピン- 7-ィル) - 4-
[4 -(4-ク口口フエ二ル)-卜ピぺリジニル] - 4-ォキソ -1-ブ夕ノン
実施例 15で得た 4- [4- (4-クロ口フエニル) -卜ピペリジニル ]-4-ォキソ - 1 -(2, 3, 4, 5 -テトラヒド口- 1H- 3 -ベンズァゼピン- 7-ィル) -1 -ブ夕ノンを用い て、 実施例 17と同様の操作を行うことにより、 表題化合物を無色粉末とし て得た。 ·
Ή-NMR (CDC13) δ: 1.64 (2Η, m), 1.89 (2H, m), 3.17-2.59 (9H, m), 3.34 (2H, t, J - 6.6 Hz), 3.53 (2H, m), 3.87 (2H, m), 4.13 (1H, d, J = 15.6 Hz), 4.76 (1H, d, J = 12 Hz), 7.35-7.11 (10H, m), 7.79 (2H, m).
融点: 158- 160 °C (結晶化溶媒: エタノール -ジイソプロピルエーテル) 実施例 21 '
4- [4- (4-クロ口フエ二ル)-卜ピペリジニル ] -4-ォキソ -1- [3- (2-ォキソ -2 -フ ェニルェチル ) -2, 3, 4, 5-テトラヒド口- 1H- 3-ベンズァゼピン- 7-ィル] -1-ブ , 夕ノン
. 実施例 1 5で得た 4- [4- (4-クロ口フエニル) -卜ピペリジニル ]-4-ォキソ - 1-(2, 3, 4, 5-テトラヒド口- 1H-3-ベンズァゼピン- 7-ィル) - 1-ブ夕ノンを用い て、 実施例 17と同様の操作を行うことにより、 表題化合物を無色粉末とし て得た。 ·
Ή-N R (CDC13) 6: 1.64 (2H, ra), 1.89 (2H, m), 2.86-2.58 (8H, m), 3.03 (4H, ni), 3.17 (1H, m), 3.35 (2H, t, J = 6.6 Hz), 3.96 (2H, s), 4.13 (1H, d, J = 15.6 Hz), 4.76 (1H, d, J = 12 Hz), 7.31-7.11 (5H, m), 7.55-7.43
(3H, m), 7.79 (2H, m), 8.05 (2H, m).
融点: 108- 109 °C (結晶化溶媒: エタノール-ジイソプロピルエーテル) 実施例 22
1 -(3 -ァセチル -2, 3, 4, 5-テトラヒドロ- 1H-3-ベンズァゼピン- 7-ィル) -4 - [4-
(4 -クロ口フエニル) -卜ピぺリジニル] -4-ォキソ -卜ブタノン
実施例 15で得た 4- [4- (4-ク口口フエニル) -1-ピぺリジニル] -4-ォキソ - 1-(2, 3, 4, 5-テトラヒドロ- 1H- 3-ベンズァゼピン- 7 -ィル) -卜ブ夕ノンを用い て、 実施例 17と同様の操作を行うことにより、 表題化合物を無色粉末とし て得た。
Ή-NMR (CDC13) δ: 1.64 (2Η, m), 1.89 (2H, m), 2.66 (3H, s), 2.58 (4H, m), 2.87 (2H, t, J = 6.6 Hz), 3.11 (4H, m), 3.17 (1H, m), 3.34 (2H, t, J = 6.6 Hz), 3.76-3.58 (4H, m), 4.13 (1H, d, J = 15.6 Hz), 4.73 (1H, d, J = 12 Hz), 7.31-7.11 (5H, m), 7.81 (2H, m).
融点: 110- 112 °C (結晶化溶媒: エタノール-ジイソプロピルエーテル) 実施例 23
4- [4- (4-クロ口フエ二ル)-卜ピぺリジニル] -4-ォキソ -1- [3- (2-ォキソプロ ピル) -2, 3, 4, 5-テトラヒド口- 1H- 3-ベンズァゼピン- 7-ィル] -卜ブ夕ノン
実施例 15で得た 4- [4- (4-クロ口フエニル) - 1-ピぺリジニル] -4-ォキソ - 1 -(2, 3, 4, 5 -テ卜ラヒド口- 1H- 3-ベンズァゼピン- 7-ィル) -卜ブ夕ノンを用い て、 実施例 17と同様の操作を行うことにより、 表題化合物を無色粉末とし て得た。
Ή-NMR (CDC13) δ: 1.64 (2Η, m), 1.89 (2H, m), 2.22 (3H, s), 2.67ズ 4H,
m), 2.87 (2H, t, J = 6.6 Hz), 3.00 (4H, m), 3.17 (1H, m), 3.78-3.32 (4H, m), 4.13 (1H, d, J = 15.6 Hz), 4.73 (1H, d, J = 12 Hz), 7.31-7.11 (5H, m), 7.81 (2H, m).
融点: 119- 120 °C (結晶化溶媒: エタノール-ジイソプロピルェ一テル) 実施例 24
4 - [4- (4-クロ口フエ二ル)-卜ピペリジニル ] -4-ォキソ -卜 [3- [2- (1 H-ピロ一. ル- 1-ィル)ェチル] -2, 3, 4, 5 -テトラヒド口- 1H- 3 -ベンズァゼピンー 7 -ィル] -
実施例 15で得た 4- [4- (4-クロ口フエニル) -卜ピぺリジニル] -4-ォキソ - 卜(2, 3, 4, 5 -テトラヒドロ- m- 3-ベンズァゼピン- 7-ィル) -卜ブタノンを用い て、 実施例 17と同様の操作を行うことにより、 表題化合物を無色粉末とし て得た。
Ή-NMR (CDC13) (5: 1.64 (2H, ) , 1.89 (2H, m), 2.95-2.59 (14H, m), 3.17 (1H, m), 3.34 (2H, t, J = 6.2 Hz), 4.18-4.00 (3H, m), 4.75 (1H, m), 6.15 (2H, m), 6.70 (2H, i), 7.31-7.11 (5H, m), 7.81 (2H, m).
融点: 96- 97 °C (結晶化溶媒: エタノール-ジイソプロピルエーテル) 実施例 25
4 - [4- (4-クロ口フエニル) -1 -ピペリジニル] -1-[3- (2-メチルベンジル) - 2, 3, 4, 5-テトラヒドロ- 1H- 3-ベンズァゼピン- 7-ィル] -4-ォキソ -1-ブタノン
実施例 15で得た 4- [4- (4-クロ口フエニル) -1 -ピペリジニル] -4-ォキソ- 1-(2,3,4, 5-テトラヒドロ- 1H- 3-ベンズァゼピン- 7-ィル) -卜ブ夕ノンを用い て、 実施例 1 7と同様の操作を行うことにより、 表題化合物を無色粉末とし
て得た。
一匪 R (CDC13) <5: 1.64 (2H, m), 1.89 (2H, m), 2.40 (3H, s), 2.72-2.65 (6H, m)., 2.82 (2H, t, J = 6.4 Hz), 2.94 (4H, m), 3.23 (1H, m), 3.35 (2H, t, J - 6.6 Hz), 3.54 (2H, s), 4.13 (1H, d, J = 15.6 Hz), 4.76 (1H, d, J = 12 Hz), 7.35-7.11 (9H, m), 7.79 (2H, m).
融点: 108-109 °C (結晶化溶媒: エタノール-ジイソプロピルエーテル) 実施例 26
4 - [4- (4-ク口口フエニル) - 1-ピぺリジニル] -1- [3- (3-メチルベンジル) -
2, 3, 4, 5-テトラヒドロ- 1H - 3-ベンズァゼピン- 7-ィル] - 4-ォキソ -1-ブ夕ノン
実施例 15で得た 4- [4- (4-クロ口フエ: ±ル)- 1-ピぺリジニル] -4-ォキソ - 1-(2, 3, 4, 5-テトラヒドロ- 1H- 3-ベンズァゼピン- 7-ィル) -1-ブタノンを用い て、 実施例 17と同様の操作を行うことにより、 表題化合物を無色粉末とし て得た。
Ή-NMR (CDC13) 6 1.64 (2H, m), 1.89 (2H, m), 2.36 (3H, s), 2.72-2.65 (6H, m), 2.82 (2H, t, J = 6.4 Hz), 2.94 (4H, m), 3.23 (1H, m), 3.35 (2H, t, J = 6.6 Hz), 3.60 (2H, s), 4.13 (1H, d, J = 15.6 Hz), 4.76 (1H, d, J = 12 Hz), 7.35-7.11 (9H, m), 7.79 (2H, 1).
融点: 127- 128で (結晶化溶媒: エタノール-ジィソプロピルエーテル) 実施例 27
4- [4- (4 -ク口口フエニル)ピぺリジン -トイル] -1- [3- (4-メチルベンジル) - 2, 3, 4, 5-テトラヒドロ- 1H-3 -ベンズァゼピン- 7-ィル] -4-ォキソブ夕ン- 1 -ォ ン
実施例 15で得た 4- [4- (4-ク口口フエニル) -卜ピぺリジニル] - 4-ォキソ- 1 -(2, 3, 4, 5 -テトラヒド口- 1H-3-ベンズァゼピン- 7-ィル)- 1-ブ夕ノンを用い て、 実施例 17と同様の操作を行うことにより、 表題化合物を無色粉末とし て得た。
'H-NMR (CDC13) δ 1.63 (2Η, ); 1.88 (2Η, m), 2.35 (3H, s), 2.64 (6H, m), 2.78 (2H, t, J = 6.4 Hz),, 2.95 (4H, m), 3.23 (1H, m), 3.34 (2H, t, J = 6.6 Hz), 3.60 (2H, s), 4.13 (1H, i), .76 (1H, m), 7.35-7.11 (9H, m), 7.79 (2H, m).
融点: 137- 138 °C (結晶化溶媒: エタノール-ジイソプロピルエーテル) 実施例 28
1 -(3-ァリル- 2, 3, 4, 5-テトラヒドロ- 1H-3-ベンズァゼピン- 7-ィル) - 4 - [4-
(4 -クロロフエニル)ピペリジン- 1-ィル] -4-ォキソブタン- 1-オン
実施例 15で得た 4- [4- (4-ク口口フエニル) -卜ピぺリジニル] -4-ォキソ - 1-(2, 3, 4, 5-テトラヒド口- 1H- 3-ベンズァゼピン- 7-ィル)-卜ブ夕ノンを用い て、 実施例 17と同様の操作を行うことにより、 表題化合物を無色粉末とし て得た。
'H-NMR (CDC13) δ: 1.63 (2Η, m), 1.88 (2H, m), 2.65 (7H, m), 2.78 (2H, t, J = 6.4 Hz), 2.97 (4H, m), 3.23 (2H, m), 3.35 (2H, t, J = 6.6 Hz), 4.13 (1H, m), 4.76 (1H, m), 5.23-5.15 (2H, m), 5.90 (1H, in), 7.31-7.11 (5H, m), 7.79 (2H, m).
融点: 136- 137 °C (結晶化溶媒: エタノール-ジイソプロピルエーテル) 実施例 2.9
4- [4- (4-ク口口フエニル)ピぺリジン-卜ィル] -4-ォキソ -卜(2-プロピニル- 2, 3, 4, 5-テトラヒド口- 1H- 3-ベンズァゼピン -7-ィル)ブ夕ン -1-オン
実施例 15で得た 4- [4- (4-ク口口フエニル) -1-ピぺリジニル] -4-ォキソ - 1-(2, 3, 4, 5-テトラヒドロ- 1H- 3-ベンズァゼピン- 7-ィル) -卜ブ夕ノンを用い て、 実施例 17と同様の操作を行うことにより、 表題化合物を無色粉末とし て得た。
Ή-NMR (CDC13) δ: 1.63 (2Η, m), 1.88 (2H, ), 2.21 (IH, s), 3.43-2.58 (15H, m), 4.13 (2H, m), 4.76 (IH, m), 5.07 (IH, m), 5.84 (IH, m), 7.31-7.11 (5H, m), 7.79 (2H, m).
融点: 132- 134 (結晶化溶媒: エタノール-ジイソプロピルエーテル) 実施例 30
4- [4- (4-ク口口フエニル)ピぺリジン-トイル] -1- (3 -ィソプロピル _2, 3, 4, 5 - テトラヒドロ- 1H- 3-ベンズァゼピン- 7-ィル) -4-ォキソブタン-卜オン
実施例 15で得た 4- [4- (4-クロ口フエ二ル)- 1-ピぺリジニル] -4-ォキソ- 1-(2,3,4, 5-テトラヒドロ- 1H- 3-ベンズァゼピン- 7-イリレ)-卜ブ夕ノンを用い て、 実施例 17と同様の操作を行うことにより、 表題化合物を無色粉末とし て得た。
Ή-NMR (CDC13) δ: 1.00 (6Η, d, J = 6.6 Hz), 1.62 (4H, m), 1.89 (2H, m), 2.64 (7H, i), 2.82 (2H, t, J = 6.4 Hz), 2.95 (4H, m), 3.23 (IH, m), 3.35 (2H, t, J = 6.6 Hz), 4.13 (IH, m), 4.76 (IH, m), 7.35-7.11 (5H, m), 7.79 (2H, m).
融点: 139- 140 (結晶化溶媒: エタノール-ジイソプロピルェ一テル) 実施例 31·
4 -ォキソ -4- (フエニル-卜ピペリジニル )-1- [3- (トリフルォロアセチル) -
2, 3, 4, 5 -テトラヒドロ- 1Η - 3-ベンズァゼピン - 7 -ィル] -卜ブ夕ノン
参考例 16で得た 4 -ォキソ -4- [3- (トリフルォロアセチル )-2, 3, 4, 5-テト ラヒドロ- 1H- 3-ベンズァゼピン- 7-ィル]ブタン酸を用いて、 実施例 12と同 様の操作を行うことにより、 表題化合物を無色粉末として得た。
Ή-NMR (CDC13) δ: 1.48-1.78 (2Η, m), 1.82-2.00 (2H, m), 2.60-2.88 (4H, m), 2.98-3.10 (4H, m), 3.13-3.26 (1H, m), 3.34 (2H, t, J=6.5Hz), 3.67-3.83 (4H, m), 4.07-4.18 (1H, m), 4.72-4.82 (1H, m), 7.16-7.37 (6H, m), 7.80-7.90 (2H, m).
元素分析値 C27H29F3N203として
計算値: C, 66.65; H, 6.01; N, 5.76.
実験値: C, 66.45; H, 6.09; N, 5.56. .
融点: 132- 133 °C (結晶化溶媒: イソプロパノール)
実施例 32
4-ォキソ -4- (フエニル-卜ピペリジニル) - 1- (2, 3, 4, 5 -テ卜ラヒド口- 1H- 3_ベ ンズァゼピン- 7-ィル) -卜ブ夕ノン
実施例 31で得た 4-ォキソ -4- (フエニル- 1-ピペリジニル) -卜 [3- (ドリフ ルォロアセチル) - 2, 3, 4, 5-テトラヒドロ- 1H- 3-ベンズァゼピン- 7-ィル] -卜 ブ夕ノンを用いて、 実施例 13と同様の操作を行うことにより、 表題化合物 を無色粉末として得た。
—固 R (CDC13) δ: 1.54-2.00 (5Η, m), 2.60-2.87 (4H, m), 2.97 (8H, br), 3.12-3.24 (IH, m), 3.35 (2H, t, J=6.7Hz), 4.08-4.20 (IH, m), 4.73-4.83
(1H, m), 7.16-7.37 (6H, m), 7.77-7.82 (2H, m).
元素分析値 C25 。N202として
計算値: C, 76.89; H, 7.74; N, 7.17.
実験値: C, 76.44; H, 7.68; N, 7.02.
融点: 114 °C (結晶化溶媒: ィソプロパノ一ル-ジィソプロピルエーテル) 実施例 33
卜(3-ァセチル- 2, 3, 4, 5-テトラヒド口- 1H-3-ベンズァゼピン- 7-ィル) -4- [4-
(4 -クロ口フエニル) -卜ピぺリジニル] - 1-ブタノン
1) 3-ァセチル- 2, 3, 4, 5 -テトラヒドロ- 1H- 3-ベンズァゼピン(2 g, 10.5 mmol)と 4-クロロブチリルクロリド (1.56 g, 11 mmol) のニトロェタン(5 ml) 混合液に、 室温で塩化アルミニウム(2.9 g, 21.7膽 ol)を少量ずつ加え、 室 温で 2時間撹拌した。 反応液を氷水に注ぎ、 酢酸ェチルで抽出し、 飽和食塩 水で洗浄し、 無水硫酸マグネシウムで乾燥した。 溶媒を減圧留去して、 1- (3- ァセチル- 2, 3, 4, 5-テトラヒド口- 1H- 3-ベンズァゼピン- 7-ィル) -4-ク口ロ- 1-ブ夕ノン (2.9g)を得た。
2) 上記 1) で得た卜 (3 -ァセチル- 2, 3, 4, 5-テトラヒドロ- 1H - 3 -べンズ ァゼピン- 7-ィル) -4-クロ口- 1-ブタノン (0.75 g, 2.55 mmol), 4 -クロロフ ェニルビペリジン (5.1 g, 5.1 irnnol)とよう化カリウム (0.05 g)のトルエン 混合物 (15ml)を 16時間加熱還流した。 反応液を水に注ぎ、 1規定水酸化ナ トリウム水溶液でアルカリ性とした後、 酢酸ェチルで抽出した。 抽出液を飽 和食塩水で洗浄し、 無水硫酸マグネシウムで乾燥した。 溶媒を減圧留去し、 シリカゲルカラムクロマトグラフィー (展開溶媒;酢酸ェチル:メタノール = 1 : 1) で精製し、 表題化合物 0.6 gを無色粉末として得た。
Ήー醒 R (CDC13) δ 1.54-2.25 (11H, ra), 2.37-2.56 (3H, m), 2.90-3.12 (8H, m), 3.53-3.64 (2H, m), 3.66-3.79 (2H, m), 7.07-7.31 (5H, m), 7.72-7.82
(2H, m).
融点: 131-132 °C (結晶化溶媒: イソプロパノ一ル-ジイソプロピルエーテ ル)
実施例 34
4- [4- (4-ク口口フエニル) -1-ピぺリジニル] - 1 -(2, 3, 4, 5—テトラヒド口- 1H - 3 -べンズァゼピン- 7 -ィル) -1 -ブ夕ノン
実施例 33で得られた 1- (3-ァセチル -2, 3, 4, 5-テトラヒドロ- 1H- 3-ベンズ ァゼピン- 7-ィル) -4- [4- (4-クロ口フエニル) -卜ピぺリジニル] -卜ブタノン を用いて、 参考例 10と同様の操作を行うことにより、 表題化合物を無色粉 末として得た。
Ή-NMR (CDC13, 'フリー塩基) δ: 1.53-2.13 (9Η, ), 2.35-2.55 (3H, m),' 2.90-3.10 (12H, m), 7.07-7.30 (5H, m), 7.68-7.80 (2H, m).
元素分析値 C25H31C1N20 · 2HC1として
計算値: C, 62.05; H, 6.87; N, 5.79.
実験値: C, 61.93; H, 6.78; N, ''5.48.
融点: 243- 247 °C (dec.) (結晶化溶媒: イソプロパノール-ジイソプロピ ルエーテル)
実施例 35
4- [4- (4-ク口口フエニル) -卜ピぺリジニル] -卜(3 -メチル- 2, 3, 4, 5-テトラヒ ドロ- 1H- 3-ベンズァゼピン- 7 -ィル) -1-ブ夕ノン
実施例 34で得られた 4-[4- (4-クロ口フエニル) -1 -ピペリジニル] -卜 (2, 3, 4, 5-テトラヒド口- 1H- 3-ベンズァゼピン- 7-ィル) -卜ブ夕ノンを用いて、
実施例 16と同様の操作を行うことにより、 表題化合物を無色粉末として得 た。
Ή-NMR (CDC13! フリー塩基) δ: 1.62-2.20 (8Η, m), 2.36-2.67 (10H, m) , 2.93-3.15 (8H, in), 7.07-7.30 (5H, m), 7.70-7.80 (2H ,m).
元素分析値 C26H33C1N20 · 2HC1 · 0.5¾0として
計算値: C, 61.60; H, 7; 16; N, 5.53.
実験値: C, 61.73; H, 7.32; N, 5.48.
融点: 248- 252 °C (dec.) (結晶化溶媒: イソプロパノール)
実施例 36
N -プチル- 4 -ォキソ -4 - (2, 3, 4, 5-テトラヒド口- 1H-3 -べンズァゼピン- 7 -ィ ル)ブタンアミド トリフルォロ酢酸塩
参考例 16で得た 4-ォキソ -4- [3- (トリフルォロアセチル )-2, 3, 4, 5-テト ラヒドロ- 1H - 3-ベンズァゼピン- 7 -ィル]ブタン酸 (30.2 ' mg, 0.088 mmol), n -ブチルァミン (5.9mg, 0.08 mol)、カルポジイミド樹脂 (136 mg, 0.12腿 ol, 0.88 minol/g)をジクロロメタン (1 ml)中、 室温で 12時間攪拌した。 反応混 合物をろ過し、 ろ液を濃縮後、 反応混合物にメタノール (500 u 1)と炭酸力 リウム(331 mg, 2.4腿 ol)の水溶液 (0.5 ml)を加え、 室温で 12時間攪拌した。 溶媒を留去後、 分取液体クロマトグラフィー (展開溶媒: 0.1% トリフルォ 口酢酸含有水 /0.1Γ トリフルォロ酢酸含有ァセトニトリル = 90/10〜10/90) で精製して、 表題化合物 10.2 mgを無色粉末として得た。
MS (ESI) (M+l): 303
実施例 37
N -(シク口へキシルメチル) - 4 -ォキソ -4- (2, 3, 4, 5-テトラヒドロ- 1H-3-ベン ズァゼピン- 7-ィル)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして ¾題化合物を得た。
MS (ESI) (M+l) : 343
実施例 3 8
N-シクロプロピル -4-ォキソ _4_ (2, 3, 4, 5 -テトラヒド口- 1H- 3-ベンズァゼピ ン -7-ィル)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (APCI) (M+l): 287
実施例 3 9
N -べンジル -4-ォキソ - 4- (2, 3, 4, 5 -テトラヒド口- 1H- 3 -ベンズァゼピン- 7-ィ ル)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (ESI) (M+l): 337
実施例 4 0
N- (l, 3 -べンゾジォキソール- 5-ィルメチル) - 4-ォキソ -4 -(2, 3, 4, 5 -テトラヒ ドロ- 1H- 3-ベンズァゼピン- 7-ィル)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た c
MS (ESI) (M+l): 381
実施例 4 1
4-ォキソ -N- (2-フエネチル ) -4 -(2, 3, 4, 5-テトラヒドロ- 1H-3-ベンズァゼピ ン -7-ィル)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (ESI) (M+1): 351
実施例 4 2
4-ォキソ -N- (3-フエニルプロピル)- 4- (2, 3, 4, 5 -テトラヒドロ- 1H- 3-ベンズ ァゼピン -7-ィル)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (ESI) (M+1): 365
実施例 4 3
N -べンズヒドリル- 4-ォキソ -4- (2, 3, 4, 5 -テトラヒドロ- 1H- 3-ベンズァゼピ ン -7-ィル)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (ESI) (MID: 413
実施例 4 4
N -(2-メトキシェチル) -4-ォキソ -4- (2, 3, 4, 5-テトラヒドロ- 1H - 3- ゼピン- 7-ィル)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (APCI) (Mil): 305
実施例 4 5
N- [3- (メチルチオ)プロピル] -4 -ォキソ -4- (2, 3, 4, 5-テトラヒドロ- 1H - 3 -べ ンズァゼピン- 7-ィル)ブ夕ンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (ESI) (M+1) : 335
実施例 4 6
4 -ォキソ -4- (2, 3, 4, 5 -テトラヒドロ- 1H-3-ベンズァゼピン- 7-ィル) (テト ラヒドロフラン- 2-ィルメチル)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (APCI) (M+1): 331
実施例 4 7
N- [2- ( 1 H -インドール - 3-ィル)ェチル] -4 -ォキソ- 4- (2, 3, 4, 5-テトラヒドロ - m- 3-ベンズァゼピン- 7-ィル)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た c
MS (ESI) (M+1): 390
実施例 4 8
N -( 1 -ェチルプロピル) -4-ォキソ -4 -(2, 3, 4, 5-テトラヒド口- 1H- 3-ベンズァ ゼピン- 7-ィル)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (ESI) (M+l): 317
実施例 4 9
N- (ter t -ブチル) - 4 -ォキソ -4 - (2, 3, 4, 5 -テトラヒド口- 1H-3-ベンズァゼピン
実施例 3 6と同様にして表題化合物を得た。
MS (ESI) (M+l): 303
実施例 5 0
N- (シクロへキシル )-4-ォキソ -4- (2, 3, 4, 5-テトラヒドロ- 1H-3-ベンズァゼ ピン- 7-ィル)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (ESI) (Mil): 329
実施例 5 1
4 -ォキソ -N-プロプ- 2-ィニル -4 -(2, 3, 4, 5-テトラヒド口- 1H-3-ベンズァゼピ ン- 7-ィル)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (APCI) (M+1): 285
実施例 5 2
4-ォキソ - 4- (2, 3, 4, 5-テトラヒドロ- 1H- 3 -ベンズァゼピン- 7 -ィル) -N - [4- (トリフリレオロメチル)ベンジル]ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (ESI) (M+1): 405
実施例 5 3 ·
N- [2 -(3, 4-ジメトキシフエニル)ェチル ] -4-ォキソ -4- (2, 3, 4, 5 -テトラヒド 口- 1H- 3-ベンズァゼピン- 7-ィル)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (ESI) (M+1): 411
実施例 5 4
N- (3, 3 -ジフエニルプロピル) - 4-ォキソ -4- (2, 3, 4, 5 -テトラヒドロ- 1H-3 -べ ンズァゼピン- 7-ィル)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (ESI) (Mil): 41
実施例 5 5
N- (2, 3 -ジヒドロ- 1H -ィンデン -2-ィル) -4-ォキソ -4- (2, 3, 4, 5-テトラヒドロ
ド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (ESI) (M+1) : 363
実施例 5 6
N- (3 -ィソプロポキシプロピル) - 4-ォキソ -4- (2, 3, 4, 5-テトラヒド P-1H-3- ベンズァゼピン- 7-ィル)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (ESI) (M+1): 347
実施例 5 7
N - (3-7リルメチル) - 4 -ォキソ -4 - (2, 3, 4, 5 -テ卜ラヒドロ- 1H - 3 -べンズァゼ ピン- 7-イ レ)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (ESI) (M+1): 327 ·
実施例 5 8
4 -ォキソ - N- [3- (2-ォキソピロリジン- 1 -ィル)プロピル] -4 -(2, 3, 4, 5 -テ卜ラ ヒドロ- 1H- 3-ベンズァゼピン- 7-ィル)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た(
MS (APCI) (M+l): 372
実施例 5 9
4 -ォキソ - N, N -ジプロピル _4 -(2, 3, 4, 5-テトラヒド口- 1H- 3-ベンズァゼピン-
7 -ィル)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (ESI) (M+l): 331
実施例 6 0
N -メチル -N_ (l-ナフチルメチル) -4 -ォキソ - 4- (2, 3, 4, 5-テトラヒドロ- 1H - 3- ベンズァゼピン- 7-ィル)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (ESI) (M+l): 01
実施例 6 1
N- [2- (3, 4 -ジメトキシフエニル)ェチル] -N -メチル- 4-ォキソ -4- (2, 3, 4, 5 -テ トラヒドロ- 1H-3-ベンズァゼピン- 7-ィル)ブタンアミド トリフルォロ酢酸
実施例 3 6と同様にして表題化合物を得た。
MS (ESI) (Mil): 425
実施例 6 2
N, N -ビス (2-メトキシェチル)- 4-ォキソ -4- (2, 3, 4, 5-テトラヒドロ- 1H - 3-ベ
ンズァゼピン _7-ィル)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (ESI) (Mil): 363
実施例 6 3
4-ォキソ -4-ピペリジン- 1 -ィル- 1- (2, 3, 4, 5-テトラヒドロ- 1H- 3-ベンズァゼ ピン- 7-ィル)ブタン- 1-オン トひフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (ESI) (M+1): 315
実施例 6 4 '
4- (2, 6 -ジメチルモルホリン- 4-ィル) -4-ォキソ -卜(2, 3, 4, 5-テトラヒドロ-
1H - 3-ベンズァゼピン- 7-ィル)ブタン-卜オン トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (ESI) (M+1): 345
実施例 6 5
4- (3, 4-ジヒドロイソキノリン- 2 (1H) -ィル) -4 -ォキソ- 1-(2, 3, 4, 5 -テトラヒ ドロ- 1H- 3-ベンズァゼピン- 7-ィル)ブタン-卜オン トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (ESI) (M+l): 363
実施例 6 6
1 - [4-ォキソ - 4 - (2, 3, 4, 5-テトラヒド口- 1H- 3-ベンズァゼピン -7-ィル)ブタ ノィル]ピぺリジン- 4-カルポキシアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (APCI) (M+l): 358
実施例 6 7
4- [4 - (2-ヒド口キシェチル)ピぺリジン -トイル] - 4-ォキソ -1- (2, 3, 4, 5 -テト ラヒドロ- 1H- 3-ベンズァゼピン- 7-ィル)ブタン-卜オン トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (ESI) (M+l) : 359
実施例 6 8
4 -ォキソ -1- (2, 3, 4, 5-テトラヒドロ- 1H-3-ベンズァゼピン- 7-ィル) -4-チォ モルフオリン -4-ィルブタン-卜オン トリフルォロ酢酸塩
0 r '
実施例 3 6と同様にして表題化合物を得た。 ■
MS (ESI) (M+1): 333
実施例 6 9
4- (4-ベンジルピペリジン-卜ィル) -4-ォキソ -1- (2, 3, 4, 5 -テトラヒドロ- 1H- 3_ベンズァゼピン- 7-ィル)ブタン-卜オン トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (ESI) (M+1): 405
実施例 7 0
N - [卜 [4-ォキソ -4 -(2, 3, 4, 0 -テトラヒドロ- 1H-3-ベンズァゼピン- 7-ィル)ブ タノィル]ピロリジン- 3-ィル]ァセタミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (APCI) (M+1): 358
実施例 7 1
N -シク口へキシル メチル -4-ォキソ -4- (2, 3, 4, 5 -テトラヒドロ- 1H - 3-ベン ズァゼピン- 7-ィル)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題匕合物を得た。
MS (ESI) (M+1): 343
実施例 7 2
N-ベンジル- N-メチル -4-ォキソ -4- (2, 3, 4, 5-テトラヒドロ- 1H- 3-
ピン - 7 - ド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (ESI) (M+1): 351
実施例 7 3
N -ェチル -N- (2 -メトキシェチル) - 4-ォキソ -4 -(2, 3, 4, 5 -テトラヒドロ- 1H - 3- ベンズァゼピン- 7-ィル)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (ESI) (M+1): 333
実施例 7 4
4 -モルフオリン- 4-ィル- 4-ォキソ -卜(2, 3, 4, 5 -テトラヒドロ- 1H- 3-ベンズァ ゼピン- 7-ィル)ブタン- 1-オン トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (APCI) (M+1): 317
実施例 7 5
4 -(3, 5-ジメチルピペリジン-卜ィル) -4-ォキソ - 1 -(2, 3, 4, 5 -テトラヒドロ-
1H- 3-ベンズァゼピン- 7-ィル)ブ夕ン-卜オン トリフルォ口酢酸塩
Me
実施例 36と同様にして表題化合物を得た。 , MS(ESI) (M+1): 343
実施例 76
ォクタヒドロイソキノリン - 2 (1H)-ィル- 4-ォキソ - 1_(2, 3, 4, 5 -テトラヒド 口- 1H- 3-ベンズァゼピン- 7-ィル)ブタン-卜オン トリフルォロ酢酸塩
実施例 36と同様にして表題化合物を得た。
MS(ESI) (M+1): 369
実施例 77
4 - (4 -ヒドロキシピペリジン-卜ィル) -4-ォキソ -卜(2, 3, 4, 5-テトラヒドロ-
1H- 3-ベンズァゼピン- 7-ィル)ブタン-卜オン トリフルォロ酢酸塩
実施例 36と同様にして表題化合物を得た。
MS (APCI) (M-fl): 331
実施例 78
4-((2S)-2-[[(2, 6 -ジメチルフエニノ -1 -ィル). 4 -ォキソ -1- (2, 3, 4, 5-テトラヒド口- 1H- 3-ベンズァゼピン - 7- 卜オン トリフルォロ酢酸塩
実施例 36と同様にして表題化合物を得た。
MS(ESI) (M+1): 434
実施例 79
4一 [4- (4—クロ口フエニル) -4-ヒドロキシピペリ 1-ィル] -4-ォキソ -卜 (2, 3, 4, 5 -テトラヒドロ- 1H-3 -ベンズァゼピン - 7-ィル)ブタン- 1-オン トリ フルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (ESI) (M+1): 41
実施例 8 0
N -ェチル- N_ [l_ [4-ォキソ - 4 -(2, 3, 4, 5-テトラヒドロ- 1H- 3 -ベンズァゼピン- ァセトアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (ESI) (M+1): 386
実施例 8 1
N - [2- (ジメチルァミノ)ェチル ] -4 -ォキソ - 4-(2, 3, 4, 5 -テ卜ラヒドロ- 1H - 3 - ベンズァゼピン- 7-ィル)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物'を得た。
MS (APCI) (M+1): 318 '
実施例 8 2
N- [3- (ジメチルァミノ)プロピル ] -4 -ォキソ - 4- (2, 3, 4, 5 -テトラヒドロ- 1H -
ド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (APCI) (M+1): 360
実施例 8 3
4 -ォキソ - N - (2 -ピペリジン-卜ィルェチル) -4- (2, 3, 4, 5-テトラヒド P-1H-3- ベンズァゼピン- 7-ィル)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (APCI) (M+1): 358
実施例 8 4
N- (2-モルフオリン- 4-ィルェチル) - 4-ォキソ -4- (2, 3, 4, 5-テトラヒドロ- 1H -
3 -ベンズァゼピン- 7-ィル)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (APCI) (M+1): 360
実施例 8 5
N - [3- (4-メチルビペラジン-卜ィル)プロピル] - 4-ォキソ - 4- (2, 3, 4, 5-テトラ ヒドロ- 1H-3-ベンズァゼピン- 7-ィル)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た
MS (APCI) (M+l): 387
実施例 8 6
N - [3- [メチル(フエニル)ァミノ]プロピル] -4 -ォキソ- 4 - (2, 3, 4, 5-テトラヒ ドロ- 1H-3-ベンズァゼピン- 7-ィル)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (APCI) (M+l): 394
実施例 8 7
N -(卜べンジルピぺリジン -4-ィル) - 4 -ォキソ - 4 - (2, 3, 4, 5 -テトラヒド D-1H-
3 -ベンズァゼピン- 7-ィル)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (APCI) (M+l): 420
実施例 8 8
4 -ォキソ - 4_ (2, 3, 4, 5-テトラヒドロ- 1H - 3 -べンズァゼピン -7-ィル) -N- (2, 2, 6, 6-テトラメチルビペリジン- 4 -ィル)ブタンアミド トリフルォロ酢酸
実施例 3 6と同様にして表題化合物を得た。
MS (APCI) (M+l): 386
実施例 8 9
N- (2-ァニリノェチル) -4-ォキソ - 4- (2, 3, 4, 5 -テトラヒド口- 1H- 3-ベンズァ ゼピン- 7-ィル)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (APCI) (M+1): 366 '
実施例 9 0
4 -ォキソ -N- (ピリジン- 2 -ィルメチル) -4- (2, 3, 4, 5 -テトラヒドロ- 1H- 3-ベ ンズァゼピン- 7-ィル)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (APCI) (M+1): 338
実施例 9 1
4 -ォキソ -N- (ピリジン- 4一ィルメチル) - 4- (2,3, 4, 5-テトラヒドロ- 1H-3-ベ ンズァゼピン- 7-ィル)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (APCI) (M+1): 352
実施例 9 2
N - [3- (1H -イミダゾール- 1-ィル)プロピル] - 4-ォキソ -4- (2, 3, 4, 5-テトラヒ ドロ- 1H-3-ベンズァゼピン- 7-ィル)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (APCI) (M+1): 355
実施例 9 3
N- [3- (ジィソプロピルァミノ)ェチル] -4 -ォキソ - 4- (2, 3, 4, 5-テトラヒドロ-
1H-3-ベンズァゼピン- 7-ィル)ブ夕ンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (APCI) (Mil): 374
実施例 9 4
N - [3 -(ジメチルァミノ) - 2, 2-ジメチルプロピル] - 4-ォキソ -4- (2, 3, 4, 5 -テト ラヒドロ- 1H- 3-ベンズァゼピン- 7-ィル)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (APCI) (Mil) : 360
実施例 9 5
N - [3- (2 -メチルピぺリジン -トイル)プロピル] -4 -ォキソ - 4 - (2, 3, 4, 5-テトラ ヒドロ- 1H- 3-ベンズァゼピン- 7-ィル)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (APCI) (M+1): 386
実施例 9 6
N- (3 -モルフオリン- 4-ィルプロピル)- 4-ォキソ -4 -(2, 3, 4, 5 -テトラヒドロ- 1H-3-ベンズァゼピン- 7-ィル)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (APCI) (M+1): 374
実施例 9 7
4-ォキソ -N- (2-ピロリジン- 1 -ィルェチル) -4- (2, 3, 4, 5 -テトラヒド Π-1Η-3- ベンズァゼピン- 7-ィル)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (APCI) (M+1): 344
実施例 9 8
N- [2- [ェチル (2-メチルフエニル)ァミノ]ェチル] - 4-ォキソ - 4- (2, 3, 4, 5-テ 卜ラヒドロ- 1H- 3-ベンズァゼピン- 7-ィル)ブタンアミド トリフルォロ酢酸
実施例 3 6と同様にして表題化合物を得た。
MS (APCI) (M+1): 408
実施例 9 9
N - (卜べンジルピロリジン - 3-ィル) -4-ォキソ -4- (2, 3, 4, 5 -テトラヒドロ- 1H- ド トリフルォロ酢酸塩
MS (APCI) (M+1): 06
実施例 1 0 0
N - [3- [ビス(2-ヒドロキシェチル)ァミノ]プロピル] - 4-ォキソ -4- (2, 3, 4, 5- テトラヒドロ- 1H- 3-ベンズァゼピン- 7-ィル)ブタンアミド トリフルォロ酢
実施例 3 6と同様にして表題化合物を得た
MS (APCI) (M+1): 392
実施例 1 0 1
N- [3- [ (5 -二 卜 4-ォキソ -4- (2, 3, 4, 5-テトラヒ ドロ- 1H- 3-ベンズァゼピン- 7 -ィル)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (APCI)则: 412
実施例 1 0 2
4 -ォキソ - N- (ピリジン- 4-ィルメチル) - 4- (2, 3, 4, 5-テトラヒドロ- 1H- 3-ベン ズァゼピン- 7-ィル)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (APCI) (M+1): 338
実施例 1 0 3
4 -ォキソ -N -(ピリジン- 3 -ィルメチル ) _4- (2, 3, , 5-テトラヒドロ- 1Η- 3 -ベン ズァゼピン- 7-ィル)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (APCI) (M+1): 338
実施例 1 0 4
4-ォキソ -N- (2-ピリジン- 3-ィルェチル) -4- (2, 3, 4, 5-テトラヒドロ- 1H- 3 -べ ンズァゼピン- 7-ィル)ブタンアミド トリフルォ口酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (APCI) (M+1): 352
実施例 1 0 5
N- [2- (ジメチルァミノ )ェチル] - N-メチル -4-ォキソ -4 - (2, 3, 4, 5 -テトラヒド ロ- 1H-3-ベンズァゼピン- 7-ィル)ブタノヒドラジド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (APCI) (M+1): 332
実施例 1 0 6
N- (卜べンジルピロリジン- 3-ィル) -N-メチル -4-ォキソ -4 -(2, 3, 4, 5 -テトラ ヒドロ- 1H- 3-ベンズァゼピン- 7-ィル)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。 ' MS (APCI) (Mil): 420
実施例 1 0 7
N -ェチル- 4-ォキソ -N- (ピリジン- 4-ィルメチル) -4 -(2, 3, 4, 5 -テ卜ラヒドロ- 1H- 3-ベンズァゼピン- 7-ィル)ブタンアミド トリフルォロ酢酸塩
• 実施例 3 6と同様にして表題化合物を得た。
MS (APCI) (Mil): 366
実施例 1 0 8
4-ォキソ - N, N-ビス (ピリジン- 3-ィルメチル) -4- (2, 3, 4, 5 -テトラヒド Π-1Η- 3 -ベンズァゼピン- 7-ィル)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (APCI) (M+l): 429
実施例 1 0 9
4 - (4 -ェチルピペラジン-卜ィル) -4-ォキソ -1 -(2, 3, 4, 5 -テトラヒドロ- 1H - 3- ベンズァゼピン- 7-ィル)ブタン-卜オン トリフルォロ酢酸塩
0 'Me
実施例 3 6と同様にして表題化合物を得た。
MS (APCI) (M+1): .344
実施例 1 1 0
ェチル [4- [4-ォキソ - 4- (2, 3, 4, 5 -テ卜ラヒドロ- 1H- 3 -べンズァゼピン _7 -ィ
実施例 3 6と同様にして表題化合物を得た。
MS (APCI) (M+1): 01
実施例 1 1 1
4 -(4-ベンジルピペラジン- 1-ィル ) -4-ォキソ -1- (2, 3, 4, 5 -テ卜ラヒドロ- 1H -
3-ベンズァゼピン -7-ィル)ブタン-卜オン トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (APCI) (M+1): 406 '
実施例 1 1 2
4_ォキソ -4- [4- (ピリジン- 2-ィル)ピぺラジン- 1-ィル] -1_ (2, 3, 4, 5-テトラ ヒドロ- 1H- 3-ベンズァゼピン- 7-ィル)ブタン-卜オン トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た
MS (APCI) (M+1): 393
実施例 1 1 3
4_ (4 -べ. 卜ィル) -4-ォキソ-卜(2, 3, 4, 5-テトラヒド ロー 1H - 3-ベンズァゼピン- 7-ィル)ブタン-卜オン トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (ESI) (M+1): 482
実施例 1 1 4
4 -ォキソ -4- (4-フエニルピペラジン-卜ィル) -卜(2, 3, 4, 5-テトラヒドロ- 1H-
3-ベンズァゼピン- 7-ィル)ブタン-卜オン トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (ESI) (M+1): 392
実施例 1 1 5
4 - [4 -(2 -メトキシフエニル)ピペラジン-卜ィル] -4-ォキソ -卜(2, 3, 4, 5 -テト ラヒドロ- 1H-3-ベンズァゼピン- 7-ィル)ブタン-卜オン トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (ESI) (M+1): 32
実施例 1 1 6
4- (1,4,-ビピペリジン- 1 '_ィル) -4-ォキソ -卜(2, 3, 4, 5 -テトラヒド口- 1H- 3- ベンズァゼピン- 7-ィリレ)ブタン -1-ォン トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (APCI) (M+1): 398
実施例 1 1 7
4 - [3- (ジメチルァミノ)ピロリジン-〗 -ィル] -4-ォキソ-卜 (2, 3, 4, 5-テトラヒ ドロ -1Η_3-ベンズァゼピン- 7-ィル)ブタン- 1-オン トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (APCI) (M+1): 344
実施例 1 1 8
N -ベンジル- N -(1 -べンジルピロリジン- 3 -ィル) -4-ォキソ -4- (2, 3, 4, 5-テト ラヒドロ- 1H- 3-ベンズァゼピン- 7-ィル)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (ESI) (M+1): 496
実施例 1 1 9
4 -ォキソ - N, N -ビス(ピリジン- 2-ィルメチル) -4- (2, 3, 4, 5 -テトラヒド P-1H- 3_ベンズァゼピン- 7-ィル)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (APCI) (M+1): 29
実施例 1 2 0
4 - (4-メチル -1, 4 -ジァゼピン-卜ィル) -4 -ォキソ -卜(2, 3, 4, 5-テトラヒドロ- 1H-3-ベンズァゼピン- 7-ィル)ブタン- 1-オン トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (APCI) (M+1): 344
実施例 1 2 1
4- [4- (2-ヒドロキシェチル)ピペラジン-卜ィル] -4-ォキソ -卜(2, 3, 4, 5_テト ラヒドロ- 1H- 3-ベンズァゼピン- 7-ィル)ブタン- 1-オン トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た
MS (APCI) (M+1): 360
実施例 1 2 2
4- [4- (1 , 3-ベンゾジォキソール- 5- 1-ィル] +ォキ ソ -1- (2, 3, 4, 5-テトラヒド口- 1H - 3-ベンズァゼピン- 7 -ィル)ブタン- 1-オン トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (APCI) (M+1): 450
実施例 1 2 3
4 -ォキソ -4- [4- (ピリミジン- 2-ィル)ピぺラジン -1 -ィル ] - 1_ (2,3,4, 5 -テト ラヒド口- 1H-3-ベンズァゼピン- 7-ィル)ブタン- 1-オン トリフルォロ酢酸
実施例 3 6と同様にして表題化合物を得た。
MS (ESI) (M+1): 394
実施例 1 2 4
4 -ォキソ -4- [4- [ (2E) -3-フェニル- 2-プロぺニル]ピぺラジン-卜ィル] -卜 (2, 3, 4, 5 -テトラヒド口- 1H - 3-ベンズァゼピン -7-ィル)ブタン-卜オン トリ フルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (ESI) (M+1): 432
実施例 1 2 5
N -ベンジル- N- [2- (ジメチルァミノ)ェチル ] -4-ォキソ -4- (2, 3, 4, 5 -テトラヒ ドロ- 1 H-3-ベンズァゼピン- 7-ィル)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (APCI) (M+1): 08
実施例 1 2 6 ,
N-メチル- N- (1 -メチルピペラジン- 4-ィル) -4-ォキソ -4- (2, 3, 4, 5-テトラヒ ドロ- 1H- 3-ベンズァゼピン- 7-ィル)ブタンアミド トリフルォロ酢酸塩
実施例 3 6と同様にして表題化合物を得た。
MS (APCI) (M+1): 358
実施例 1 2 7
4-ォキソ - 4- [2- (ピロリジン- 1-ィルメチル)ピロリジン- 1-ィル] -卜
(2, 3, 4, 5-テトラヒド口- 1H- 3-ベンズァゼピン- 7-ィル)ブ夕ン-卜オン トリ フルォロ酢酸塩 .
実施例 3 6と同様にして表題化合物を得た。
MS (APCI) (M+1): 384
実施例 1 2 8
4一ォキソ一
4— [ (ピロリジン— ィル)ピペリジン一 }一ィル]一卜(
2,
3,
4,
5-テト ラヒドロ- 1H-3-ベンズァゼピン- 7-ィル)ブタン- 1-オン トリフルォロ酢酸
実施例 36と同様にして表題化合物を得た。
MS(APCI) (M+1): 384
実施例 129
N -ベンジル- N- (2-力ルポキシェチル) -4-ォキソ -4- (2, 3, 4, 5-テトラヒドロ- 1H- 3-ベンズァゼピン- 7-ィル)ブタンアミド トリフルォロ酢酸塩
実施例 36と同様にして表題化合物を得た。
MS(ESI) (M+1): 409
実施例 130
4- [4- (4 -クロ口フエニル) -卜ピぺリジニル] -4-ォキソ-卜(2, 3, 4, 5-テトラヒ ドロ- 1H - 2 -ベンズァゼピン- 8 -ィル) -卜ブタノン
1 ) 2- (トリフルォロアセチル )-2, 3, 4, 5-テトラヒド口- 1H-2-ベンズァゼ ピンを用いて、 参考例 15と同様の操作を行うことにより、 4-ォキソ -4- [2- (トリフルォロアセチル) - 2, 3, 4, 5-テ卜ラヒド口- 1H- 2 -ベンズァゼピン- 8 -ィ ル]ブタン酸を得た。
'H-NMR (DMSO— d6) δ 1.82 (2Η, m), 2.58 (2H, t, J = 6.2 Hz), 3.08 (2H, m), 3.23 (2H, t, J = 6,0 Hz), 3.89 (2H, m), 4.73 (2H, m), 7.37-7.41 (1H,
m), 7.84-7.88 (2H, m), 12.16 (1H, s).
2) 上記 1) で得た 4-ォキソ -4- [2- (トリフルォロアセチル )-2, 3, 4, 5 - テトラヒドロ- 1H- 2-ベンズァゼピン- 8-ィル]ブタン酸を用いて、 実施例 12 および実施例 13と同様の操作を順次行うことにより、 表題化合物を無色粉 末として得た。
'H-NMR (CDC13) δ: 1.57-1.90 (6Η, m), 2.60-2.74 (3H, m), 2.82 (2H, t, J = 6.6 Hz), 2.99 (2H, m), 3.12-3.24 (3H, m), 3.34 (2H, t, J = 6.6 Hz), 4.01 (2H, s), 4.13 (1H, d, J = 15.6 Hz), 4.76 (1H, d, J = 12 Hz), 7.12-7.30 (5H, m), 7.79 (2H, m).
融点: 122- 124 °C (結晶化溶媒: エタノール-ジイソプロピルエーテル) 実施例 131
4 - [4- (4 -ク口口フエニル) -卜ピぺリジニル ] -1- (2-メチル- 2, 3, 4, 5-テトラヒ ド口- 1H-2 -ベンズァゼピン -8 -ィル)- 4-ォキソ -1 -ブタノン
実施例 130で得た 4- [4- (4-クロ口フエニル) -卜ピペリジニル ]-4-ォキソ - 1-(2, 3, 4, 5-テトラヒドロ- 1H- 2-ベンズァゼピン- 8-ィル) -卜ブタノンを用 いて、 実施例 16と同様の操作を行うことにより、 表題化合物を無色粉末と して得た。
'H-NMR (CDC13) δ: 1.57-1.94 (6Η, m), 2.33 (3H, s), 2.61-2.70 (2H, m), 2.84 (2H, t, J = 6.6 Hz), 3.00 (2H, m), 3.02 (2H, t, J = 5.1 Hz), 3.18 (1H, m), 3.36 (2H, t, J = 6.6 Hz), 3.85 (2H, s), 4.14 (1H, d, J = 15.6 Hz), 4.76 (1H, d, J = 12 Hz), 7.12-7.30 (5H, m), 7.83 (2H, m).
融点: 133-134 °C (結晶化溶媒: エタノール-ジイソプロピルエーテル) 実施例 132
4- [4- (4-クロ口フエ二ル)- 1-ピぺリジニル] -1- (2, 3 -ジヒドロ- 1H-イソイン ドール- 5-ィル) -4-ォキソ -1-ブタノン
1) 2- (トリフルォロアセチル) イソインドールを用いて/参考例 1 5と 同様の操作を行うことにより、 4-ォキソ -4- [2- (トリフルォロアセチル )- 2,3 - ジヒドロ- 1H -ィソィンドール - 5-ィル]ブ夕ン酸を得た。
Ή-N R (DMS0 - d6) δ: 2.59 (2Η, t, J = 6.2 Hz), 3.25 (2H, t, J = 6.0 Hz), 4.90 (2H, m), 5.12 (2H, m), 7.55 (1H, m), 7.96-8.05 (2H, i), 12.16 (1H, s).
2) 上記 1)で得た 4-ォキソ -4- [2- (トリフルォロアセチル )-2, 3 -ジヒド ロ- 1H-ィソインドーソレ- 5-ィル]ブ夕ン酸を用いて、 実施例 12および実施例 1 3と同様の操作を順次行うことにより、表題化合物を無色粉末として得た。 ■H-NMR (CDC13) δ: 1.56-1.68 (2Η, m), 1.82-1.96 (2H, i), 2.58-2.74 (2H, s), 2.84 (2H, t, J = 6.6 Hz), 3.04 (1H, s), 3.17 (1H, i), 3.36 (2H, t, J = 6.6 Hz), 4.15 (1H, d, J = 15.6 Hz), 4.31 (4H, s), 4.76 (1H, d, J = 12 Hz), 7.11-7.36 (5H, m), 7.92 (2H, m).
融点: 133- 134 (結晶化溶媒: ェ夕ノール-ジィソプロピルエーテル) 実施例 1 33
Ν,Ν-ジプロピル-(3, 4-ジヒドロ- 2Η- 1, 4-ベンズォキサジン- 3-ォキソ -6 -ィ ル)ァセ卜アミド
参考例 1 7で得た Ν, Ν-ジプロピル- (4-ェトキシカルポニルメトキシ -3 -二 トロフエニル)ァセトアミド (11 g, 30.0 MIOI)のエタノ-ル溶液 (500 ml)に 10 %パラジウム-炭素 (2.5 g)を加え、 常圧下に室温で接触水素添加反応に付 した。 反応終了後、 触媒をろ去し、 得られたろ液を濃縮した。 残渣をトルェ ン(500 ml)に溶解し、 終夜加熱還流した。 反応液を濃縮後、 酢酸ェチル -へキ
サンより再結晶し、 表題化合物 (8.4 g)を即 121- 122°Cの結晶として得た。 Ή-NMR (CDC13) δ: 0.8-1.0 (6Η, m), 1.4-1.7 (4H, HI), 3.15-3.4 (4H, m); 3.62 (2H, s), 4.53 (2H, s), 6.7-6.9 (3H, m), 9.1-9.4 (1H, br).
元素分析値 C16H22N203として ' 計算値: C, 66.18; H, 7.64; N, 9.65.
実験値: C, 66.07; H, 7.37; N, 9.59.
実施例 134
3, 4-ジヒド口- 6- [2- (N, N-ジプロピルァミノ)ェチル] -2H-1 , 4-ベンズォキサ ジン 塩酸 ¾
実施例 133で得た N, ジプロピル -(3, 4-ジヒド口- 2H- 1, 4-ベンズォキサ ジン- 3-ォキソ -6-ィル)ァセトアミド (10 g, 34.4 mmol)の THF (200 ml)溶液 に 1規定のポラン ZTHF溶液 (140 ml, 140 mmol)を加え、 室温で 4時間撹拌 した後、 氷冷下、 反応液に 6規定塩酸(30 ml, 180匪 ol)を滴下した。 反応液 を 6規定水酸化ナトリウム水溶液で中和後、 酢酸ェチルで抽出した。 抽出液 を水洗後、 無水硫酸マグネシウムで乾燥し、 濃縮した。 残渣をシリカゲル力 ラムクロマトグラフィー (展開溶媒;へキサン:酢酸ェチル =4:1)で精製し、 4規定塩酸 Z酢酸ェチル溶液を加えた後、 濃縮することにより表題化合物 (6.8 g)を非晶状粉末として得た。
'H-NMR (CDC13, フリ一塩基) <5: 0.91 (6H, t, J = 7.2 Hz), 1.6-1.8 (4H, m), 2.6-2.8 (4H, m), 2.84 (4H, brs), 3.41 (2H, t, J = 4.4 Hz), 3.6-4.0 (1H, br), 4.22 (2H, t, J = 4.4 Hz), 6.4-6.6 (2H, m), 6.65"-6.75 (1H, m). 実施例 135
3, 4-ジヒド口 -6 - [2- (N, N -ジプロピルァミノ )ェチル] -4- 0 -ナフタレンスル ホニル )-2H- 1,4-ベンズォキサジン シユウ酸塩
実施例 134で得た 3, 4-ジヒドロ- 6- [2- (N, N- 2H - 1, 4-ベンズォキサジン 塩酸塩 (300 mg, 1.14 mmol), 4-ジメチルァミノ ピリジン (HO mg, 1.14匪 ol)およびトリェチルァミン (0.48 ml, 3.43mmol) のァセトニトリル溶液 (15 ml)に、卜ナフタレンスルホニルクロリド (388 mg, 1.72 mmol)のァセトニトリル溶液 (5 ml)を氷冷下加え、 室温で 4時間撹拌し た。 反応液に水 (50ml)を加え、 酢酸ェチルで抽出した。 抽出液を、 10%炭酸 力リゥム水溶液および飽和食塩水で洗浄後、 無水硫酸ナトリゥムで乾燥し、 濃縮した。残渣をシリカゲル力ラムクロマトグラフィー (展開溶媒;酢酸ェチ ル)で精製し、 シユウ酸 (1当量) を加えた後、 酢酸ェチル -ジイソプロピル エーテルから再結晶し、 表題化合物 (220 nig)を、 mp 144-145°Cの結晶として 得た。
Ή-NMR (CDC13, フリー塩基) δ 0.89 (6Η, t, J = 7.2 Hz), 1.4-1.6 (4H, in), 2.4-2.6 (4H, m), 2.66 (4H, brs), 3.65 (2H, t, J = 4.6 Hz), 3.89 (2H, t, J = 4.6 Hz), 6,64 (1H, d, J = 8.4 Hz), 6.89 (1H, dd, J = 8.4, 1.8 Hz), 7.3-7.6 (4H, m) , 7.90 (1H, d, J = 7.8 Hz), 8.08 (1H, d, J = 8.4 Hz), 8.2-8.4 (2H, m).
実施例 136
3, 4 -ジヒド Π-6- [2- (Ν, Ν-ジプロピルァミノ )ェチル] -4- (2-ナフタレンスル ホニル) - 2H-1, 4-ベンズォキサジン シユウ酸塩 .
実施例 134で得た 3, 4-ジヒドロ- 6 - [2 - (N, N- 2H-1, 4-ベンズォキサジン 塩酸塩を用いて、実施例 1 35と同様の操作を行 うことにより、 表題化合物を無色非晶状粉末として得た。
'H-匪 R (CDC13, フリー塩基) δ: 0.90 (6Η, t, J = 7.2 Hz) , 1.4-1.6 (4H, m),
2.4- 2.6 (4H, m), 2.71 (4H, brs), 3.68 (2H, t, J = 4.6 Hz), 3.93 (2H, t, 4.6 Hz),.6.68 (1H, d, J = 8.4 Hz), 6.90 (1H, dd, J = 8.4, 1.8 Hz),
7.5- 7.8 (4H, m), 7.8-8.0 (3H, m), 8.29 (1H, brs).
実施例 137
4 - (4-クロ口べンゼンスルホニル) -3, 4-ジヒドロ- 6- [2- (N, N-ジプロピルァミ ノ)ェチル ]-2H - 1,4-ベンズォキサジン シユウ酸塩
実施例 1 34で得た 3, 4-ジヒドロ- 6 - [2 - (Ν,Ν-ジプロピルァミノ)ェチル] - 2Η- 1,4-ベンズォキサジン 塩酸塩を用いて、実施例 135と同様の操作を行 うことにより、 表題化合物を粉末として得た。
Ή-腿 (CDC13, フリー塩基) <5: 0.89 (6H, t, J = 7.2 Hz), 1.4-1.6 (4H, 1), 2.4-2.6 (4H, m), 2.69 (4H, brs), 3.72 (2H, t, J = 4.6 Hz), 3.88 (2H, t, J = 4.6 Hz), 6.72 (1H, d, J = 8.4 Hz) , 6.92 (1H, dd, J = 8.6, 2.0 Hz) , 7.41 (2H, d, J = 8.8 Hz) , 7.56 (2H, d, J = 8.8 Hz) , 7.64 (1H, d, J = 2.0 Hz).
元素分析値 C24H31C1N207Sとして
計算値: C, 54.70; H, 5.93; N, 5.32.
実験値: C, 54.46; H, 5.88; N, 5.29.
融点: 130- 133°C (結晶化溶媒: アセトン)
実施例 138
3, 4 -ジヒド口- 6- [2- (N,N-ジプロピルァミノ)ェチル ] -4- (2, 4, 6-トリメチル ベンゼンスルホ二ル)- 2H- 1,4-ベンズォキサジン シユウ酸塩
• 実施例 134で得た 3, 4-ジヒドロ- 6- [2-(N,N-ジプロピルァミノ)ェチル] - 2H-1,4-ベンズォキサジン 塩酸塩を用いて、実施例 135と同様の操作を行 うことにより、 表題化合物を粉末として得た。
'H-NMR (CDC13, フリー塩基) (5: 0.88 (6H, t, J = 7.4 Hz), 1.3-1.6 (4H, m), 2.3-2.6 (4H, in), 2.33 (3H, s), 2.48 (4H, brs), 2.57 (6H, s), 3.83 (2H, t, J = 4.6 Hz), 4.23 (2H, t, J = 4.6 Hz) , 6.61 (1H, brs), 6.8-6.85 (2H, m), 7.00 (2H, s). ' 融点: 157- 158°C (結晶化溶媒:酢酸ェチル-ジイソプロピルエーテル) 実施例 139 '
4- (4- -ブチルベンゼンスルホ二ル)- 3, 4-ジヒド口- 6- [2- (N, N-ジプロピルァ ミノ)ェチル]-211-1,4-べンズォキサジ.ン シユウ酸塩
実施例 134で得た 3, 4 -ジヒドロ- 6- [2- (N,N -ジプロピルアミノ)ェチル] - 2H-1,4-ベンズォキサジン 塩酸塩を用いて、実施例 135と同様の操作を行 うことにより、 表題化合物を非晶状粉末として得た。 '
Ή-NMR (CDC13, フリー塩基) δ: 0.90 (6Η, t, J = 7.2 Hz), 1.30 (9H, s), 1.3-1.6 (4H, m), 2.4-2.55 (4H, i), 2.69 (4H, s), 3.71 (2H, t, J '= 4.0 Hz), 3.85 (2H, t, J = 4.0 Hz), 6.72 (1H, d, J - 8. Hz), 6.90 (1H, dd, J = 8.2, 2.0 Hz), 7.44 (2H, d, J = 8.8 Hz), 7.57 (2H, d, J = 8.8 Hz), 7.68 (1H, d, J = 2.0 Hz).
元素分析値 C2SH4()N207Sとして
計算値: C, 61.29; H, 7.35; N, 5.11.
実験値: C, 61.02; H, 7.57; N, 5.00.
実施例 140
4 -べンジルスルホニル -3, 4-ジヒド口- 6- [2- (N, N-ジプロピルァミノ)ェチ リレ ]- 2H - 1,4 -べンズォキサジン シユウ酸塩
(C¾H)2 Me
実施例 134で得た 3, 4-ジヒドロ- 6- [2- (N,N-ジプロピルアミノ)ェチル] - 2H - 1, 4-ベンズォキサジン 塩酸塩を用いて、実施例 135と同様の操作を行 うことにより、 表題化合物を粉末として得た。
Ή-NMR (CDC13, フリ一塩基) δ: 0.89 (6Η, i, J - 7.2 Hz), 1.4-1.6 (4H, ), 2.4-2.55 (4H, i), 2.66 (4H, brs), 3.53 (2H, t, J = 4.2 Hz), 3.73 (2H, t, J = 4.2 Hz), 4.44 (2H, s), 6.7-7.0 (2H, m), 7.1-7.4 (6H, m).
融点: 150- 151°C (結晶化溶媒:酢酸ェチル -ジィソプロピルエーテル) 実施例 141
3, 4-ジヒド口- 6- [2- (N, N -ジプロピルァミノ )ェチル] -4- (2 -ナフトィル) -2H-
1,4-ベンズォキサジン 塩酸塩
実施例 134で得た 3, 4-ジヒド口- 6- [2- (N, N-ジプロピルァミノ)ェチル] - 2H - 1,4-ベンズォキサジン 塩酸塩を用いて、実施例 135と同様の操作を行 うことにより、 表題化合物を粉末として得た。
Ή -匪 R (CDClj, フリー塩基) (5: 0.75 (6H, t, J = 7.2 Hz), 1.0-1.4 (4H, m), 1.9-2.2 (6H, m), 2.2-2.4 (2H, m), 4.06 (2H, t, J = 4.2 Hz), 4.39 (2H, t, J = 4.2 Hz), 6.5-6.9 (3H, m) , 7.4-7.6 (3H, m), 7.7-7.9 (3H, m), 8.04 (1H, s).
融点: 165-166 °C (結晶化獰媒:メタノ -ル-ジェチルエーテル)
実施例 142
4 -(4-ビフエ二リレ-卜カルボニル) -3, 4-ジヒドロ- 6- [2- (Ν,Ν-ジプロピルアミ ノ)ェチル] -2H-1, 4 -べンズォキサジン
実施例 134で得た 3, 4-ジヒドロ- 6- [2-(N,N-ジプロピルァミノ)ェチル] - 2H - 1, 4-ベンズォキサジン 塩酸塩を用いて、実施例 135と同様の操作を行 うことにより、 表題化合物を粉末として得た。
Ή-NMR (CDC13) ά: 0.75 (6Η, t, J = 7.2 Hz), 1.1-1.4 (4H, m), 2.1-2.6 (8H, m), 4.04 (2H, t, J = 4.6 Hz)., 4.38 (2H, t, J = 4.6 Hz), 6.6-6.9 (3H, in), 7.3-7.5 (3H, in), 7.5-7.7 (6H, m).
融点: 95- 96 °C (結晶化溶媒:酢酸ェチル -ジイソプロピルエーテル) 実施例 143
3, 4-ジヒドロ- 6-[2- (N, N-ジプロピルァミノ)ェチル ]-4 -(1-ナフチルメチ ル) -2H- 1,4 -べンズォキサジン 塩酸塩
実施例 134で得た 3, 4-ジヒドロ- 6- [2- (N,N-ジプロピルァミノ)ェチル] - 2H_1,4-ベンズォキサジン 塩酸塩 (200 mg, 0.76 mmol)および卜クロロメチ ルナフタレン (400 mg, 2.29 mmol)の DMF溶液 (15 ml)に炭酸カリウム (316 mg, 2.29腿 ol)を加えた。 反応液を室温で 2時間撹拌後、 水を加え、 酢酸ェ チルで抽出した。 抽出液を水洗し、 無水硫酸ナトリウムで乾燥、 濃縮した。 残渣をシリ力ゲル力ラムクロマトグラフィー (展開溶媒;へキサン:酢酸エヂ ル =3:1)で精製後、 4規定塩酸ノ酢酸ェチル溶液で処理し、 アセトン-ペン夕 ンより結晶化して、 表題化合物 (80' mg)を mp 177-178 °Cの結晶として得た。 'H-NMR (CDC13, フリー塩基) (5 : 0.82 (6H, t, J = 7.4 Hz), 1.4-1.7 (4H, m), 2.3-2.5 (4H, m), 2.59 (4H, brs), 3.28 (2H, t, J = 4. Hz) , 4.21 (2H, t, J = 4.4 Hz), 4.84 (2H, s), 6.4-6.6 (2H, m), 6.7-6.8 (1H, m), 7.3-7.6 (4H,
m), 7.7-8.0 (2H, m), 8.0-8.1 (1H, m).
元素分析値 C27H35C1N20 · 0.5H20として
計算値: C, 72.38; H, 8.10; N, 6.25.
実験値: C, 72.24; H, 7.91; N, 6.12.
実施例 144
3, 4 -ジヒドロ- 6- [2-(N, N- 1-4- (2-ナフチルメチ ル)- 2H- 1,4-ベンズォキサジン 塩酸塩
実施例 134で得た 3, 4-ジヒドロ- 6- [2- (N,N-ジプロピルアミノ)ェチル] - 2H-1, 4-ベンズォキサジン 塩酸塩を用いて、実施例 143と同様の操作を行 うことにより、 表題化合物を粉末として得た。
Ή-NMR (CDC13, フリー塩基) δ: 0.82 (6Η, t, J = 7.4 Hz), 1.4-1.7 (4H, m), 2.4-2.9 (8H, ι), 3.3-3.5 (2H, m), 4.2-4.4 (2H, i), 4.59 (2H, brs), 6.4-6.6 (2H, m), 6.7-6.8 (1H, m), 7.3-7.5 (3H, m), 7.7-7.9 (4H, i).
融点: 169-170 °C (結晶化溶媒:ジェチルェ一テルへキサン)
実施例 145 ,
3, 4 -ジヒド口- 6- [3- (N, N -ジプロピルァミノ)プロピル] -4- (2 -ナフタレンス ルホニル) - 2H - 1,4-ベンズォキサジン シユウ酸塩
参考例 19で得た 3, 4-ジヒド口- 6- (3-ョ-ドプロピル) -4- (2-ナフタレンス ルホニル)- 2H- 1,4-ベンズォキサジン (1.0 g, 2.16 n皿 ol)およぴジプロピル ァミン(263 mg, 2.60 mmol)の DMF溶液 (20 ml)に炭酸カリウム (0.9 g, 6.48 ramol)を加え、 室温で終夜撹拌した。 反応液に水を加え、 酢酸ェチルで抽出し
た。 抽出液を水および飽和重曹水で洗浄後、 無水硫酸ナトリウムで乾燥し、 濃縮した。 残渣をアルミナカラムクロマトグラフィー (展開溶媒;へキサン: 酢酸ェチル =4:1)で精製後、 酢酸ェチルに溶解した。 得られる溶液に 1当量 のシユウ酸を加えた後、 溶媒を留去して表題化合物 (1.17 g)を非晶状粉末と して得た。
Ή -醒 R (CDC13, フリー塩基) (3: 0.8-1.0 (6H, m), 1.3-1.6 (4H, m), 1.6- 1.9 (2H, m), 2.3-2.6 (8H, m), 3.67 (2H, t, J = 4.6 Hz), 3.92 (2H, t, J = .6 Hz) , 6.68 (1H, d, J = 8.4 Hz), 6.91 (1H, dd, J = 8.4, 2.0 Hz) , 7.52 (1H, dd, J = 8.4, 2.0 Hz), 7.5-7.5 (2H, m), 7.76 (1H, d, J = 2.0 Hz), 7.8-8.0 (3H, m), 8.28 (1H, d, J = 1.8 Hz).
実施例 146
3, 4-ジヒドロ- 4 - (2-ナフタレンスルホニル) - 6 - [3- (N -プロピルアミノ)プロ ピル] - 2H-1, 4 -べンズォキサジン シユウ酸塩
参考例 19で得た 3, 4-ジヒド口- 6- (3-ョ-ドプロピル) -4- (2 -ナフタレンス ルホニル) -2H-1, 4-ベンズォキサジンを用いて、実施例 145と同様の操作を 行うことにより、 表題化合物を粉末として得た。
Ή-NMR (CDC13, フリー塩基) <5: 0.92 (3H, t, J = 7.4 Hz), 1.4-1.7 (2H, m), 1.7-2.0 (4H, m), 2.5-2.8 (4H, m), 3.68 (2H, t, J = 4.6 Hz), 3.92 (2H, t, J = 4.6 Hz), 6.68 (1H, d, J = 8.4 Hz) , 6.89 (1H, dd, J = 8.4, 2.2 Hz) , 7.4-7.7 (3H, m), 7.74 (1H, d, J = 1.8 Hz), 7.8-8.0 (3H, m), 8.28 (1H, d, J - 1.6 Hz).
融点: 155- 156 °C (結晶化溶媒:メタノ -ル-ジェチルェ一テル)
実施例 147
3, 4 -ジヒド D-4- (2-ナフタレンスルホニル) -6- [3- (4-ピぺリジノピぺリジ ノ)プロピル] - 2H-1, 4-ベンズォキサジン 2塩酸塩
参考例 19で得た 3, 4-ジヒド口- 6- (3-ョ-ドプロピル) -4- (2-ナフタレンス ルホニル )-2H- 1,4-ベンズォキサジンを用いて、実施例 145.と同様の操作を 行うことにより、 表題化合物を粉末として得た。
Ή-NMR (CDC13, フリー塩基) (5: 1.3-2.0 (13H, m) , 2.1-2.4 (4H, m), 2.4-2.7 (6H, m), 2.9-3.1 (2H, m), 3.68 (2H, d, J = 4.6 Hz), 3.91 (2H, d, J = 4.6 Hz), 6.68 (1H, d, J = 8.2 Hz), 6.89 (1H, dd, J = 8.2, 2.0 Hz), 7.4-7.7 (3H, m), 7.74 (1H, d, J = 2.0 Hz), 7.8-8.0 (3H, m), 8.28 (1H, d, J = 1.6 Hz).
融点: 240-241 °C (結晶化溶媒:メタノ-ル-ジェチルエーテル)
実施例 148
3, 4-ジヒド口- 4 - (2 -ナフタレンスルホニル) -6- [3 - (4-フエニルピぺリジノ) プロピル]- 2H- 1,4 -べンズォキサジン 塩酸塩
参考例 19で得た 3, 4-ジヒドロ- 6- (3-ョ-ドプロピル)- 4- (2 -ナフタレンス ルホニル)- 2H- 1,4-ベンズォキサジンを用いて、実施例 145と同様の操作を 行うことにより、 表題化合物を粉末として得た。
Ή-NMR (CDC13, フリ一塩基) δ: 1.6-2. (8Η, m) , 2.3-2.6 (3H, m) , 2.64 (2Η, ί, J = 7.6 Hz), 3.0-3.2 (2H, m), 3.68 (2H, t, J - 4.6 Hz), 3.93 (2H, t, J = 4.6 Hz), 6.69 (1H, d, J = 8. Hz), 6.91 (1H, dd, J = 8.4, 2.0 Hz), 7.1-7.4 (5H, m), 7.4—7.7 (3H, m), 7.76 (1H, d, J = 2.0 Hz), 7.8-8.0 (3H, m), 8.30 (1H, brs).
融点: 182- 183 °C (結晶化溶媒:メタノ-ル-ジェチルエーテル)
実施例 149 .
6- [3- [4- (4-クロ口フエニル) - 4-ヒドロキシピペリジノ]プロピル] -3, 4 -ジヒ ド口- 4- (2-ナフタレンスルホニル) -2H-1 , 4-ベンズォキサジン 塩酸塩
参考例 1 9で得た 3,4-ジヒドロ- 6- (3-ョ-ドプロピル)- 4- (2-ナフ夕レンス ルホニル) - 2H-1, 4-ベンズォキサジンを用いて、実施例 145と同様の操作を 行うことにより、 表題化合物を粉末として得た。
Ή-N R (CDC13) δ: 1.7-2.0 (4Η, ) , 2.15 (2H, td, J = 13.2, 4.4 Hz) ,
2.3-2.6 (4H, m), 2.65 (2H, t, J = 7.6 Hz), 2.7-2.9 (2H, i), 3.67 (2H, t, J = 4.6 Hz), 3.92 (2H, t, J = 4.6 Hz), 6.70 (1H, d, J = 8.4 Hz), 6.91
(1H, dd, J = 8.4, 1.8 Hz), 7.2-7.4 (2H, m), 7,4-7.7 (7H, m), 7.77 (1H, d, J = 2.0 Hz), 7.8-8.0 (3H, ) , 8.29 (1H, brs).
融点: 125-126 °C (結晶化溶媒:メタノ-ル-ジェチルエーテル)
実施例 150 ル] -4- (2-ナフタレンスルホニル) -2H-1, 4-ベンズォキサジン 2塩酸塩
参考例 19で得た 3, 4-ジヒドロ- 6- (3-ョ-ドプロピル)- 4- (2 -ナフタレンス ルホニル) -2H- 1,4-ベンズォキサジンを用いて、実施例 145と同様の操作を 行うことにより、 表題化合物を粉末として得た。
Ή-NMR (CDC13J フリ一塩基) δ: 1.7-1.9 (2Η, m), 2.3-2.7 (12H, m), 3.42 (2H, s), 3.68 (2H, t, J = 4.6 Hz), 3.92 (2H, t, J = 4.6 Hz), 5.94 (2H,
s), 6.68 (1H, d, J = 8.4 Hz), 6.75 (2H, brs), 6.8-7.0 (2H, m), 7.4-7.7 (3H, m), 7.74 (1H, d, J = 2.0 Hz), 7.8-8.0 (3H, m), 8.28 (1H, d, J = 1.6 Hz).
融点: 212-213 °C (結晶化溶媒:メタノ-ル-ジェチルエーテル)
実施例 151
3, 4-ジヒドロ -4- [3, 4-ジヒドロ- 6, 7-ジメトキシスピロ [ナフタレン- 2 (1H), 2,ーピぺリジン]—2,—ィル] _4- -ナフタレンスルホニル) -2H-1, 4-ベンズォキ サジン 塩酸塩
参考例 19で得た 3, 4-ジヒドロ- 6_(3-ョ-ドプロピル)- 4- (2-ナフタレンス ルホニル)- 2H-1, 4-ベンズォキサジンを用いて、実施例 145と同様の操作を 行うことにより、 表題化合物を非晶状粉末として得た。
Ή-NMR (CDC13, フリー塩基) δ 1.3-2.0 (10H, m), 2.3-2.9 (10H, m), 3.66 (2H, t, J = 4.4 Hz), 3.82 (6H, s), 3.90 (2H, t, J = 4.4 Hz), 6.56 (2H, brs), 6.68 (1H, d, J = 8.4 Hz) , 6.90 (1H, dd, J = 8.4, 2.0 Hz), 7. 7 (1H, dd, J = 8.6, 2.0 Hz), 7.5-7.7 (2H, m), 7.7-8.0 (4H, m), 8.27 (1H, brs). 実施例 152
3, 4-ジヒド口- 4- (2-ナフタレンスルホニル) -6- [3- (4-ピリジルメチルァミ ノ)プロピル] - 2H - 1, 4 -べンズォキサジン 2塩酸塩
参考例 19で得た 3, 4-ジヒド口- 6- (3-ョ-ドプロピル) -4- (2 -ナフタレンス ルホニル)- 2H- 1,4-ベンズォキサジンを用いて、実施例 145と同様の操作を 行うことにより、 表題化合物を非晶状粉末として得た。
Ή-NMR (CDC13, フリー塩基) δ: 1.7-2.0 (2Η, m), 2.67 (4H, t, J = 7.0 Hz) ,
3.68 (2H, t, J = 4.4 Hz), 3.81 (2H, s), 3.91 (2H, t, J = 4. Hz), 6.68 (1H, d, J = 8.4 Hz), 6.88 (1H, dd, J = 8.4, 2.2 Hz), 7.1-7.3 (2H, m), 7.4-7.7 (3H, m), 7.7-8.0 (4H, m), 8.28 (1H, brs), 8.53 (2H, d, J = 6.2 Hz).
実施例 153
6- {3- [2 - (3 -ィンドリルェチル)ァミノ]プロピル) -3, 4ージヒド口- 4- (2 -ナフ 夕レンスルホニル) -2H-1 , 4-ベンズォキサジン 塩酸塩
9で得た 3,4-ジヒドロ- 6- (3-ョ-ドプロピル)- 4- (2-ナフタレンス ルホニル)- 2H-1, 4-ベンズォキサジンを用いて、実施例 145と同様の操作を 行うことにより、 表題化合物を非晶状粉末として得た。
Ή-NMR (CDC13, フリー塩基) δ 1.7-2.0 (2Η, m), 2.58 (2H, ί, 8.0 Hz), 2.69 (2H, t, J = 8.0 Hz), 2.8-3.1 (4H, m), 3.67 (2H, t, J = 4.4 Hz), 3.90 (2H, t, J = 4.4 Hz), 6.64 (1H, d, J = 8.4 Hz), 6.82 (1H, dd, J = 8.2, 2.0 Hz), 7.0-7.3 (3H, m), 7.3-7.4 (1H, m), 7.4-7.8 (5H, m), 7.8-8.0 (3H, m), 8.18 (1H, brs), 8.27 (1H, brs).
実施例 154
Ν,Ν-ジプロピル -[3,4-ジヒドロ- 3- (4 -メトキシフエ二ル)- 2Η - 1, 4-ベンズォ キサジン- 6-ィル]ァセトアミド
参考例 20で得た Ν,Ν-ジプロピル- [4- (4-メトキシベンゼン)力ルポニルメ トキシ -3-ニトロフエニル]ァセトアミドを用いて、 実施例 133と同様の操 作を行うことにより、 表題化合物を油状物として得た。
Ή-NMR (CDC13) δ: 0.8-1.0 (6H, m), 1.4-1.7 (4H, ni), 3.1-3.4 (4H, m), 3.56
(2H, s), 3.82 (3H, s), 3.8-4.0 (2H, m), 4.22 (1H, d, J = 10.6 Hz), 4.44 (1H, dd, J = 8.8, 3.0 Hz), 6.52 (1H, dd, J - 8.2, 2.2 Hz), 6.60 (1H, d, J = 2.2 Hz), 6.74 (1H, d, J = 8.2 Hz), 6.91 (2H, d, J = 8.8 Hz), 7.30 (2H, d, J = 8.8 Hz).
元素分析値 C23H3。N203として
計算値: C, 72.22; H, 7.91; N, 7.32.
実験値: C, 71.91; H, 8.10; N, 7.35.
実施例.155
3, 4-ジヒドロ- 6- [2- (N,N-ジプロピルアミノ)ェチル ]- 3-(4 -メトキシフエ二 リレ )- 2H_1,4-ベンズォキサジン 塩酸塩.
実施例 154で得た Ν,Ν-ジプロピル _ [3, 4-ジヒドロ- 3- (4-メトキシフエ二 ル) -2H-1, 4 -べンズォキサジン -6-ィル]ァセトアミドを用いて、実施例 133 と同様の操作を行うことにより、 表題化合物のフリ-塩基体を、 mp 85-90 °C の粉末として得た。得られた粉末に 規定塩酸 Z酢酸ェチル溶液を加えた後、 濃縮することにより表題化合物を非晶状粉末として得た。
Ή-NMR (CDClj, フリー塩基) δ: 0.91 (6Η, t, J = 7.4 Hz), 1.5-1.8 (4H, m), 1.6-1.8 (4H, m), 2.87 (4H, s), 3.82 (3H, s), 3.8-4.0 (2H, m), 4.23 ClH, dd, J = 10.6, 3.0 Hz), 4.43 (1H, dd, J = 8.8, 3.0 Hz), 6.4—6.6 (2H, m), 6.77 (1H, d, J = 8.8 Hz), 6.91 (2H, d, J = 8.8 Hz) , 7.30 (2H, d, J = 8.8 Hz).
実施例 156
4- [4- (4-クロロフェニル) -1-ピぺリジニル] -4-ォキソ -卜 [2- (トリフルォロ ァセチル)- 2, 3, 4, 5-テトラヒドロ- 1H- 2-ベンズァゼピン- 8-ィル] -卜ブ夕ノ ン
実施例 130の 1) で得た 4_ォキソ -4- [2- (トリフルォロアセチル) - 2, 3, 4, 5-テトラヒドロ- 1H- 2-ベンズァゼピン- 8 -ィル]ブタン酸を用いて、 実 施例 12と同様の操作を行うことにより、 表題化合物を粉末として得た。 Ή-腿 (CDC13) δ: 1.57-1.93 (6Η, m), 2.61-2.81 (4H, m), 3.06 (2H, m), 3.22 (1H, i), 3.33 (2H, m), 3.94 (2H, m), 4.13 (IH, i), .68-4.79 (3H, i), 7.13 (2H, m), 7.29 (3H, m), 7.88 (IH, m), 8.03 (IH, m).
融点: 153- 155 (結晶化溶媒:エタノ -ル-ジィソプロピルエーテル) 実施例 157 ,
4- [4- (4 -ク口口フエニル)ピぺリジン +ィル] -1- (2-ェチル- 2, 3, 4, 5-テトラ ヒドロ- 1H- 2-ベンズァゼピン- 8-ィル) -4-ォキソブタン-卜オン 塩酸塩
実施例 130で得た 4- [4- (4-クロ口フエ二ル)-卜ピペリジニル ]-4-ォキソ -1-(2, 3, 4, 5 -テトラヒドロ- 1H - 2 -ベンズァゼピン- 8-ィル) - 1-ブ夕ノンを用 いて、 実施例 17と同様の操作を行うことにより、 表題化合物を非晶状粉末 として得た。
Ή-NMR (DMS0-d6) δ: 1.27 (3Η, t, J = 7.4 Hz), 1.42 (1H, m), 1.63 (IH, m), 1.73-1.96 (4H, m), 2.51-2.89 (5H, in), 3.07 (4H, m), 3.22 (2H, m), 3.49 (2H, m), 4.10 (IH, m), 4.45-4.67 (3H, m), 7.27-7.46 (5H, m), 7.85 (2H, m), 10.47 (IH, m).
実施例 158
4- [4- (4-ク口口フエニル)ピぺリジン-トイル] - 1_ (2-ィソプロピル - 2, 3, 4, 5- テトラヒドロ- 1H- 2-ベンズァゼピン - 8-ィル) -4-ォキソブタン- 1-オン 塩酸
実施例 130で得た 4- [4- (4-クロ口フエ二ル)-卜ピペリジニル ]-4-ォキソ -1-(2,3,4, 5-テトラヒドロ- 1H - 2 -ベンズァゼピン- 8-ィル) -卜ブ夕ノンを用 いて、 実施例 17と同様の操作を行うことにより、 表題化合物を非晶状粉末 として得た。
Ή-NMR (DMS0-d6) δ: 1.31-1.44 (6Η, m), 1.55 (1H, m), 1.81-1.92 (3H, m), 2.07 (1H, m), .2.61 (1H, m), 2.74 (4H, m), 3.04 (1H, m), 3.24-3.30 (4H, ), 3.57 (3H, m), 4.08 (1H, i), 4.47-4.63 (3H, m), 7.24-7.46 (5H, i), 7.96 (2H, m), 9.89 (1H, m).
実施例 159 '
1 -(2-ベンジル- 2, 3, 4, 5 -テ卜ラヒドロ- 1H- 2 -べンズァゼピン- 8-ィル) -4- [4-
(4 -クロ口フエニル)ピぺリジン-卜ィル ]-4-ォキソブタン- 1-オン 塩酸塩
実施例 130で得た 4- [4- (4-クロ口フエ二ル)- 1-ピペリジニル ]_4-ォキソ - 1- (2, 3, 4, 5 -テ卜ラヒドロ- 1H-2-ベンズァゼピン- 8-ィル) -1 -ブ夕ノンを用 いて、 実施例 17と同様の操作を行うことにより、 表題化合物を非晶状粉末 として得た。
'H-NMR (DMS0-d6) 6: 1.37 (1H, m), 1.58 (1H, m), 1.74-1.85 (3H, m), 2.07 (1H, m), 2.65-2.89 (5H, m), 3.07-3.21 (6H, m), 4.08 (2H, m), 4.40-4.50 (3H, m), 4.73 (1H, m), 7.28-7.61 (10H, m), 7.96 (2H, m), 10.84 (1H, m). 実施例 160
4- [4- (4-クロ口フエニル)ピぺリジン-卜ィル]- 4-ォキソ -1 _ [2- (トリフルォ ロアセチル )-2, 3-ジヒド口- 1H-ィソインドール- 5-ィル]ブタン- 1-オン
実施例 132の 1) で得た 4-ォキソ -4- [2- (トリフルォロアセチル )-2, 3 - ジヒドロ- 1H-イソインド一ル -5-ィル]ブタン酸を用いて、 実施例 12と同様 の操作を行うことにより、 表題化合物を粉末として得た。 .
Ή-NMR (CDC13) δ: 1.58-1.67 (2Η, m), 1.84-1.96 (2H, m), 2.62-2.75 (2H, m), 2.86 (2H, t, J = 6.6 Hz), 3.19 (1H, t, J = 11.7 Hz), 3.33 (2H, t, J = 6.6 Hz), 4.12 (1H, m), 4.75 (1H, m), 4.97 (2H, s), 5.09 (2H, m), 7.13-7.46 (5H, m), 7.96-8.04 (2H, i).
実施例 161
4- [4- (4-クロ口フエニル)ピぺリジン-卜ィル] -1- (2-メチル- 2, 3 -ジヒドロ-
1H -ィソインドール- 5-ィル) -4-ォキソブタン-卜オン
実施例 132で得た 4 - [4-(4 -クロ口フエ二ル)ピぺリジン-卜ィル] -卜 (2,3-ジヒドロ- 1H-イソインドール- 5-ィル) -4-ォキソブ夕ン- 1-オンを用い て、 実施例 16と同様の操作を行うことにより、 表題化合物を粉末として得 た。
Ή-N R (CDC13) δ: 1.56-1.68 (2Η, m), 1.82-1.96 (2H, m), 2.63 (3H, s), 2.74 (2H, m), 2.84 (2H, t, J = 6.6 Hz), 3.17 (1H, m), 3.36 (2H, t, J = 6.6 Hz), 4.15 (1H, d, J = 15.6 Hz), 4.31 (4H, s), 4.76 (1H, d, J = 12 Hz), 7.11-7.36 (5H, m), 7.92 (2H, m).
実施例 162 '
4- [4- (4 -クロ口フエニル)ピペリジン-トイル]-卜(2-ェチル -2, 3-ジヒドロ-
1H -ィソインド一ル- 5-ィル) -4-ォキソブ夕ン-卜オン
実施例 132で得た 4- [4 - (4-クロ口フエニル)ピぺリジン- 1-ィル] -卜 (2, 3-ジヒドロ- 1H-イソインドール- 5-ィル) -4-ォキソブタン- 1-オンを用い て、 実施例 17と同様の操作を行うことにより、 表題化合物を粉末として得 た。
Ή-NMR (CDC13) δ 1.22 (3Η, t, J = 7.2 Hz), 1.26-1.62 (2H, m), 1.83- 1.94 (2H, m), 2.61-2.80 (6H, m), 3.17 (1H, m), 3.36 (2H, t, J = 6.6 Hz), 3.96 (4H, s), 4.15 (1H, d, J = 15.6 Hz), 4.76 (1H, d, J = 12 Hz), 7.11-7.36 (5H, m), 7.88 (2H, m).
実施例 163
4- [4- (4-クロ口フエニル)ピぺリジン- 1-ィル]- 1- (2-ィソプロピル- 2, 3-ジヒ ドロ- 1H-イソィンドール -5-ィル) -4-ォキソブタン- 1-オン
実施例 132で得た 4- [4- (4-クロ口フエニル)ピぺリジン- 1-ィル] -卜 (2, 3-ジヒドロ- 1 H-イソインド一ル- 5-ィル) -4-ォキソブタン-卜オンを用い て、 実施例 17と同様の操作を行うことにより、 表題化合物を粉末として得 た。
'Η-画 R (CDC13) δ: 1.21 (6Η, . d, J = 5.4 Hz), 1.62-1.80 (2H, m) , 1.83- 1.94 (2H, m), 2.61-2.82 (5H, m), 3.17 (1H, m), 3.36 (2H, t, J - 6.6 Hz), 4.00 (4H, s), 4.15 (1H, d, J = 15.6 Hz), 4.76 (1H, d, J = 12 Hz), 7.11-7.36 (5H, m), '7.88 (2H, m).
実施例 164
1 -(2-ベンジル- 2, 3 -ジヒドロ- 1H -ィソインド一ル- 5-ィル) -4- [4- (4-ク口口 フェニル)ピぺリジン- 1-ィル] -4 -才キソブタン- 1-オン
実施例 132で得た 4- [4- (4-クロ口フエニル)ピぺリジン- 1-ィル: N - (2, 3-ジヒドロ- III-イソインド一ル -5-ィル) -4-ォキソブタン-卜オンを用い て、 実施例 17と同様の操作を行うことにより、 表題化合物を粉末として得 た。
Ή-NMR (CDC13) δ 1.62-1.80 (2Η, m), 1.83-1.94 (2H, m), 2.59-2.82 (4H, m), 3.17 (1H, m), 3.36 (2H, t, J = 6.6 Hz), 3.93 (2H, s), 3.97 (4H, s), 4.15 (1H, d, J = 15.6 Hz), 4.76 (1H, d, J = 12 Hz), 7.18, (2H, m), 7.29-7.42 (8H, m), 7.88 (2H, m) .
実施例 165
4- (3-ィソプロピル- 2, 3, 4, 5-テトラヒド口- m-3 -ベンズァゼピン- 7-ィル) - 4 -ォキソ -N- (3-フエニルプロピル)ブタンアミド 塩酸塩
実施例 42で得た 4-ォキソ -N - (3-フエニルプロピル) - 4-(2, 3, 4, 5-テトラ ヒドロ- 1H-3-ベンズァゼピン- 7-ィル)ブタンアミド トリフルォロ酢酸塩を 用いて、 実施例 17と同様の操作を行うことにより、 表題化合物を非晶状粉 末として得た。
Ή-NMR (DMS0 - d6) δ: 1.04 (3Η, d, J = 6.3 Hz), 1.27 (6H, d, J = 6.3 Hz), 1.64 (1H, m), 2.91-3.23 (6H, m), 3.60-3.79 (10H, m), 7.17-7.40 (6H, m), 7.85 (2H, m), 11.0 (1H, m).
実施例 166
N -(卜メチル -3-フエニルプロピル)- 4-ォキソ -4- (2, 3, 4, 5 -テトラヒド Π-1Η- 3 -ベンズァゼピン- 7-ィル) -ブタンアミド 塩酸塩
実施例 36と同様にして表題化合物を非晶状粉末として得た。
Ή-NMR (DMS0— d6) δ: 1.05 (3Η, d, J = 6.6 Hz), 1.65 (2H, m), 2.50-2.60 (6H, m), 3.19 (8H, m), 3.75 (1H, ), 4.37 (1H, m), 7.17-7.40 (6H, ), 7.86-7.96 (2H, m), 9.53 (1H, m).
実施例 167
4- (3-イソプロピル- 2, 3,4, 5 -テトラヒドロ- 1H-3-ベンズァゼピン- 7-ィル) - N -(卜メチル -3-フエニルプロピル )-4_ォキソブタンアミド 塩酸塩
実施例 166で得た N- (卜メチル -3-フエニルプロピル)- 4-ォキソ - 4 - (2,3,4, 5 -テトラヒドロ- 1H - 3-ベンズァゼピン- 7 -ィル) -ブタンアミド 塩酸 塩を用いて、 実施例 17と同様の操作を行うことにより、 表題化合物を非晶 状粉末として得た。
'H-NMR (DMS0— d6) δ: 1.05 (3Η, d, J = 6.3Hz), 1.27 (6H, d, J = 6.3Hz), 1.67 (2H, m), 2.92-3.23 (6H, m), 3.57-3.79 (5H, m), 3.99-4.05 (5H, m), 7.17-7.40 (6H, m), 7.86-7.96 (2H, m), 10.97 (1H, m).
実施例 1 '68
4 -ォキソ- N- (2 -フエノキシェチル) 4- [3- (トリフルォ口ァセチル) -2, 3, 4, 5- テトラヒドロ- 1H-3-ベンズァゼピン- 7-ィル]ブタンアミド
参考例 16で得た 4-ォキソ -4- [3- (トリフルォロアセチル )-2, 3, 4, 5-テト ラヒドロ -1H- 3-ベンズァゼピン- 7-ィル]ブタン酸を用いて、 実施例 12と同 様の操作を行うことにより、 表題化合物を粉末として得た。
Ή-NMR (CDC13) δ: 2.66 (2Η, t, J = 6.6 Hz), 3.03 (4H, m), 3.34 (2H, t,
J = 6.6 Hz), 3.67 (4H, m), 3.78 (2H, m), 4.04 (1H, d, J = 4.8 Hz), 6.23 (1H, m), 6.89, (3H, m), 7.24(3H, m), 7.78 (2H, m).
実施例 169
4 -ォキソ -N - (2 -フエノキシェチル) -4- (2, 3, 4, 5-テトラヒドロ- 1H - 3-ベンズ ァゼピン- 7_ィル)ブタンアミド
実施例 168で得 4-ォキソ -N_(2-フエノキシェチル)4- [3- (トリフルォ 口ァセチル) -2, 3, 4, 5-テトラヒドロ- 1H - 3-ベンズァゼピン -7 -ィル]ブ夕ンァ ミドを用いて、 実施例 13と同様の操作を行うことにより、 表題化合物を粉 末として得た。
Ή-NMR (CDC13) δ 2.26 (1H, s), 2.65 (2H, t, J = 6.6 Hz), 2.98 (8H, m), 3.34 (2H, t, J = 6.6 Hz), 3.67 (2H, q, J = 5.1 Hz) , 4.04 (2H, t, J = 4.8 Hz), 6.28 (1H, m), 6.89, (3H, m), 7.24(3H, m), 7.71 (2H, i).
実施例 170
N- [3- (4-クロロフェニル)プロピル] -4-ォキソ -4- [3- (トリフルォロァセチ ル〉 -2,.3, 4, 5 -テトラヒドロ- m- 3-ベンズァゼピン- 7 -ィル]ブタンアミド
参考例 16で得た 4-ォキソ -4- [3- (トリフルォロアセチル )-2, 3, 4, 5 -テト ラヒドロ- 1H- 3-ベンズァゼピン- 7-ィル]ブタン酸と参考例 23で得た 3- (4 - クロ口フエニル)プロピルアミンを用いて、実施例 12と同様の操作を行うこ とにより、 表題化合物を油状物として得た。
'Η -丽 R (CDC13) δ 1.73-1.85 (2H, ra), 2.60 (4H, m), 3.05 (4H, m), 3.24-3.34 (4H, m), 3.77-3.80 (4H, m), 5.87 (1H, m), 7.09-7.28 (5H, m), 7.77 (2H, m).
実施例 171
N- [3 - (4-クロロフエニル)プロピル] -4一ォキソ一 4— (2, 3, 4, 5 -テトラヒドロ-
1H-3- ド 塩酸塩
実施例 170で得た [3- (4-ク口口フエニル)プロピル] -4-ォキソ -4- [3- (トリフルォロアセチル) - 2, 3, 4, 5-テトラヒドロ- 1H - 3 -ベンズァゼピン- 7 -ィ ル]ブタンアミドを用いて、 実施例 13と同様の操作を行うことにより、表題 化合物を非晶状粉末として得た。
Ή-NMR (CDC13) 'δ: 1.73-1.85 (2Η, q, J = 7.4 Hz), 2.56-2.72 (6H, m), 2.96 (7H, m), 3.21-3.37 (4H, m), 5.94 (1H, m), 7.07-7.28 (5H, m), 7.75 (2H, m).
実施例 172
4-ォキソ- N- (4-フェニルブチル) -4- [3- (トリフルォロアセチル )-2, 3, 4, 5 -テ トラヒドロ- 1H - 3_ベンズァゼピン- 7-ィル]プタンアミド
参考例 16で得た 4-ォキソ -4- [3- (トリフルォロアセチル )-2, 3, 4, 5-テト ラヒドロ- 1H- 3-ベンズァゼピン- 7-ィル]ブタン酸を用いて、 実施例 12と同 様の操作を行うことにより、 表題化合物を油状物として得た。
Ή-NMR (CDC13) δ 1.54-1.70 (4Η, m 2.60 (4H, q, J = 6.6 Hz), 3.05 (4H, m), 3.24-3.34 (4H, m), 3.69-3.81 (4H, m 5.73 (1H, m), 7.15-7.32 (6H, m), 7.78 (2H, m).
実施例 173
4 -ォキソ -N- (4 -フエニルブチル) -4- (2, 3, 4, 5-テトラヒド口- 1H- 3-ベンズァ ゼピン- 7-ィル)ブタンアミド 塩酸塩
実施例 172で得た 4-ォキソ -N- (4-フエ二ルブチル)- 4- [3- (トリフルォロ
ァセチル)- 2, 3, 4, 5-テトラヒド口- 1H- 3_ベンズァゼピン- 7 -ィル] を用いて、 実施例 13と同様の操作を行うことにより、 表題化合物を非晶状粉末として 得た。
Ή-NMR (CDC13) δ 1.54-1.65 (4Η, m), 2.48-2.61 (5H, m), 3.01 (8H, m), 3.26-3.49 (4H, m), 5.79 (1H, m), 7.11-7.28 (6H, m), 7.73 (2H, ra). 実施例 174
N- [3- (4-ク口口フエニル)プロピル] - 4 -ォキソ -4- (3-ィソプロピル _2, 3, 4, 5- テトラヒドロ- 1H- 3-ベンズァゼピン- 7-ィル)ブタンアミド
実施例 171で得た N- [3- (4-ク口口フエニル)プロピル ] -4-ォキソ -4 -
(2, 3, 4, 5 -テトラヒドロ- 1H-3-ベンズァゼピン- 7 -ィル)ブタンアミド 塩酸塩 を用いて、 実施例 17と同様の操作を行うことにより、 表題化合物を粉末と して得た。
Ή— NMR (CDC13) δ: 1.03 (6Η, d , J = 6.6 Hz), 1.77 (2H, m), 2.57-2.66 (9H, m), 2.96 (4H, in), 3.23-3.34 (4H, m), 5.92 (1H, m), 7.07-7.28 (5H, m), 7.75 (2H, m).
実施例 175
4- (3-ィソプロピル- 2, 3, 4, 5-テトラヒド口- 1H-3-ベンズァゼピン -7-ィル) -
4 -ォキソ -N -(2-フエノキシェチル) -ブタンアミド
実施例 169で得た 4-ォキソ (2-フエノキシェチル )-4- (2, 3, 4, 5-テト ラヒドロ- 1H- 3-ベンズァゼピン -7-ィル)ブタンアミドを用いて、 実施例 17 と同様の操作を行うことにより、 表題化合物を粉末として得た。
Ή-NMR (CDC13) δ: 1.02 (6H, d, J = 6.6 Hz), 2.65 (7H, m), 2.95 (4H, m), 3.34 (2H, t, J = 6.6 Hz), 3.67 (2H, q, J = 5.1 Hz), 4.04 (2H, t, J = 4.8 Hz), 6.23 (1H, m), 6.89, (3H, m), 7.24(3H, m), 7.71 (2H, m).
実施例 1 7 6
N- [2- [4- (4-クロロフェニル) -1-ピぺリジニル] - 2 -ォキソェチル] -2, 3, 4, 5- テトラヒドロ- 1H- 3-ベンズァゼピン- 7-力ルポキサミド トリフルォロ酢酸
参考例 2 2で得た 2- [4- (4-ク口口フエニル) -1-ピぺリジニル] -2-ォキソェ チルァミン 塩酸塩を用いて、 実施例 3 6と同様にして表題化合物を得た。 MS (APCi) (M+l): 26.
実施例 1 Ί 7
N - [2- [4- (2-メチルフエニル) -1-ピぺリジニル] -2-ォキソェチル] -2, 3, 4, 5- テトラヒドロ- 1H- 3-ベンズァゼピン- 7 -カルボキサミド トリフルォロ酢酸
参考例 2 3で得た 2- [4- (2-メチルフエニル) -卜ピペリジニル ] -2-ォキソェ チルァミン 塩酸塩を用いて、 実施例 3 6と同様にして表題化合物を得た。 MS (APCI) (M+l) : 406. ,
実施例 1 7 8
Ν - [2- [4- (4-フルオロフェニル) -卜ピ,ペラジニル] -2-ォキソェチル] - 2, 3, 4, 5-テトラヒドロ -1H-3-ベンズァゼピン- 7-力ルポキサミド トリフル ォロ酢酸塩
参考例 2 4で得た 2- [4- (4-フルオロフェニル) -卜ピペラジニル] -2-ォキソ ェチルァミン 2塩酸塩を用いて、実施例 3 6と同様にして表題化合物を得た MS (APCI) (M+1) : 411.
実施例 1 7 9
N- [2- [4- (2-メトキシフエニル) -卜ピペラジニル ] -2-ォキソェチル] -
2, 3, 4, 5-テトラヒドロ- 1H- 3-ベンズァゼピン- 7-力ルポキサミド トリフル ォロ酢酸塩
参考例 2 5で得た 2- [4- (2-メトキシフエ二ル) - 1 -ピペラジニル ] -2-ォキソ ェチルァミン 2塩酸塩を用いて、実施例 3 6と同様にして表題化合物を得た。 MS (APCI) (M+1) : 423.
実施例 1 8 0
N - [2- [4- (4-クロ口フエニル) -卜ピペリジニル ] -2-ォキソェチル ] -2, 3, 4, 5- テトラヒドロ- 1H-2-ベンズァゼピン- 8-力ルポキサミド トリフルォロ酢酸
参考例 2 2で得た 2 - [4- (4-クロ口フエ二ル) - 1 -ピぺリジニル] -2-ォキソェ チルァミン 塩酸塩を用いて、 実施例 3 6と同様にして表題化合物を得た。 MS (APCI) (M+1) : 426.
実施例 1 8 1
N - [2- [4- (2-メチルフエニル) -1 -ピぺリジニル] -2-ォキソェチル] -2, 3, 4, 5- テトラヒドロ- 1H- 2-ベンズァゼピン- 8-カルボキサミド トリフルォロ酢酸 塩
参考例 2 3で得た 2- [4- (2-メチルフエニル) -卜ピペリジニル ] -2-ォキソェ チルァミン 塩酸塩を用いて、 実施例 3 6と同様にして表題化合物を得た。 MS (APCI) (M+1) : 406.
実施例 1 8 2
N - [2- [4- (4 -フルォ口フエニル) -卜ピペラジニル] -2-ォキソェチル] -
2, 3, 4, 5 -テトラヒドロ- 1H- 2-ベンズァゼピン- 8 -力ルポキサミド トリフル ォロ酢酸塩
参考例 2 4で得た 2- [4- (4-フルオロフェニル ) -1-ピペラジニル ] -2-ォキソ ェチルァミン 2塩酸塩を用いて、実施例 3 6と同様にして表題化合物を得た。 MS (APCI) (M+1) : 411.
実施例 1 8 3
N- [2- [4- (2-メトキシフエ二ル) -卜ピペラジニル] -2-ォキソェチル] - 2, 3, 4, 5 -テトラヒドロ- 1H-2 -ベンズァゼピン- 8 -力ルポキサミド トリフル ォロ酢酸塩
参考例 2 5で得た 2_ [4- (2-メトキシフエニル) -卜ピペラジニル ] -2-ォキソ ェチルァミン 2塩酸塩を用いて、実施例 3 6と同様にして表題化合物を得た c MS (APCI) (M+1) : 423.
実施例 1 8 4
4 - [4- (4-メチルフエニル) - 1-ピぺリジニル] - 4-ォキソ - 1- (2, 3, 4, 5-テトラヒ ドロ- 1H - 3-ベンズァゼピン- 7-ィル) -1-ブタノン
1) 参考例 16で得た 4-ォキソ -4- [3- (トリフルォロアセチル ) -2, 3, 4, 5- テトラヒドロ- 1H- 3-ベンズァゼピン- 7-イリレ]ブタン酸を用いて、 実施例 12 と同様の操作を行うことにより、 4- [4- (4-メチルフエニル) -卜ピぺリジニ ル]- 4 -ォキソ -卜 [3 -(トリフルォロアセチル) - 2, 3, 4, 5 -テトラヒドロ- 1H - 3- ベンズァゼピン- 7-ィル] - 1-ブ夕ノンを無色粉末として得た。
'H-NMR (CDC13) δ: 1.55-2.01 (4Η, m), 2.33 (3H, s), 2.57-2.91 (4H, m), 2.97-3.27 (5H, m), 3.34 (2H, t, J=6.4Hz), 3.66-3.84 (4H, m), 4.05-4.19 (1H, m), 4.67-4.83 (1H, m), 7.04-7.30 (5H, m), 7.80-7.91 (2H, m). 融点: 132-134 °C (結晶化溶媒: ジェチルエーテル) '
2) 上記 1) で得た 4 - [4- (4-メチルフエニル) - 1 -ピペリジニル ]-4-ォキ ソ- 1- [3- (トリフルォロァセチル) -2, 3, 4, 5-テトラヒド口 -1H- 3-ベンズァゼ ピン- 7-ィル ]_1 -ブタノンを用いて、実施例 13と同様の操作を行うことによ り、 表題化合物を無色粉末として得た。
Ή-NMR (CDC13) δ: 1.47-2.00 (5Η, m), 2.33 (3H, s), 2.55-3.04 (12H, i), 3.06-3.26 (1H, m), 3.35 (2H, t, J=6.8Hz), 4.04-4.20 (1H, m), 4.68-4.85 (1H, m), 7.05-7.24 (5H, m), 7.74-7.84 (2H, m) .
融点: 115- 116 °C (結晶化溶媒: ジェチルエーテル)
'実施例 1 85
4- [4- (3-メチルフエニル) -1-ピぺリジニル] -4-ォキソ -1 -(2, 3, 4, 5 -テトラヒ ド口- 1H- 3 -べンズァゼピン- 7-ィル) -トブ夕ノン
1) 参考例 16で得た 4-ォキソ -4- [3- (トリフルォロアセチル )-2, 3, 4, 5 - テトラヒドロ- 1H- 3-ベンズァゼピン- 7-ィル]ブタン酸を用いて、 実施例 12 と同様の操作を行うことにより、 4- [4- (3-メチルフエニル) -1-ピベリジ二 ル] - 4-ォキソ -卜 [3 -(トリフルォロアセチル )-2, 3, 4, 5 -テ卜ラヒド D-1H-3- ベンズァゼピン- 7-ィル] -卜ブタノンを無色粉末として得た。
!H-NMR (CDC13) δ: 1.55-2.01 (4Η, m), 2.35 (3H, s), 2.56-2.93 (4H, m), 2.98-3.27 (5H, m), 3.34 (2H, t, J=6.4Hz), 3.67-3.84 (4H, m), 4.05-4.20 (1H, m), 4.68-4.83 (1H, m), 6.96-7.10 (3H, m), 7.14-7.31 (2H, m), 7.80-7.92 (2H, m).
融点: 128- 129 °C (結晶化溶媒: ジェチルエーテル)
2) 上記 1) で得た 4-[4- (3-メチルフエニル) -卜ピペリジニル ]-4-ォキ ソ-卜 [3- (トリフルォロアセチル) -2, 3, 4, 5-テトラヒドロ- 1H- 3-ベンズァゼ ピン- 7-ィル] -卜ブ夕ノンを用いて、実施例 13と同様の操作を行うことによ り、 表題化合物を無色粉末として得た。
¾-NMR (CDC13) δ 1.45-2.00 (5Η, ), 2.34 (3H, s), 2.56-3.03 (12H, m), 3.05-3.26 (1H, m), 3.35 (2H, i, J=6.6Hz), 4.05-4.20 (1H, m), 4.69-4.85 (1H, m), 6.95-7.08 (3H, m), 7.14-7.23 (2H, m), 7.74-7.83 (2H, m). 融点: 91-93 °C (結晶化溶媒: ジェチルエーテル)
実施例 186
4 - [4- (2 -メチルフエニル )-1-ピペリジニル ]-4-ォキソ -1- (2, 3, 4, 5 -テトラヒ ドロ- 1H- 3 -べンズァゼピン- 7 -ィル) -卜ブ夕ノン
1 ) 参考例 16で得た 4 -ォキソ -4- [3- (トリフルォロアセチル) - 2, 3, 4, 5- テトラヒドロ- 1H- 3-ベンズァゼピン- 7-ィル]ブタン酸を用いて、 実施例 12 と同様の操作を行うことにより、 4- [4-(2-メチルフエニル) -卜ピベリジ二 ル]- 4-ォキソ -1- [3- (卜リフルォロアセチル) - 2, 3, 4, 5-テトラヒド D-1H-3-
ベンズァゼピン -7_ィル] -卜ブタノンを無色粉末として得た。 '
Ή-NMR (CDC13) δ: 1.47-1.95 (4Η, m), 2.37 (3H, s), 2.58-2.77 (IH, m), 2.80-3.30 (8H, m), 3.35 (2H, t, J=6.6Hz), 3.65-3.85 (4H, m), 4.07-4.23 (IH, m), 4.72-4.87 (IH, m), 7.10-7.32 (5H, m), 7.80-7.92 (2H, m). 融点: 145-147 °C (結晶化溶媒: ジェチルェ一テル)
2) 上記 1) で得た 4- [4- (2-メチルフエニル) -1-ピペリジニル ]-4-ォキ ソ-ト [3- (トリフルォロアセチル) -2, 3, 4, 5-テトラヒドロ- 1H-3 -べンズァゼ ピン- 7-ィル] -卜ブ夕ノンを用いて、実施例 13と同様の操作を行うことによ り、 表題化合物を無色粉末として得た。
Ή-NMR (CDC13) δ: 1.50-1.96 (5Η, m), 2.37 (3H, s), 2.57-2.76 (IH, m), 2.79-3.28 (12H, m), 3.36 (2H, t, J=6.6Hz), 4.08-4.24 (IH, i), 4.72-4.87 (IH, m), 7.05-7.23 (5H, m), 7.75-7.84 (2H, m).
融点: 93-95 X: (結晶化溶媒: ジェチルエーテル)
実施例 187
4- [4- (4-フルォ口フエニル) -卜ピぺリジニル] -4-ォキソ-卜(2, 3, 4, 5-テトラ ヒド口 -1Η- 3-ベンズァゼピン- 7-ィル) - 1-ブタノン
1) 参考例 16で得た 4-ォキソ - 4- [3- (トリフルォロアセチル) - 2, 3,4, 5 - テトラヒドロ- 1H- 3-ベンズァゼピン- 7-ィル]ブタン酸を用いて、 実施例 12 と同様の操作を行うことにより、 4- [4- (4-フルォ口フエニル) -卜ピぺリジニ ル] -4-ォキソ - 1 - [3- (トリフルォロアセチル) -2, 3, 4, 5 -テトラヒド Π-1Η-3- ベンズァゼピン- 7-ィル] -卜ブタノンを無色粉末として得た。
】H-腿 (CDC13) δ: 1.53-2.01 (4Η, m), 2.57-2.90 (4H, m), 2.97-3.28 (5H, m) , 3.34 (2H, t, J=6.6Hz) , 3.65-3.84 (4H, m) , 4.05-4.20 (IH, m) , 4.68-4.84 (1H, m), 6.95-7.07 (2H, m), 7.10-7.32 (3H, m), 7.80-7.90 (2H, m). 融点: 105-108 °C (結晶化溶媒: ジェテルエーテル)
2) 上記 1) で得た 4- [4- (4-フルオロフェニル) -卜ピペリジニル ]-4 -才 キソ- 1- [3 -(トリフルォロアセチル )-2, 3, 4, 5 -テトラヒドロ- 1H- 3 -べンズァ ゼピン- 7-ィル] -卜ブ夕ノンを用いて、実施例 13と同様の操作を行うことに より、 表題化合物を無色粉末として得た。
Ή-NMR (CDC13) δ : 1.47-2.00 (5Η, m), 2.57-2.90 (4H, m), 2.98 (8H, br), 3.07-3.27 (1H, m), 3.35 (2H, t, J=6.8Hz), 4.06-4.21 (1H, m), 4.70-4.86 (1H, m), 6.94-7.07 (2H, m), 7.10-7.24 (3H, m), 7.74-7.84 (2H, m). 融点: 127- 128 °C (結晶化溶媒: ジェチルエーテル)
実施例 188
4- [4- (4-メ卜キシフエ二ル)- 1 -ピペリジニル]—4ーォキソ-卜 (2, 3, 4, 5-テトラ ヒドロ- 1H-3 -べンズァゼピン -7-ィル) - 1 -ブタノン
1) 参考例 16で得た 4-ォキソ -4 - [3- (トリフルォロアセチル )-2, 3,4, 5- テトラヒドロ- 1H- 3-ベンズァゼピン- 7-ィル]ブタン酸を用いて、 実施例 12 と同様の操作を行うことにより、 4- [4- (2-メチルフェニル) -1-ピぺリジニ ル]- 4-ォキソ -1 - [3- (トリフルォロアセチル) - 2, 3, 4, 5-テ卜ラヒドロ- 1H - 3- ベンズァゼピン- 7-ィル] -卜ブ夕ノンを無色粉末として得た。
Ή-NMR (CDC13) δ 1.50-1.74 (2Η, m), 1.80—1.97 (2H, m), 2.59-2.78 (2H, m), 2.85 (2H, t, J=6.6Hz), 3.00-3.09 (4H, m), 3.12-3.24 (1H, in), 3.34 (2H, t, J=6.6Hz), 3.67-3.83 (7H, m), 4.07-4.16 (1H, m), 4.71-4.80 ClH, m), 6.86 (2H, d, J=8.6Hz), 7.13 (2H, d, J=8:6Hz), 7.23-7.30 (1H, m), 7.80-7.90 (2H, m).
融点: 130-131 °C (結晶化溶媒: ジェチルェ一テル)
2) 上記 1 ) で得た 4- [4- (2-メチルフエニル) -卜ピぺリジニル] -4 -^キ ソ -1- [3- (トリフルォロアセチル) - 2, 3, 4, 5-テトラヒド口- 1H- 3-ベンズァゼ ピン- 7-ィル] -卜ブ夕ノンを用いて、実施例 1 3と同様の操作を行うことによ
り、 表題化合物を無色粉末として得た。 .
'H-NMR (CDC13) δ: 1.51-1.97 (5Η, m), 2.58-2.77 (2H, m), 2.83 (2H, t, J=6.7Hz), 2.97 C8H, br), 3.10-3.23 (1H, m), 3.35 (2H, t, J=6.7Hz), 3.80 (3H, s), 4.07-4.18 (1H, m), 4.73-4.83 (1H, m), 6.86 (2H, d, J=8.7Hz), 7.13 (2H, d, J=8.7Hz), 7.19 (1H, d, J=8.3Hz), 7.76-7.83 (2H, m) .
融点: 99- 100 °C (結晶化溶媒: ジェチルエーテル)
実施例 189
4_ [4- ( - 7ロロフエ二ル) - 1-ピペリジニル ]-1- (2-メチル- 1, 2, 3, 4 -テトラヒ ドロ- 7-イソキノリニル) - 4 -ォキソ -1-ブタノン
実施例 13で得た 4- [4- (4-ク口口フエニル)ピぺリジン- 1-ィル] -4-ォキソ - 1 -(1, 2, 3, 4-テトラヒドロイソキノリン- 7-ィル)ブ夕ン- 1-オンを用いて、実 施例 16と同様の操作を行うことにより、表題化合物を無色粉末として得た。' Ή-NMR (CDC13) (5: 1.62 (2H, m), 1.89 (2H, m), 2.48 (3H, s), 2.67-2.70 (4H, in), 2.82 (2H, t, J = 6.4 Hz), 2.97 (2H, t, J = 5.4 Hz), 3.23 (1H, m), 3.34 (2H, t, J = 6.6 Hz), 3.62 (2H, s), 4.13 (1H, d, J = 15.6 Hz), 4.76 (1H, d, J = 12 Hz), 7.11-7.31 (5H, m), 7.71-7.81 (2H, m).
融点: 139- 140 °C (結晶化溶媒: エタノール-ジイソプロピルエーテル) 実施例 190
4- [4- (4 -ク口口フエニル) -卜ピぺリジニル] -卜(2-ェチル -1, 2, 3, 4 -テトラヒ ドロ- 7 -イソキノリニル) - 4一ォキソ -卜ブタノン
実施例 13で得た 4- [4- (4-ク口口フエニル)ピぺリジン- 1-ィル] -4-ォキソ - 1 -(1,2, 3, 4-テトラヒドロイソキノリン - 7_ィル)ブタン - 1 -オンを用いて、実
施例 1 7と同様の操作を行うことにより、表題化合物を無色粉末として得た ( Ή-NMR (CDC13) δ: 1.21 (3Η, ί, J = 7.2 Hz), 1.62 (2H, m), 1.89 (2H, m), 2.57-2.79 (6H, m), 2.82 (2H, i, J = 6.4 Hz), 2.97 (2H, t, J = 5.4 Hz), 3.23 (1H, m), 3.34 (2H, t, J = 6.6 Hz), 3.62 (2H, s), 4.13 (1H, d, J - - 15.6 Hz), 4.76 (1H, d, J = 12 Hz), 7.11-7.31 (5H, m), 7.71-7.81 (2H, m). 融点: U5- 116 °C (結晶化溶媒: エタノール-ジイソプロピルエーテル) ' 実施例 1 9 1
1-(2-ベンジル- 1 , 2, 3, 4-テトラヒド口- 7 -ィソキノリニル) -4- [4- (4 -クロ口 フエ二ル)- 1-ピベリジニル] - 4 -ォキソ - 1-ブ夕ノン
実施例 1 3で得た 4- [4- (4-クロ口フエニル)ピペリジン- 1-ィル] -4-ォキソ -1- (1,2, 3, 4 -テトラヒドロイソキノリン- 7-ィル)ブタン- 1-オンを用いて、実 施例 1 7と同様の操作を行うことにより、表題化合物を無色粉末として得た。 Ή-NMR (CDC13) 6 1.62 (2H, m), 1.89 (2H, m), 2.58-2.80 (6H, m), 2.95 (2H, t, J = 5.4 Hz), 3.23 (1H, m), 3.34 (2H, t, J = 6.6 Hz), 3.67 (2H, s), 3.70 (2H, s), 4.13 (1H, d, J = 15.6 Hz), 4.76 (1H, d, J = 12 Hz), 7.11-7.41 (10H, m), 7.62-7.80 ' (2H, ) . ' 融点: 102- 103 °C (結晶化溶媒: エタノ一ル-ジィソプロピルエーテル) 実施例 1 92
4 - [4- (4-クロ口フエニル) - 1-ピペリジニル] - 1 -(2-イソプロピル- 1 , 2, 3, 4 -テ 卜ラヒド口- 7-ィソキノリニル) - 4 -ォキソ -1-ブタノン
実施例 1 3で得た 4- [4-(4-クロ口フエュ - 1 -ィル] -4 -ォキソ
1-オンを用いて、実
施例 17と同様の操作を行うことにより、表題化合物を無色粉末として得た。 Ή-NMR (CDC13) δ: 1.15 (6Η, d, J = 6.6 Hz), 1.62 (2H, m), 1.89 (2H, m), 2.59-2.95 (9H, m), 3.18 (1H, m), 3.34 (2H, t, J = 6.6 Hz), 3.77 (2H, s), 4.13 (1H, d, J = 15.6 Hz), 4.76 (1H, d, J = 12 Hz), 7.11-7.31 (5H, m), 7.73-7.80 (2H, m).
融点: 113- 115 °C (結晶化溶媒: エタノ一ル-ジィソプロピルェ一テル) 実施例 193
4一 [4— (4—クロ口フエニル)ピぺリジン—卜ィル]—卜(3—シクロへキシルメチルー
2,3,4, 5-テトラヒドロ- 1H-3-ベンズァゼピン- 7-ィル) -4-ォキソブタン- 1 -ォ ン
実施例 15で得た 4 - [4 - (4 -クロ口フエニル) - 1 -ピペリジニル ]-4 -ォキソ -
1- (2, 3, 4, 5-テトラヒドロ- 1H - 3-ベンズァゼピン- 7-ィル) -卜ブ夕ノンを用い て、 実施例 17と同様の操作を行うことにより、 表題化合物を無色粉末とし て得た。
Ή-NMR (CDC13) δ: 0.90 (2H, m), 1.24 (4H, m), 1.47-1.94 (10H, m), 2.23 (2H, d, J = 6.9 Hz), 2.58-2.80 (5H, m), 2.94 (2H, t, J = 6.4 Hz), 2.96 (4H, m), 3.23 (1H, m), 3.35 (2H, t, J = 6.6 Hz), 4.13 (1H, m), 4.76 (1H, m), 7.35-7.11 (5H, m), 7.79 (2H, m).
融点: 140- 141 °C (結晶化溶媒: ェ夕ノール -ジィソプロピルエーテル) 実施例 194
4 - [4- (4-ク口口フエニル) -卜ピぺリジニル] -4-ォキソ -1- [3- (テトラヒドロ-
2-フラニルメチル) -2, 3, 4, 5テトラヒドロ- 1H- 3 -べンズァゼピン- 7-ィル] - 1 -
実施例 1 5で得た 4- [4- (4-ク口口フエニル) -卜ピぺリジニル] -4-ォキソ - 1 -(2, 3, 4, 5 -テトラヒドロ- 1H- 3 -ベンズァゼピン- 7-ィル) -卜ブ夕ノンを用い て、 実施例 1 7と同様の操作を行うことにより、 表題化合物を無色粉末とし て得た。
MS (ESI) (M+H): 509.
融点: 123- 125 °C (結晶化溶媒: エタノール-ジイソプロピルエーテル) 実施例 1 9 5
4- [4- (4 -クロロフエ二ル)- 1-ピペリジニル ] -1- (3-シクロへキシル- 2, 3, 4, 5 テトラヒドロ- 1H- 3-ベンズァゼピン- 7-ィル) -4-ォキソ -卜ブタノン
実施例 1 5で得た 4- [4- (4-クロ口フエニル) -卜ピぺリジニル] -4-ォキソ- 1- (2, 3, 4, 5-テトラヒドロ- 1H- 3 -ベンズァゼピン- 7-ィル) -卜ブ夕ノンを用い て、 実施例 1 7と同様の操作を行うことにより、 表題化合物を無色粉末とし て得た。
MS (ESI) ( IH): 507.
融点: 128- 130 (結晶化溶媒: エタノール-ジイソプロピルエーテル) 実施例 1 9 6 .
4 - [4 - (4-クロロフエ二ル) - 1-ピペリジニル] -卜(3-シク口ペンチル- 2, 3, 4, 5 テトラヒドロ- 1H- 3-ベンズァゼピン- 7-ィ.ル) - 4-ォキソ -1-ブタノン
実施例 15で得た 4- [4- (4-クロ口フエニル) -卜ピペリジニル ]-4-ォキソ - 1- (2, 3, 4, 5-テトラヒドロ- 1H- 3-ベンズァゼピン- 7-ィル) - 1-ブタノンを用い て、 実施例 17と同様の操作を行うことにより、 表題化合物を無色粉末とし て得た。
Ή-N R (CDC13) δ: 1.55-1.69 (5Η, m), 1.83 (3H, m), 2.59-3.03 (17H, ι), 3.17 (1H, ra), 3.35 (2H, t, J .= 6.6 Hz), 4.13 (1H, m), 4.76 (1H, ra), 7.35-7.11 (5H, m), 7.79 (2H, m) .
融点: 160-162 °C (結晶化溶媒: エタノール-ジイソプロピルエーテル) 実施例 1 97
4- [4- (4 -クロ口フエニル) -卜ピぺリジニル] -1- (3-ィソブチル -2, 3, 4, 5テト ラヒドロ- 1H- 3-ベンズァゼピン- 7-ィル) -4 -ォキソ -卜ブ夕ノン
実施例 1 5で得た 4- [4- (4-ク口口フエニル) - 1-ピぺリジニル] -4-ォキソ - 1 -(2, 3, 4, 5 -テトラヒドロ- 1H - 3-ベンズァゼピン -7-ィル) - 1-ブタノンを用い て、 実施例 17と同様の操作を行うことにより、 表題化合物を無色粉末とし て得た。
Ή-NMR (CDC13) d: 0.93 (6H, d, J = 6.2 Hz), 1.62 (4H, m), 1.89 (3H, m), 2.21 (2H, d, J = 7.4 Hz), 2.60-2.74 (6H, ra), 2.79 (2H, t, J = 6.4 Hz), 2.95 (4H, m), 3.23 (1H, m), 3.35 (2H, t, J = 6.6 Hz), 4.13 (1H, m), 4.76 (1H, m), 7.35-7.11 (5H, m), 7.79 (2H, m).
融点: 137- 138 °C (結晶化溶媒: エタノール-ジイソプロピルエーテル) 実施例 1 98
4 - [4- (4 -メチルフエニル) -1-ピぺリジニル] -1 - (3 -メチル- 2, 3, 4, 5テトラヒ ドロ- 1H - 3-ベンズァゼピン- 7-ィル) -4-ォキソ -卜ブ夕ノン
実施例 184で得た 4- [4- (4-メチルフエニル) -卜ピペリジニル ]-4-ォキソ - 1-(2, 3, 4, 5-テトラヒド口- 1H-3 -ベンズァゼピン- 7 -ィル)- 1-ブタノンを用 いて、 実施例 16と同様の操作を行うことにより、 表題化合物を無色粉末と して得た。
Ή-NMR (CDC13) δ: 1.66 (2Η, m), 1.89 (2H, m), 2.33 (3H, s), 2.38 (3H, s), 2.65 (6H, ), 2.82 (2H, t, J = 6.4 Hz), 2.95 (4H, m), 3.23 (1H, m), 3.35 (2H, t, J = 6.6 Hz), 4.13 (1H, m), 4.76 (1H, m), 7.35-7.11 (5H, m), 7.79 (2H, m).
融点: 111-112 °C (結晶化溶媒: エタノ一ル-ジィソプロピルエーテル) 実施例 199
ト(3 -ィソプロピル - 2, 3, 4, 5 -テトラヒドロ- 1H- 3-ベンズァゼピン- 7 -ィル) - 4 - [4- (4-メチルフエ二ル)- 1-ピペリジニル ]-4-ォキソ -1-ブ夕ノン 塩酸塩
実施例 184で得た 4- [4- (4-メチルフエ二ル)- 1-ピペリジニル ]-4-ォキソ -1-(2, 3, 4, 5-テ卜ラヒドロ- 1H-3-ベンズァゼピン- 7 -ィル) -卜ブ夕ノンを用 いて、 実施例 17と同様の操作を行うことにより、 表題化合物を無色粉末と して得た。
■H-NMR (CDC13) δ: 1.26 (7Η, m), 1.56 (1H, m), 1.78 (2H, m), 2.26 (3H, s), 2.50 (1H, m), 2.73 (2H, m), 2.94-3.64 (7H, m), 4.05 (1H, m), 4.46 (1H, m), 7.12 (4H, s), 7.40 (1H. d, J = 8.4 Hz), 7.83 (2H, m).
融点: 180 °C (decomp.) (結晶化溶媒: エタノール-ジイソプロピルェ一テ ル) '
実施例 200
4 - [4- (4 -メチルフェニル)ピぺリジン-卜ィル] - 4_ォキソ - 1 - (1 , 2, 3, 4-テトラ
参考例 15で得た 4 -ォキソ -4- [2- (トリフルォロアセチル) - 1, 2, 3, 4—テト ラヒドロ -7-イソキノリニル]ブタン酸を用いて、 実施例 12および実施例 1 3と同様の操作を順次行うことにより、 表題化合物を無色粉末として得 fこ。
Ή-NMR (CDC13) δ: 1.63 (2Η, m), 1.95 (3H, m), 2.33 (3H, s), 2.59-2.72 (3H, m), 2.82 (4H, m), 2.97 (2H, t, J = 5.4 Hz), 3.17 (2H, t, J = 6.2 Hz), 3.34 (2H, t, J = 6.6 Hz), 4.08 (2H, s), 4.13 (1H, d, J = 15.6 Hz), 4.76 (1H, d, J = 12 Hz), 7.11-7.20 (5H, m), 7.71-7.81 (2H, m).
融点: 119- 120 (結晶化溶媒: ェ夕ノ一ル-ジィソプロピルエーテル) 実施例 201
4 - [4- (4-メチルフエ二ル)- 1-ピペリジニル (2 -メチル -1, 2, 3, 4-テトラヒ ドロ- 7-イソキノリニル) - 4 -ォキソ -1 -ブ夕ノン
実施例 200で得た 4- [4- (4-メチルフエニル)ピペリジン- 1-ィル] -4-ォキ ソ- 1 -(1, 2, 3, 4 -テトラヒドロイソキノリン -7-ィル)ブタン -1-オンを用いて、 実施例 16と同様の操作を行うことにより、 表題化合物を無色粉末として得 た。
Ή-NMR (CDC13) δ: 1.62 (2Η, m), 1.89 (2H, ra), 2.34 (3H, s), 2.48 (3H, s), 2.60-2.73 (4H, m), 2.82 (2H, t, J = 6.4 Hz), 2.97 (2H, t, J = 5.4 Hz), 3.23 (1H, m), 3.34 (2H, t, J - 6.6 Hz), 3.62 (2H, s), 4.13 (1H, d, J二 15.6 Hz), 4.76 (1H, d, J = 12 Hz), 7.11-7.31 (5H, m), 7.71-7.81 (2H, m).
融点: 97- 99 (結晶化溶媒: エタノ一ル-ジィソプロピルエーテル) 実施例 202
ト(2 -ィソプロピル- 1, 2, 3, 4 -テトラヒド口- 7-ィソキノリ二ル)- 4- [4- (4-メ チルフエニル) - 1-ピベリジニル] - 4 -ォキソ -卜ブ夕ノン
実施例 200で得た 4- [4- (4-メチルフエニル)ピペリジン-卜ィル] -4-ォキ ソ -1- (1,2, 3, 4-テトラヒドロイソキノリン- 7-ィル)プタン- 1-オンを用いて、 実施例 17と同様の操作を行うことにより、 表題化合物を無色粉末として得 た。
Ή-N R (CDC13) δ: 1.15 (6H, d, J = 6.6 Hz), 1.62 (2H, m), 1.89 (2H, m), 2.64 (3H, s), 2.65-2.95 (9H, m), 3.18 (1H, m), 3.34 (2H, t, J = 6.6 Hz), 3.77 (2H, s), 4.13 (1H, d, J = 15.6 Hz), 4.76 (1H, d, J = 12 Hz), 7.11-7.31 (5H, HI), 7.73-7.80 (2H, m).
融点: 78-80 °C (結晶化溶媒: エタノ一ル -ジィソプロピルエーテル) 実施例 20 3
1 -(2-ベンジル- 1, 2, 3, 4-テトラヒドロ- 7-ィソキノリニル) -4- [4 - (4 -メチル フエニル) -卜ピベリジニル] -4-ォキソ-卜ブタノン塩酸塩
実施例 200で得た 4- [4- (4-メチルフエニル)ピペリジン-卜ィル] -4-ォキ ソ -Γ- (1, 2, 3, 4 -テトラヒドロイソキノリン- 7-ィル)ブタン- 1-オンを用いて、 実施例 17と同様の操作を行うことにより、 表題化合物を無色粉末として得 た。
Ή-NMR (CDC13) δ: 1.36 (1H, m), 1.56 (1H, m), 1.78 (2H, m), 2.26 (3H, s), 2.50 (1H, in), 2.73 (2H, m), 3.08-3.43 (8H, m), 3.67 (1H, in), 4.05
(1H, m), 4.46 (4H, m), 7.12 (4H, s), 7.41 (1H. d, J = 8.4 Hz), 7.53 (3H, m), 7.67 (2H, m), 7.86 (2H, m).
融点: 72 °C (decomp) (結晶化溶媒: エタノール-ジイソプロピルエーテル) 実施例 204
5- [4- (4 -クロロフェニル) - 1 -ピぺリジニル] - 5 -ォキソ -1- [3 - (トリフルォロ ァセチル) -2, 3, 4, 5 -テトラヒドロ- 1H- 3_ベンズァゼピン- 7 -ィル] - 1_ペン夕
2, 3, 4, 5-テトラヒドロ- 1H - 3-ベンズァゼピンを用いて、 参考例 15および 実施例 12と同様の操作を順次行うことにより、 表題化合物を無色非晶状粉 末として得た。
Ή NMR (CDC13) δ: 1.57 (2Η, ι), 1.89 (2H, m), 2.10 (2H, i), 2.49 (2H, m), 2.58-2.76 (2H, m), 3.01-3.17 (7H, m), 3.75 (4H, m), 4.04 (1H, m), 4.79 (1H, m), 7.11 (2H, m), 7.28 (3H, m), 7.82 (2H, m).
実施例 205
5- [4- (4-/7ロロフエニル) -卜ピペリジニル ]-5-ォキソ -1 -(2, 3, 4, 5-テトラヒ ドロ- 1H- 3-ベンズァゼピン- 7-ィル) -卜ペン夕ノン
実施例 204で得た 5- [4- (4-クロ口フエニル) -卜ピペリジニル] -5-ォキソ - 1-[3 -(トリフルォロアセチル) - 2, 3, 4, 5 -テ卜ラヒドロ- 1H- 3 -べンズァゼピ ン -7-ィル] -卜ペンタノ; を用いて、実施例 13と同様の操作を行うことによ り、 表題化合物を無色粉末として得た。
Ή NMR (CDC13) δ: 1.57 (2Η, m), 1.87 (2H, m), 2.10 (2H, m), 2.48 (2H, m), 2.58-2.75 (2H, m), 2.96 (8H, m), 3.10 (3H, m), 4.04 (1H, m), 4.79
(1H, m), 7.11 (2H, m), 7.18 (1H, m), 7.28 (2H, m), 7.73 (2H, m). FABMS (pos) 439 [M+H]+.
融点: 112- 113 °C (結晶化溶媒: 酢酸ェチル -ジイソプロピルエーテル) 実施例 206
tert-ブチル 8- [3- [4- (4-クロ口フエニル) -卜ピペリジニル]プロポキシ ]- 1, 3, 4, 5-テトラヒド口- 2H-2-ベンズァゼピン- 2-カルポキシレート
参考例 27で得た tert -ブチル 8-ヒドロキシ- 1, 3, 4, 5-テトラヒドロ- 2H- 2 -ベンズァゼピン- 2 -カルボキシレ一ト (l.OOg, 3.80mmol) 、 3-ブロモ -1 -ク ロロプロパン (0.451ml, 4.56mmol) と炭酸カリウム (2.62g, 19.0廳 ol) の ジメチルホルムアミド (10ml) 溶液を 80°Cで 3時間攪拌した。 得られる溶液 に酢酸ェチルを加え、 飽和食塩水で洗浄し、 無水硫酸ナトリウムで乾燥した。 溶媒を減圧下濃縮後、 得られた残查をアルミナカラムクロマトグラフィー (展開溶媒;酢酸ェチル) により精製した。 得られた油状物、 および 4-(4-ク ロロフエ二ル)ピぺリジン (882mg, 3.80顧 ol) 、 炭酸カリウム (2.62g, 19.0删 ol) 、 ヨウ化ナトリウム (569mg, 3.80mmol) のジメチルホルムアミド
(10ml) 溶液を 80°Cで 3時間攪拌した。 得られる溶液に酢酸ェチルを加え、 飽和食塩水で洗浄し、 無水硫酸ナトリウムで乾燥した。溶媒を減圧下濃縮後、 得られた残査をシリカゲルカラムクロマトグラフィー (展開溶媒;へキサ ン:酢酸ェチル =3: 1) により精製して、 表題化合物 (1.25g) を得た。 'Η醒 R (CDC13) δ: 1.41 (9Η, s), 1.72-1.82 (6H, m), 1.96-2.05 (4H, m), 2.48-2.58 (3H, m), 2.88 (2H, m), 3.03-3.09 (2H, m), 3.66 (2H, m), 4.01 (2H, m), 4.32-4.39 (2H, m), 6.66-6.75 (2H, m), 7.01-7.05 (1H, m), 7.15 (2H, d, J = 8.6 Hz), 7.26 (2H, d, J = 8.6 Hz).
実施例 207
8 - [3- [4- (4 -ク口口フエニル) -卜ピペリジニル〕 プロポキシ ]-2, 3, 4, 5 -テト
実施例 206で得た tert-ブチル 8- [3- [4- (4-クロ口フエ二ル)- 1-ピペリ ジニル]プロポキシ ]-1, 3, 4, 5 -テトラヒド口- 2H-2-ベンズァゼピン- 2-力ルポ キシレート (l,10g, 2.20mmol) のトリフルォロ酢酸 (10ml) 溶液を 1時間攪 拌後、 減圧下濃縮した。 得られた油状物に酢酸ェチルを加え、 炭酸カリウム 水溶液と飽和食塩水で洗浄し、 無水硫酸ナトリウムで乾燥した。 溶媒を減圧 下濃縮後、 得られた残査をへキサンにより粉末として、 表題化合物 (682mg) を得た。
'H MR (DMS0 - d6) δ: 1.57-2.03 (10H, Bi), 2.43 (3H, ffl), 2.78 (2H, m), 3.00 (4H, m), 3.72 (2H, m), 3.96 (2H, m), 6.55-6.70 (2H, m), 7.02 (1H, d, J = 8.0 Hz), 7.24-7.36 (4H, m).
融点: 97- 99 °C (結晶化溶媒:ジイソプロピルエーテル-へキサン) 実施例 208
8 - [3- [4- (4-ク口口フエニル) -卜ピぺリジニル]プロボキシ] -2-メチル-
2, 3, 4, 5 -テトラヒドロ- 1H- 2 -ベンズァゼピン塩酸塩
実施例 207で得た 8- [3- [4- (4-クロ口フエ二ル)- 1-ピベリジニル] プロ ポキシ] - 2, 3, 4, 5-テトラヒドロ- 1H- 2-ベンズァゼピンを用いて、 実施例 16 'と同様の操作を行うことにより、 表題化合物を無色非晶状粉末として得た。 'HNMR (CDC13, フリー塩基) δ: 1.71-1.80 (6Η, m), 1.96-2.07 (4H, m), 2.31 (3H, s), 2.45-2.57 (3H, m), 2.81 (2H, m), 2.98-3.09 (4H, m), 3.75 (2H, s), 3.99 (2H, t, J = 6.3 Hz), 6.65-6.71 (2H, m), 7.01 (1H, d, .J = 7.2 Hz), 7.15 (2H, d, J = 8.7 Hz), 7.26 (2H, d, J = 8.7 Hz).
実施例 209
2 -ァセチル- 8- [3- [4- (4-ク口口フエニル) -卜ピぺリジニル]プロポキシ] - 2, 3, 4, 5-テトラヒドロ- 1H-2-ベンズァゼピン 塩酸塩
実施例 207で得た 8- [3- [4- (4-クロ口フエニル) -卜ピペリジニル] プロ ポキシ ]-2, 3, 4, 5-テトラヒド口- 1H- 2-ベンズァゼピンと無水酢酸を用いて、 実施例 17と同様の操作を行うことにより、 表題化合物を無色非晶状粉末と して得た。
Ή NMR (DMS0-d6) δ: 1.84 (2Η, m), 2.01 (2H, m), 2.32 (3H, s), 2.47-2.62 (4H, ι), 2.75-2.95 (5H, m), 3.24 (2H, m), 3.70-3.82 (4H, m), 4.09 (2H, m), 4.57 (2H, m), 6.72-6.90 (2H, m), 7.09 (1H, m), 7.21-7.30 (4H, m). 実施例 210
4 - [4- (4-ク口口フエニル) - 1 -ピぺリジニル] -1- (3 -ィソプロピル- 2, 3, 4, 5-テ トラヒド口- 1H- 3-ベンズァゼピン -7-ィル) - 1-ブ夕ノン 2塩酸塩
実施例 34で得た 4- [4- (4-ク口口フエニル) -1-ピぺリジニル] -1- (2, 3, 4, 5-テトラヒド口- 1H- 3-ベンズァゼピン- 7-ィル) -卜ブタノンを用いて、 実施例 17と同様の操作を行うことにより、 表題化合物を無色粉末として得 た。
!H- MR (CDClg) δ : 1.02 (6Η, d, J = 6.6Hz), 1.62-1.74 (6H, m), 1.93-2.05
(4H, m), 2.44 (2H, t like), 2.63-2.67 (2H, m), 2.89-3.05 (10H, m),
7.09-7.27 (5H, m), 7.72-7.75 (2H, m).
融点: 236 °C (deco即) (結晶化溶媒: 酢酸ェチル -へキサン)
実施例 211
1- (3-ベンジル- 2, 3, 4, 5-テトラヒドロ- 1H - 3 -べンズァゼピン -7-ィル) -4- [4- (4-ク口口フエニル) -卜ピぺリジニル] -卜ブタノン
実施例 34で得た 4- [4- (4-ク口口フエニル) - 1-ピぺリジニル ]- 1- (2, 3,4, 5-テトラヒドロ- 1H- 3-ベンズァゼピン- 7-ィル) -1-ブタノンを用いて、 実施例 17と同様の操作を行うことにより、 表題化合物を無色粉末として得 た。
!H-NMR (CDClj) δ : 1.60-1.79 (6H, m), 1.96-2.08 (4H, m), 2.43 (2H, t like), 2.61-2.65 (2H, 1) , 2.94-3.04 (9H, m), 3.63 (2H, s), 7.09-7.36 (10H, m), 7.71-7.75 (2H, m).
融点: 99- 100 °C (結晶化溶媒: 酢酸ェチル -へキサン)
実施例 212
4 - [4- (4-クロ口フエ二ル)- 1-ピペリジニル ]-1-(3 -ィソプロピル- 2, 3, 4, 5-テ トラヒドロ- 1H- 3-ベンズァゼピン- 7-ィル) -4 -ォキソ - 1 -ブタノール
実施例 30で得た 4- [4- (4-ク口口フエ二ル)- 1-ピペリジニル ]-1- (3-ィソ プロピル- 2, 3, 4, 5-テトラヒド口- m-3-ベンズァゼピン- 7-ィル) -4-ォキソ - 1 -ブ夕ノン (0.50 g, 1.07匪 ol) のメタノール (20 mL) 懸濁液に、 水素化 ホウ素ナトリウム(81 mg, 2.14薦 ol)を添加して、 室温で 30分間攪拌した。 反応溶液を減圧下濃縮し、 残査を酢酸ェチルー水で分配した。 酢酸ェチル層 を飽和食塩水で洗浄し、 硫酸マグネシウムで乾燥した。 減圧下溶媒を留去し て、 表題化合物を非晶状粉末として得た。
½ー賺 (CDC13) δ : 1.02 (6Η, d, J = 6.6Hz), 1.54-1.63 (2H, m), 1.85-1.91 (2H, br in), 2.05-2.17 (2H, m), 2.54 (2H, ί like), 2.66-2.78 (6H, m),
2.89-2.93 (5H, m), 3.12 (1H, m), 3.95 (IH, br d), 4.72-4.85 (2H, m); 7.04-7.14 (5H, m), 7.30-7.31 (2H, m) .
実施例 213
7- [ (E) -4- [4- (4-ク口口フエニル) -1-ピぺリジニル] -4-ォキソ -卜ブテニル] - 3 -イソプロピル- 2, 3, 4, 5 -テトラヒド口- 1H- 3-ベンズァゼピン塩酸塩
実施例 212で得た 4 - [4 - (4 -クロ口フエニル) -卜ピペリジニル] - 1 -(3-ィ ソプロピル - 2, 3, 4, 5-テトラヒドロ- 1H- 3-ベンズァゼピン- 7-ィル) -4-ォキソ -卜ブ夕ノール (O. g, 0.30 mmol)および p-トルエンスルホン酸一水和物 (0.03g, 0.16画 ol )のトルエン (10 mL)溶液を 24時間加熱還流した。 反応溶 液を減圧下濃縮し、 得られた残査をアルミナカラムクロマトグラフィー (展 開溶媒;へキサン:酢酸ェチル = 1 : 1) で精製して、 表題化合物のフリー 塩基体 0.09 gを無色非晶状粉末として得た。得られた粉末を酢酸ェチルに溶 解し、 氷冷下に 4 N塩酸-酢酸ェチルで処理して、 表題化合物 0.04 gを無色 非晶状粉末として得た。
腿(CDC13) δ : 1.02 (6Η, d, J = 6.6Hz), 1.50-1.71 (2H, m), 1.86-1.92 (2H, m), 2.57-2.72 (6H, m), 2.87-3.00 (5H, m), 2.64 (IH, m), 3.34 (2H, d, J = 6.2Hz), 4.01-4.07 (IH, br d like), 4.78-4.85 (1H, br d like), 6.26-6.37 (IH, m), 6.46 (IH, d, J = 16.2Hz), 7.05-7.29 (7H, m).
実施例 2 1 4
1 -(3-ァセチル- 2, 3, 4, 5 -テトラヒドロ- 1H- 3-ベンズァゼピン- 7-ィル) -4- [4- (4-ク口口フエ二ル)- 1-ピぺリジニル] - 1-ブ夕ノール
実施例 33で得た卜(3-ァセチル- 2,3,4, 5-テトラヒドロ- 1H-3-ベンズァゼ
ピン- 7 -ィル) -4- [4- (4 -クロロフエニル) -1-ピぺリジニル] - 1-プ夕ノンを用 いて、 実施例 212と同様の操作を行うことにより、 表題化合物を.無色粉末 として得た。
Ή-NMR (CDC13) (5: 1.50-2.27 (14H, m), 2.42-2.60 (3H, m), 2.85-2.97 (4H, m), 3.01-3.10 (1Η, ι), 3.23-3.32 (1H, m), 3.47-3.82 (4H, m), 4.64 (1H, brd, J 5.4Hz), 7.05-7.30 (7H, m).
融点: 113- 114 °C (結晶化溶媒: ジェチルエーテル)
実施例 215
3 -ァセチル- 7- [ (E) -4- [4- (4-クロ口フエニル) -卜ピぺリジニル] -卜ブテニ ル] -2, 3, 4, 5 -テトラヒド口- 1H- 3-ベンズァゼピン
実施例 214で得た卜(3 -ァセチル- 2,3,4, 5-テトラヒドロ- 1H-3-ベンズァ ゼピン- 7-ィル) -4- [4- (4-ク口口フエ二ル)- 1-ピぺリジニル] -卜ブ夕ノ一ル を用いて、 実施例 213と同様の操作を行うことにより、 表題化合物を無色 粉末として得た。
Ή-NMR (CDC13) δ: 1.57-1.90 (4Η, m), 2.04-2.17 (2H, m), 2.19 (3H, s),
2.39-2.58 (5H, m), 2.84-2.95 (4H, m), 3.05-3.15 (2H, m), 3.52-3.61 (2H, m), 3.68-3.77 (2H, m), 6.13-6.27 (1H, ra), 6.39 (1H, d, J = 15.7Hz),
7.03-7.20 (5H, m), 7.23-7.30 (2H, m).
融点: 153- 155 t: (結晶化溶媒: ジェチルエーテル)
実施例 216
N - [2- (4-クロロフエノキシ)ェチル] -4-ォキソ- 4- [3- (トリフルォロァセチ ル) -2, 3, 4, 5 -テトラヒド口- 1H-3 -べンズァゼピン -7 -ィル]ブタンアミド
参考例 16で得た 4-ォキソ -4- [3- (トリフルォロアセチル )-2, 3, 4, 5 -テト
ラヒド口- lH- 3-ベンズァゼピン- 7-ィル]ブタン酸と参考例 26で得た 2- (4 - クロロフエノキシ)ェチルァミンを用いて、実施例 12と同様の操作を行うこ とにより表題化合物を油状物として得た。 . !H-NMR (CDC13) δ 2.65 (2Η, ί, J = 6.6 Hz), 3.02 (4H, ), 3.32 (2H, ί, J = 6.6 Hz), 3.62-3.69 (4H, m), 3.78 (2H, in) , 3.97 (2H, t, J = 5.4 Hz), 6.24 (1H, m), 6.81 (2H, m)', 7.22-7.28 (3H, m), 7.78 (2H, m).
実施例 217
N- [2- (4-クロロフエノキシ)ェチル] -4-ォキソ- 4- (2, 3, 4, 5-テトラヒドロ-
1H - 3-ベンズァゼピン- 7-ィル)ブタンアミド 塩酸塩
実施例 2 16で得た N- [2 - (4-クロロフエノキシ)ェチル ]-4-ォキソ -4- [3- (トリフルォロアセチル )-2, 3, 4, 5-テトラヒドロ- 1H- 3 -ベンズァゼピン- 7-ィ リレ]ブタンアミドを用いて、実施例 1 3と同様の操作を行うことにより表題化 合物を非晶状粉末として得た。
Ή-NMR (CDC13, フリー塩基) (5: 2.02 (1H, m), 2.65 (2H, t, J = 6.6 Hz), 2.99 (8H, m), 3.33 (2H, t, J = 6.6 Hz), 3.66 (2H, m), 3.97 (2H, t, J = 5.4 Hz), 6.31 (1H, m), 6.81 (2H, m), 7.16-7.27 (3H, m), 7.70 (2H, m). 実施例 21 8
N - [3- (4 -クロ口フエニル)プロピル] - N -メチル- 4 -ォキソ - 4 - [3- (トリフルォ ロアセチル )-2, 3, 4, 5-テトラヒドロ- 1H- 3 -ベンズァゼピン- 7-ィル]ブタンァ Sド
3- (4-クロ口フエニル)プロピルアミン (1.69 g, 9.96画 ol)と 37%ホルムァ ルデヒド水溶液 (0.811 ml, 10.0 mmol)をギ酸 (10 ml)中、 100°Cで 7時間加 熱撹拌した。 得られる混合液を室温に冷却後、 ギ酸を留去し、 8N水酸化ナト リウム水溶液を加えてアルカリ性にし、 酢酸ェチルで抽出した。 抽出液を飽
和 NaCl水溶液で洗浄し、 無水硫酸マグネシウムで乾燥した。溶媒を減圧下に 留去して得られた残査、参考例 16で得た 4-ォキソ -4- [3- (トリフルォロアセ チル)- 2, 3, 4, 5 -テトラヒドロ- 1H- 3-ベンズァゼピン- 8-ィル]ブタン酸 (3.4 g, 9.96丽 ol)とトリエチルァミン (1.39 ml, 9.96 mmol)をジメチルホルム アミド (5 ml)中室温で 30分攪拌し、 0°Cに冷却後、 シアノリン酸ジェチル (1.51 ml, 9.96 mmol)を加えた。 得られる混合液を 1時間攪拌した後、 水に 注ぎ、 酢酸ェチルで抽出した。 抽出液を飽和 NaCl水溶液で洗浄し、 無水硫酸 マグネシウムで乾燥した。 溶媒を減圧下に留去した後、 シリカゲルカラムク 口マトグラフィー (展開溶媒;酢酸ェチル:へキサン =1 : 1) で精製し、 表題 化合物 1.44 gを油状物として得た。
Ή-NMR (CDC13) δ: 1.86 (2Η, m), 2.57-2.80 (4H, m), 3.05 (7H, m), 3.30-3.36 (4H, m), 3.77-3.79 (4H, m), 7.10-7.33 (5H, m), 7.76 (2H, m). 実施例 219
N— [3- (4-ク口口フエニル)プロピル] -N-メチル -4-ォキソ - 4 - (2, 3, 4, 5-テトラ ヒドロ- 1H- 3-ベンズァゼピン- 7-ィル)ブタンアミド
実施例 218で得た N- [3- (4-クロ口フエニル)プロピル] -N-メチル -4-ォキ ソ- 4- [3- (トリフルォロアセチル )-2, 3, 4, 5-テトラヒドロ- 1H- 3-ベンズァゼ ピン- 7-ィル]ブタンアミドを用いて、 実施例 13と同様の操作を行うことに より表題化合物を非晶状粉末として得た。
Ή-NMR (CDC13, フリー塩基) 6: 1.76-2.05 (3H, m), 2.51-2.68 (6H, m), 3.00 (7H, m), 3.24-3.41 (4H, in), 3.90 (2H, m), 7.07-7.30 (5H, m), 7.76 (2H, m), '
実施例 220 '
(E) -3- (ジメチルァミノ)-卜 [卜 [ [6- (4-メチルフェニル) -3-ピリジニル]カル ポニル ]-1,2, 3, 4-テトラヒドロ- 6-キノリニル] -2-プロペン-卜オン
1) 6-ァセチル- 1,2, 3, 4-テトラヒドロキノリンと 6- (4 -メチルフエニル) ニコチン酸を用いて、参考例 5と同様の操作を行うことにより、卜 [1- [[6- (4 - メチルフエニル) -3 -ピリジニル]力ルポニル] - 1 , 2, 3, 4-テトラヒド口- 6-キノ リニル]エタノンを淡黄色粉末として得た。
Ή-NMR (DMSO— d6) δ 2.00 (2Η, m), 2.36 (3H, s), 2.49 (3H,'s), 2.93 (2H, dd, J=6.3 and 6.6Hz), 3.83 (2H, dd, J=6.1 and 6.3Hz), 7.00 (1H, d, J=9.3Hz), 7.30 (2H, d, J=8.1Hz), 7.52 (1H, dd, J=l.5 and 8.3Hz), 7.83 (2H, in), 7.95 (1H, d, J=8.3Hz), 8.01 (2H, d, J=8.1Hz), 8.59 (1H, m).
2) 上記 1)で得た卜 [1- [[6- (4-メチルフエ二ル)- 3-ピリジニル]力ルポ 二ル]- 1, 2, 3, 4 -テトラヒドロ- 6-キノリニル]エタノンを用いて、 参考例 6と 同様の操作を行うことにより、 表題化合物を淡黄色結晶として得た。
'H-NMR (DMSO— d6) <5: 2.00 (2H, tt, J=6.3, 6.3Hz), 2.35 (3H, s), 2.87 (3H, br s), 2.91 (2H, t, J=6.3Hz), 3.11 (3H, br s), 3.83 (2H, t, J=6.3Hz), 5.78 (1H, d, J=12.5Hz), 6.86 (1H, d, J=8.1Hz), 7.30 (2H, d, J=8.3Hz), 7.66 (1H, d, J=12.5Hz), 7.80 (3H, m), 7.94 (1H, d, J=8.3Hz), 8.00 (2H, d, J=8.1Hz), 8.57 (1H, m).
実施例 221
(E) - N, N-ジメチル- 3- [1- [ [6- (4-メチルフエニル) -3-ピリジニル] 力ルポ二 ル]- 1,2,3, 4 -テトラヒドロ- 6 -キノリニル]- 2 -プロペン-卜ァミン 塩酸塩
実施例 220で得た (E)- 3- (ジメチルァミノ)-卜 D- [[6- (4-メチルフエ二 ル)- 3 -ピリジニル]力ルポニル] - 1, 2, 3, 4 -テトラヒドロ- 6-キノリニル] - 2 -プ 口ペン- 1-オンを用いて、実施例 4および実施例 5と同様の操作を順次行うこ とにより、 表題化合物を黄色結晶として得た。
Ή-NMR (DMSO— d6) δ: 1.98 (2Η, m), 2.36 (3H, s), 2.70 (3H, s), 2.71 (3H, s), 2.86 (2H, t, J=6.3Hz), 3.00 (2H, m), 3.79 (2H, t, J= 6.3Hz), 5.66 (1H, m), 6.98 (2H, s), 7.24 (1H, s), 7.31 (2H, d, J=8.1Hz), 7.86 (1H, m), 7.96 (1H, m), 8.00 (2H, d, J=8.1Hz), 8.57 (1H, m), 10.42 (1H, br s). 実施例 222
1 - [卜 [(4-フエ二ル-卜ピペリジニル)力ルポ二ル]- 1, 2, 3, 4-テトラヒドロ- 6- キノリエル]- 3- (卜ピロリジニル) -卜プロパノン
参考例 28で得た 1- [(4 -フエ二ル- 1-ピベリジニル)力ルポ二ル]- 1, 2,3,4- テトラヒドロキノリンを用いて、 参考例 7および参考例 8と同様の操作を順 次行うことにより、 表題化合物を無色液体として得た。
Ή-NMR (CDC13) δ 1.70 (2Η, m), 1.79 (4H, m), 1.84 (2H, ra), 2.01 (2H, m), 2.56 (4H, m), 2.69 (1H, m), 2.84 (2H, t, J=6.6Hz), 2.89 (2H, dd, J=7.0 and 8.0Hz), 2.91 (2H, m), 3.14 (2H, dd, J=7.0 and 8.0Hz), 3.64 (2H, t, J=5.8Hz), 4.05 (2H, in), 7.02 (1H, d, J=8.8Hz), 7.19-7.33 (5H, m), 7.73 (2H, m).
実施例 223
1_ [ (4-フエ二ル- 1 -ピぺリジニル)力ルポニル] -6- [ (E) -3- (卜ピロリジニル) - 卜プロべニル] - 1 , 2, 3, 4 -テトラヒドロキノリン 塩酸塩
実施例 222で得た卜 [卜 [(4-フエニル-卜ピベリジニル)力ルポニル] - 1,2,3, 4 -テトラヒドロ- 6 -キノリニル] - 3- (1-ピロリジニル) -卜プロパノンを 用いて、 実施例 4および実施例 5と同様の操作を順次行うことにより、 表題 化合物を黄色非晶状粉末として得た。
'H-NMR (DMS0-d
6) δ: 1.70 (2Η, m), 1.83 (2H,
1.97 (2H, m), 2.07 (2H, m), 2.23 (2H, m), 2.68 (1H, m), 2.79 (2H, m), 2.88 (4H, m), 3.64 (2H, m), 3.72 (2H, m), 3.78 (2H, m), 4.00 (2H, m), 6.32 (1H, m), 6.82 (1H, d, J=15.8Hz), 7.14-7.33 (8H, m), 12.54 (1H, br s) . 製剤例 1
(1) 実施例 1で得られた化合物 ¾ 0 mg
(2) ラク卜ース 34mg
(3) トウモロコシ澱粉 1 0. 6 mg
(4) トウモロコシ澱粉 (のり状) 5mg
(5) ステアリン酸マグネシウム 0. 4mg
(6) カルポキシメチルセルロースカルシウム 2 Omg 一
計 12 Omg
常法に従い上記 (1) - (6) を混合し、 錠剤機を用いて打錠することに より、 錠剤が得られる。
製剤例 2
(1) 実施例 5で得られた化合物 t? Omg
(2) ラク卜ース 34mg
(3) トウモロコシ澱粉 1 0. 6 mg
(4) トウモロコシ澱粉 (のり状) 5mg
(5) ステアリン酸マグネシウム 0. 4mg
(6) カルポキシメチルセル口一スカルシゥム 2 Omg
計 12 Omg
常法に従い上記 (1) 〜 (6) を混合し、 錠剤機を用いて打錠することに より、 錠剤が得られる。 参考例 1一 1 ラット脳由来 cDNAを用いた PCR法によるラット SLC- 1 受容体 cDNAの増幅
ラット脳由来 poly (A) ¾NA (クロ一ンテック社) を錶型とし、 ランダムプ ライマーを用いて逆転写反応を行なった。逆転写反応は、夕カラ RNA.PCRver. 2キットの試薬を使用した。次にこの逆転写生成物を錶型として用い、配列番 号: 1および 2の合成 DNAプライマーを用いて PCR法による増幅を行なった。 合成 DNAプライマーは受容体蛋白に翻訳される領域の遺伝子が増幅されるよ うに構築したが、 その際に遺伝子の 5'側に制限酵素 Sal Iの認識する塩基配 列が付加され、 また 3'側に制限酵素 Spe Iの認識する塩基配列が付加される ように、 側および 3' 側にそれぞれの制限酵素の認識配列を付加した。 反 応液の組成は、 cDNA铸型 5 a 1、合成 DNAプライマー各 0.4 ^ M、0.25mMdNTPs、 pfu (ス卜ラタジーン社) DNAポリメラ一ゼ 0.5 n 1および酵素に付属のパッ ファーで、総反応量は 50 a 1とした。増幅のためのサイクルはサーマルサイ クラ一 (パーキンエルマ一社) を用い、 94°C · 60秒の加熱の後、 94°C * 60秒、 60°C · 30秒、 72°C · 150秒のサイクルを 35回繰り返し、最後に 72°Cで 10分間 反応させた。 増幅産物の確認は、 0.8%ァガロースゲル電気泳動の後、 ェチ ゥムブ口マイド染色によって行なった。
参考例 1 _ 2 PCR産物のプラスミドベクタ一へのサブクローニングおよび 挿入 cDNA部分の塩基配列の解読による増幅 cDNA配列の確認
参考例 1一 1で行なった PCR後の反応産物は 0.8 %の低融点ァガ口一スゲ ルを用いて分離し、 パンドの部分をカミゾリで切り出した後、 細片化、 フエ ノール抽出、 フエノール'クロ口ホルム抽出、エタノール沈殿を行なって DNA を回収した。 PCR-ScriptTMA即 SK(+)クローニングキット (ストラタジーン社) の処方に従い、 回収した DNAをプラス^ドベクター pCR- Script Amp SK(+)へ
サブクローニングした。 これをェシエリヒア コリ (Escher ichia col i) XL- 1 Blue (ストラタジーン) に導入して形質転換した後、 cDNA揷入断片を持つク ローンをアンピシリンおよび X- galを含む LB寒天培地中で選択し、白色を呈 するクローンのみを滅菌したつま楊枝を用いて分離し、 形質転換体 Ε· col i XL- 1 Blue/ラット SLC- 1を得た。 個々のクローンをアンピシリンを含む LB培 地でー晚培養し、 QIA prep8 mini prep (キアゲン社) を用いてプラスミド DNA を調製した。 調製した DNAの一部を用いて制限酵素 Sal Iおよび Spe Iによ る切断を行ない、 挿入されている受容体 cDNA断片の大きさを確認した。塩基 配列の決定のための反応は DyeDeoxy Terminator Cycle Sequence Ki t (パー キンエルマ一社) を用いて行ない、 蛍光式自動シーケンサーを用いて解読し た。 得られた 3クロ一ンの配列を解析し全ての配列が報告されているラット SLC-1タンパク質 (配列番号: 3 ) をコードする cDNA配列 (Lakaye, B. et al . Biochim. Biophys. Acta, Vol . 1401, pp. 216-220 (1998), access ion No. AF08650) の 5, 側に Sal I認識配列が付加し、 3 ' 側に Spe I認識配列が付加 した遺伝子配列と一致することを確認した (配列番号: 4 ) 。 .
参考例 1一 3 ラット SLC- 1発現 CH0細胞の作製
参考例 1一 2で配列が確認されたラット脳由来の SLC- 1の全長アミノ酸配 列をコードし、 5 ' 側に Sal I認識配列が付加し、 また 3' 側に Spe I認識配 列を付加した遺伝子が導入されたプラスミドによって形質転換された!^ col iのクローンより Pl asmid Midi Ki t (キアゲン社) を用いてプラスミドを 調製し、 制限酵素 Sal Iおよび Spe Iで切断してィンサ一ト部分を切り出し た。 インサート DNAは電気泳動後、 ァガ口一スゲルからカミゾリで切り出し、 次に細片化、 フエノ一ル抽出、 フエノ一ル'クロ口ホルム抽出、 エタノ一ル 沈殿を行なって回収した。 このインサート DNAを Sal Iおよび Spe Iで切断 した動物細胞発現用べクタ一プラスミド pAKKO- 111H (Hinuma, S. et al . Biochim. Biophys. Acta, Vol . 1219, pp. 251-259 (1994)記載の pA Ol . 11H と同一のベクタープラスミド) に加え、 T4ライゲ一ス (宝酒造) を用いてラ ィゲ一シヨンを行ない、 蛋白発現用フ。ラスミド pAKKO- SLC-1を構築した。 pAKKO- SLC-1で形質転換した E. col i DH5 (ト一ョ一ポ一)を培養後、 Plasmid
Midi Kit (キアゲン社) を用いて pAKKO- SIX- 1のプラスミド DMを調製した。 これを CellPhect TransfectionKit (アマシャムフアルマシアバイオテク社) を用い添付のプロトコルに従って CHO dhfr細胞に導入した。 10 gの DNA をリン酸カルシウムとの共沈懸濁液とし、 24時間前に 5 X 105または 1 X 106 個の CHO dhfr—細胞を播種した 10 cmシャーレに添加した。 10%ゥシ胎児血清 を含む MEM «培地で 1 日間培養した後、 継代し、 選択培地である 10%透析ゥ シ胎児血清を含む核酸不含 MEM α培地で培養した。 選択培地中で増殖してく る SLC- 1発現 CH0細胞である形質転換細胞のコロニー 56クローンを選択した。 参考例 1—4 全長ラット SLC- 1レセプ夕一蛋白質 mRNAの発現量の高い CH0/ SLC- 1細胞株の選択 ,
参考例 1 _ 3で樹立された CHO/ SLC- 1株 56クローンの全長ラット SLC-1 レセプ夕一蛋白質 mRNAの発現量を CytostarT Plate (アマシャムフアルマシ ァバイオテク社) を用い、 添付のプロトコルに従って以下のように測定した。 CHO/ SLC-1株の各クロ一ンを Cytostar T Plateの各 wellに 2.5 x 104個ず つ播種して 24時間培養した後、 10%ホルマリンによって細胞を固定した。各 wellに 0.25% Tri ton X- 100を添加して細胞の透過性をあげた後、 35Sラベル した配列番号: 5の riboprobeを加えてハイブリダィズさせた。 20 mg/mlの RNaseAを各 wellに加えて遊離の riboprobeを消化し、プレートをよく洗浄し た後、ハイブリダィズした riboprobeの放射活性を Topcounterで測定した。 放射活性の高い株が mRNA発現量が高い。 mRNA発現量の高い 3クローンの中か ら、 特にクローン番号 44を主に用いた。
参考例 1一 5 ヒト SLC- 1 cDNAを含むプラスミドの単離
ヒト胎児脳由来 cDNA library (SUPERSCRIPT™ cDNA Library;GIBC0BRL ¾) を、 Genetrapper cDNA positive selection system (GIBC0BRL社)のマ二ユア ルに従って 、ファージ F1 エンドヌクレアーゼを用いて、 DNAに nickを入れ た後、 ェシエリヒア コリ ェキソヌクレアーゼ . IIIで消化することにより、 1本鎖ヒト胎児脳由来 cDNA libraryを調製した。
Kolakowski Jr.ら ( olakowski Jr., et al (1996) FEBS Lett. Vol. 398, P. 253-258) の報告に基づいて作製した配列番号: 6の合成オリゴヌクレオ
チド (accession No. U71092の 1434- 1451に相当) の 3, 末端に biotin- 14 - dCTPを Terminal Deoxynucleotidyl Transferaseを用いて付加し、 biotin化 オリゴヌクレオチドを調製した。 反応液の組成、 反応時間はマニュアルに従 つた。
1本鎖ヒト胎児脳由来 cDNA 1 ibrary 4 ^ gを 95°Cで 1分保温した後、 氷上 で急冷し、 biotin化オリゴヌクレオチド 20 ngを加え、 37°Cで 1時間、 添付 ハイブリダイゼーションパッファーでハイブリダィズした。 ストレプトァビ ジンビーズを加え、 MAGNA - SEP Magnetic Particle Separator (GIBCOBRL社) を用いて、 biotin化オリゴヌクレオチドにハイブリダィズした 1本鎖ヒト胎 児脳由来 cDNAを単離し、 Kolakowski Jr.らの報告 (Kolakowski Jr., et al (1996) FEBS Lett. Vol. 398, pp. 253-258) に基づいて作製した配列番号: 7の合成オリゴヌクレオチド (accession No. U71092の 1011- 1028に相当) 50ngをプライマ一にしてマニュアルに従って相補鎖を合成し、 2本鎖プラス ミドとした。
参考例 1—6 単離したヒト SLC-1 cDNAを含むプラスミドの塩基配列の決定 参考例 1一 5で得られたプラスミドを ELECTROMAXTMDH10BTMCellsにエレク トロポレーション法で導入して形質転換した後、 cDNA揷入断片を持つクロ一 ンをアンピシリン及び X- galを含む LB寒天培地中で選択し、 白色を呈するク ローンのみを滅菌したつま楊枝でつついて分離し、 形質転換体 ^ coli. DHlOB/hSLC-1を得た。個々のクロ一ンをアンピシリンを含む LB培地でー晚培 養し、 QIA prep8 mini prep (キアゲン社)を用いてプラスミド DNAを精製し た。塩基配列決定のための反応は、 DyeDeoxy Terminator Cycle Sequence Kit (パーキンエルマ一社) を用いて行ない、 蛍光式自動シーケンサーを用いて 解読した。 その結果、 配列番号: 8に示す配列が得られた。 ここに得られた 塩基配列がコードするアミノ酸配列 (配列番号: 9) は、 Lakayeらの報告 (Lakaye, B. et al. (1998) Biochem. Biophys. Acta, vol. 1401, pp. 216-220) において、 ヒト SLC-1の配列を含むヒト染色体 DNA配列 (accession number :Z86090)をもとにしてラット SLC-1から類推された配列として推定さ れていたヒト SLC- 1アミノ酸配列とは異なっており、推定配列のさらに 69及
び 64ァミノ酸上流に開始コドンである ATGが mRNA上で存在することを示し ている。 この配列をコードする DNAを含むプラスミドによる形質転換体 Escherichia coli DH10B/phSLClL8を I F〇および N I BHに寄託した。
参考例 1— 7 ヒト胎児脳由来 cDNAを用いた PCR法によるヒト SL'C- kDMの 増幅
ジ一ントラップ法によりクローニングされたヒト SLC-1 DNA配列を含む プラスミドを铸型とし、 配列番号: 10-および 1 1の合成 DNAプライマーと 配列番号: 12および 13の合成 DNAプライマーを用いて PCR法による増幅. をそれぞれ行なった。 前者の増幅 DNAをヒト SIX- 1(S)と、 後者の増幅 DN Aをヒト SIX- 1(L)と命名した。 合成 DNAプライマーは受容体蛋白に翻訳され る領域の遺伝子が増幅されるように構築したが、その際に遺伝子の 5'側に制 限酵素 Sal Iの認識する塩基配列が付加され、 また 3' 側に制限酵素 Spe I の認識する塩基配列が付加されるように、 5' 側および 3' 側にそれぞれの制 限酵素の認識配列を付加した。 ヒト SLC- 1(S)増幅の反応液の組成は、 ヒト SLC- 1 DNA配列を含むプラスミド錶型 5 a 合成 DNAプライマー各 0.4 M、 0.2 mM dNTPs、 pfuDNAポリメラーゼ 0.5 n 1および酵素に付属のバッ ファーで、総反応量は 50 1とした。増幅のためのサイクルはサーマルサイ クラー (パーキンエルマ一社) を用い、 94°C · 60秒の加熱の後、 94°C · 60秒、 57°C ' 60秒、 72で · 150秒のサイクルを 25回繰り返し、 最後に 72°C ' 10分 保温した。 また、 ヒト SLC- 1(L)増幅の反応液の組成は、 ヒト SLC- 1 DNA配 列を含むプラスミド铸型 5 a 1、合成 DNAプライマー各 0.4 ^ M、0.2mMdNTPs、 pfuDNAポリメラーゼ 0.5 a 1および酵素に付属のパッファーで、総反応量は 50 1とした。 増幅のためのサイクルはサーマルサイクラ一(パーキンエル マー社) を用い、 94°C · 60秒の加熱の後、 94°C ' 60秒、 60°C · 60秒、 72°C · 3分のサイクルを 25回繰り返し、 最後に 72°C · 10分保温した。 増幅産物の 確認は、 0.8%ァガロースゲル電気泳動の後、 ェチジゥムブロマイド染色によ つて行なった。
参考例 1一 8 PCR産物のプラスミドベクターへのサブクローニングおよび 揷入 cDNA部分の塩基配列の解読による増幅 cDNA配列の確認'
参考例 1一 Ίで行なった PCR後の反応産物は 0. 8 %の低融点ァガロースゲ ルを用いて分離し、 バンドの部分を力ミソリで切り出した後、 細片化、 フエ ノール抽出、 フエノール ·クロロホルム抽出、エタノール沈殿を行なって DNA を回収した。 PCR-Script™Amp SK(+)クロ一ニングキット (ストラタジーン社) の処方に従い、 回収した DNAをプラスミドベクタ一 pCR- Script Amp SK(+)へ サブクローニングした。 これをェシエリヒア コリ (Escherichia col i) DH5 competent cel l (トーョーポ一) に導入して形質転換した後、 cDNA揷入断 片を持つクロ一ンをアンピシリンおよび X- galを含む LB寒天培地中で選択し、 白色を呈するクローンのみを滅菌したつま楊枝を用いて分離し、 ヒト SLC - 1 (S)の形質転換体 L coH DH5 a /hSLC-1 (S)とヒト SLC-l (L)の形質転換体 col i藝 α/hSLC- 1 (L)を得た。個々のクローンをアンピシリンを含む LB培地 でー晚培養し、 QIA prep8 mini prep (キアゲン社) を用いてプラスミド DNA を調製した。 調製した DNAの一部を用いて制限酵素 Sal Iおよび Spe Iによ る切断を行ない、 揷入されている受容体 cDNA断片の大きさを確認した。塩基 配列の決定のための反応は DyeDeoxy Terminator Cycle Sequence Ki t (パー キンエルマ一社) を用いて行ない、 蛍光式自動シーケンサーを用いて解読し た。 得られたクローンの配列は、 ヒト SLC-1遺伝子を铸型として配列番号: 1 0および 1 1の合成 DNAプライマーで増幅されるべき D NA配列 (配列番 号: 1 4 ) およびヒト SLC-1遺伝子を铸型として配列番号: 1 2および 1 3 の合成 DNA 7°ライマ一で増幅されるべき D NA配列 (配列番号: 1 5 ) にそ れぞれ一致した。
参考例 1—9 ヒト SLC- 1 (S)発現 CH0細胞およびヒト SLC- 1 (L)発現 CH0細胞 の作製
参考例 1― 8で配列が確認されたヒト SLC- 1 (S)と、 ヒト SLC- 1 (L)が導入さ れたプラスミドによって形質転換された! ^ col iのクロ一ンより Pl asmi d Midi Ki t (キアゲン社) を用いてプラスミドを調製し、 制限酵素 Sal Iおよ び Spe Iで切断してインサート部分を切り出した。 インサート MAは電気泳 動後、 ァガロースゲルからカミゾリで切り出し、 次に細片化、 フエノール抽 出、 フエノール ·クロ口ホルム抽出、 エタノール沈殿を行なって回収した。
このインサート DNAを Sal Iおよび Spe Iで切断した動物細胞発現用べクタ 一プラスミド pAKKO - 111H (Hinuraa, S. et al. Biochim. Biophys. Acta, Vol. 1219, pp. 251-259 (1994)記載の pAKKOl.11Hと同一のベクタ一プラスミド) に加え、 T4ライゲース (宝酒造) を用いてライゲーシヨンを行ない、 蛋白発 現用プラスミド pMKO- hSLC- 1 (S)と pAKKO-hSLC-1 (L)を構築した。
pAKKO-hSLC-1 (S)および pAKKO - hSLC-1 (L)で形質転換した E. coli DH5 (ト ーョ一ポー) を培養後、 Plasmid Midi Kit (キアゲン社) を用いて pAKKO- hSLC-1 (S)と AKKO-hSLC-1 (L)のプラスミド DNAを調製した。これを CellPhect Transfeciion Kit (アマシャムファルマ アバイォテク社) を用い添付のプ ロトコルに従って CHO dhfr細胞に導入した。 10 gの DNAをリン酸カルシ ゥムとの共沈懸濁液とし、 24時間前に 5 X 105または 1 X 106個の CHO dhfr 細胞を播種した 10 cmシャーレに添加した。 10%ゥシ胎児血清を含む MEM α 培地で 1日間培養した後、 継代し、 選択培地である 10%透析ゥシ胎児血清を 含む核酸不含 MEM 培地で培養した。 選択培地中で増殖してくるヒト SLC - KS) 遺伝子導入 CH0細胞である形質転換細胞のコロニー 56クローンおよび、 ヒト SIX- 1(L) 遺伝子導入 CH0細胞である形質転換細 のコロニー 61クロー ンを選択した。
参考例 1一 10 ヒト SLC- 1 (S)およびヒト SLC- 1 (L) mRNAの発現量の高い遺 伝子導入細胞株の選択
参考例 1—9で樹立された CHO/hSLC- 1 (S)株 56クローンおよび CHO/hSLC - 1 (L) 株 61クローンの mRNAの発現量を CytostarTPlate (アマ ャムフアル マシアバイオテク社) を用い、 添付のプロトコルに従って以下のように測定 した。 CHO/hSLC- 1(S)株および CHO/hSLC- 1(L) 株の各クローンを Cytostar T Plateの各 wellに 2.5 x 10
4個ずつ播種して 24時間培養した後、 10%ホルマ リンによって細胞を固定した。 各 wellに 0.25% TritonX- 100を添加して細 胞の透過性をあげた後、 ラベルした配列番号: 16の riboprobeを加えて ハイブリダィズさせた。 20
の1 56 を各 ^11に加ぇて遊離の .. riboprobeを消化し、 プレートをよく洗浄した後、 ハイブリダィズした riboprobeの放射活性を Topcounterで測定した。 放射活性の高い株が mRNA
発現量が高い。 mRNA発現量の高い 7クローンの中から、 特にクローン番号 57を主に用いた。 実験例 1 被験化合物の GIT r 'Sバインディングアツセィを用いたアンタゴ ニス卜活性の測定
参考例 1一 1 0で得られたヒト SLC - 1発現 CH0細胞クローン 57および参考 例 1一 4で得られたラット SLC- 1発現 CH0細胞クローン 44を用いて、以下の 方法により膜画分を調製した。 5 mMEDTA (エチレンジァミン四酢酸)を添加し たリン酸緩衝生理食塩水 (pH 7.4) にヒト、 およびラット SLC- 1発現 CH0細 胞(IxlO8個)を浮遊させ、 遠心した。 細胞のペレットにホモジネートバッファ 一(10 mM NaHC03、 5 mM EDTA、 pH 7.5)を 10 ml加え、 ポリトロンホモジナ ィザーを用いてホモジネートした。 400Xgで 15分間遠心して得られた上清を さらに 100, OOOXgで 1時間遠心し、膜画分の沈澱物を得た。この沈澱物を 2 ml のアツセィバッファ一 [50 mM Trls-HCKpH 7.5)、 1 mM EDTA、 0.1% BSA (ゥ シ血清アルブミン)、 10 iM MgC12、 100 mM NaCK 1 ^ M GDP (グアノシン 5' -二リン酸)、 0.25 mMPMSF (フ土二ルメチルスルホニルフルオラィド)、 1 mg/ml ぺプスタチン、 20 mg/ml ロイぺプチン、 10 mg/ml フォスフオラミドン]に懸 濁し、 100, OOOXgで 1時間遠心した。 沈澱物として回収された膜画分を再び 20 mlのアツセィ バッファーに懸濁し、 分注後 - 80° Cで保存し、 使用の都 度解凍して用いた。
被験化合物のアンタゴニスト活性の測定は以下の通り実施し广こ。 ポリプロ ピレン製の 96穴プレートに、 アツセィバッファーで希釈した SLC-1発現 CH0 細胞膜画分 171 1を分注した後、 DMS0溶液で希釈した 3xl0—¾ MCH 2 1、 種々の濃度に希釈した被験化合物溶液 2 1、 および [35S]— Guanos ine5' -(r -thio) triphosphate (第一化学薬品 社製) 25 1を、 それぞれ添加した(細 胞膜終濃度: 2011 /inK [35S]-Guanosine5,-(ァ- thio) triphosphate終濃度.: 0.33nM)。 この反応液を 25°Cで 1時間、攪拌しながら反応させた後、 グラスフ ィル夕一(GF-C)を用いて吸引ろ過し、 さらに洗浄液 (50mM Tris_HCl緩衝液 pH7.5) 300 1で 3回洗浄した。 グラスフィルタ一に液体シンチレ一夕一を
50ml添加し、残った放射活性を液体シンチレーションカウンターで測定した。 結合阻害率(%) = (化合物と MCHを添加したときの放射活性一 DMS0溶液を 添加したときの放射活性)/ (MCHを添加したときの放射活性一 DMS0溶液を添 加したときの放射活性) X 100として、 結合阻害率 (%) から化合物の IC50 値を算出した。
結果を以下に示す。 化合物番号 阻害活性 (ICS„値: ^ M )
実施例 1 0. 3
実施例 5 0. 02 産業上の利用可能性
化合物 ( I ) 、 ( I,) 、 ( I") .、 (I,") およびそれらの塩は、 優れた M CH受容体拮抗作用を有しており、 肥満症などの予防 ·治療剤として有用で ある。